Clear Sky Science · sv
Salinomycin som en dödsströmbrytare: hur magsäckscancerceller väljer sitt fördärv
Varför denna forskning är viktig för patienter
Magsäckscancer är fortfarande en av världens dödligaste cancerformer, till stor del eftersom många tumörer lär sig att ignorera standardbehandlingar. En stor del av problemet är att tumörer består av många olika celltyper, inklusive en liten men envis grupp kallad cancerstamceller som kan återskapa sjukdomen efter behandling. Denna studie undersöker om ett gammalt veterinärläkemedel, salinomycin, kan omvandlas till ett nytt vapen mot magsäckscancer genom att tvinga dessa celler att dö på mer än ett sätt.
Ett gammalt läkemedel med en ny roll
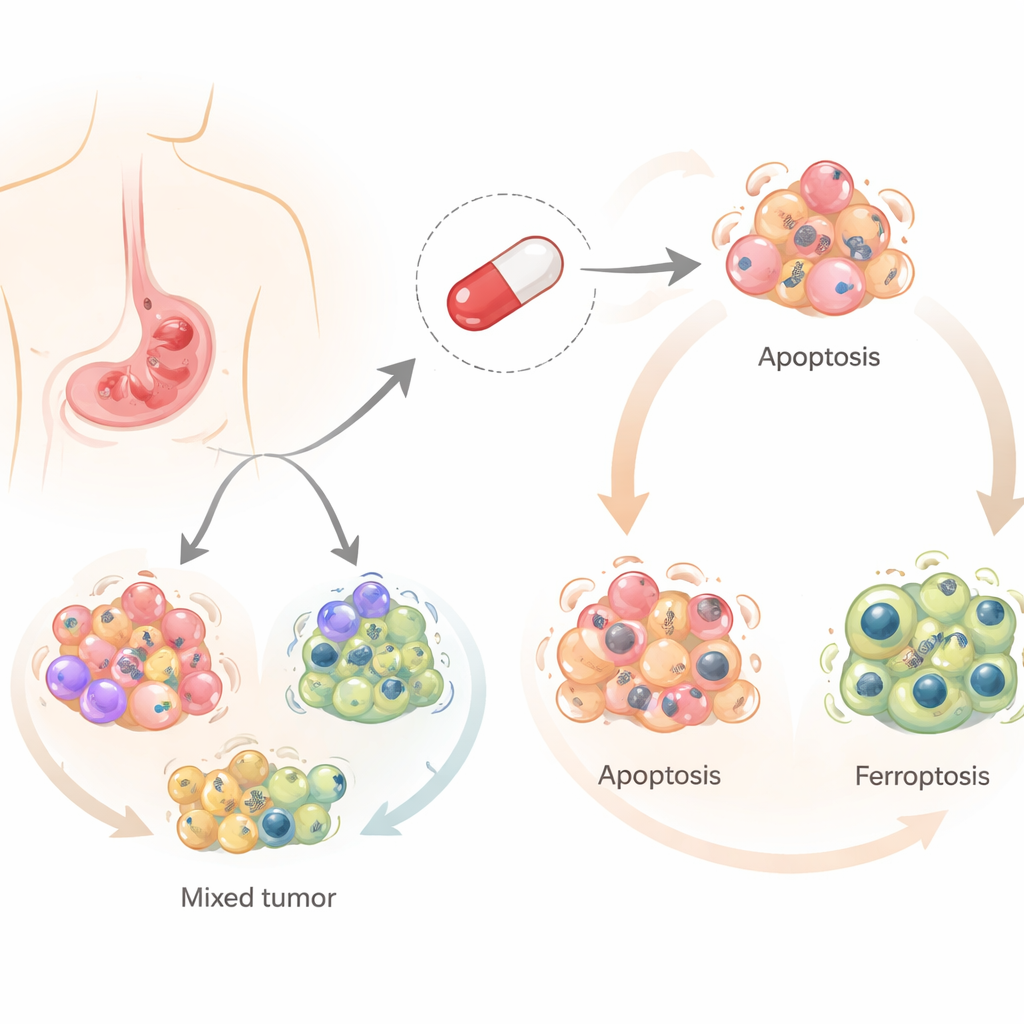
Salinomycin utvecklades ursprungligen för att förebygga infektioner hos produktionsdjur, men under det senaste decenniet har det fått uppmärksamhet för sin förmåga att döda cancerceller, särskilt cancerstamceller. Till skillnad från de flesta cytostatika, som vanligtvis förlitar sig på en huvudmekanism för att döda celler, kan salinomycin utlösa flera kontrollerade former av celldöd. Forskarna fokuserade på tre av dessa: klassisk programmerad celldöd (apoptos), en återvinningsrelaterad process (autofagi) och en nyare, järnberoende dödsform driven av fettskada (ferroptos). Att förstå vilka av dessa vägar som aktiveras i magsäckscancer är viktigt, eftersom tumörer som undviker en väg fortfarande kan vara sårbara för en annan.
Hur tumörceller väljer sitt sätt att dö
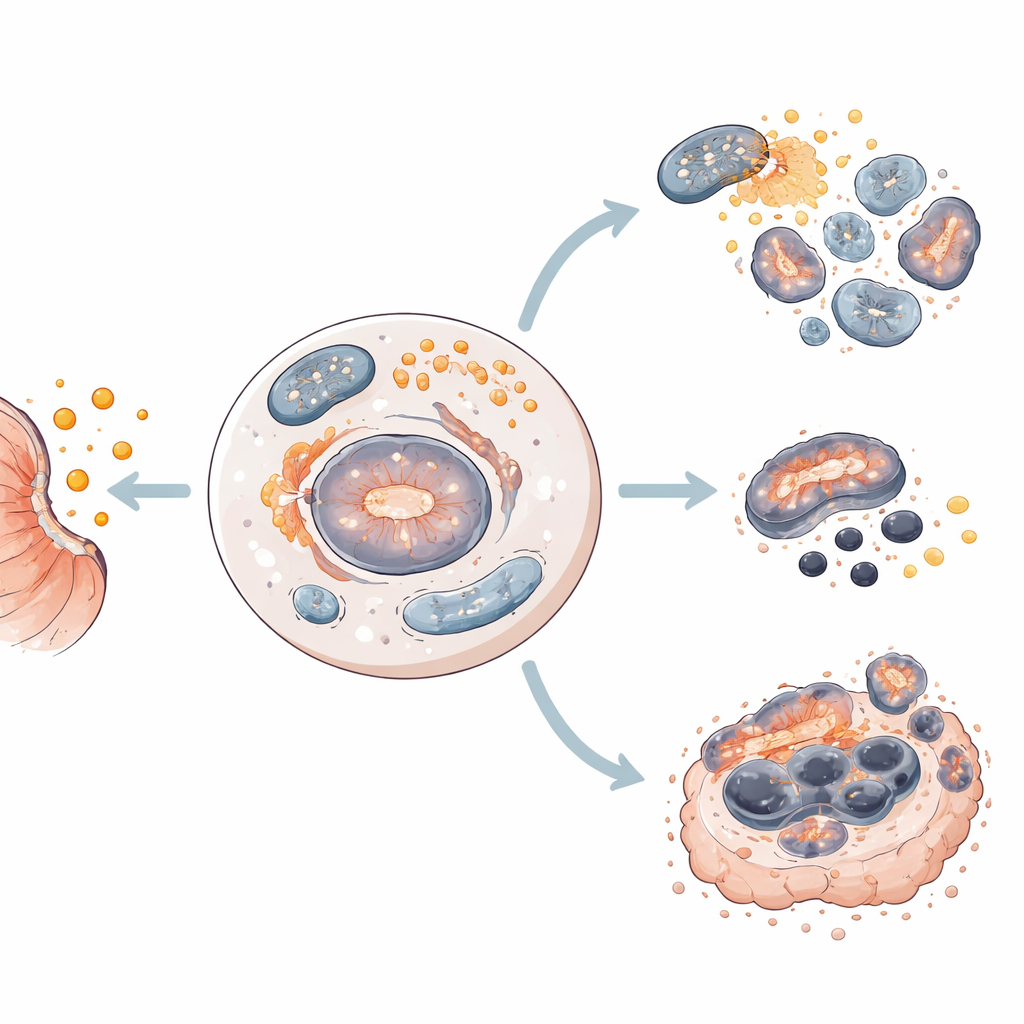
Teamet testade salinomycin på fyra olika humana magsäckscellinjer som representerar den mångfald som ses hos patienter. De fann att samma läkemedel pressade olika celler mot olika öden. I två cellinjer orsakade salinomycin främst apoptos, där celler tyst plockas isär. I de andra två drev det ferroptos, en mer explosiv död kopplad till järn, reaktiva syreföreningar och skada på cellens fetthaltiga komponenter. I samtliga fall slog autofagi på tidigt, vilket tyder på en gemensam utgångspunkt varifrån celler styrs mot den ena eller andra dödsfärden.
Signaler som vägleder dödsbeslutet
Genom att gå djupare mätte forskarna nyckelproteiner som fungerar som trafikljus inuti cellen. I celler på väg mot apoptos dämpade salinomycin tillväxt- och överlevnadssignaler (såsom mTOR och survivin) och aktiverade proteiner som klipper upp cellinnehåll och skadar mitokondrierna, cellens kraftverk. I celler som genomgick ferroptos minskade läkemedlet återigen mTOR och survivin, men undertryckte också två viktiga skyddare mot fettskada, SLC7A11 och GPX4. Genom att analysera genaktivitetsdata identifierade de ett 20-genersmönster som kännetecknar celler predisponerade för ferroptos snarare än apoptos, vilket antyder att varje tumörs molekylära "koppling" bidrar till hur den kommer att ge vika för behandlingen.
Rikta in sig på återfallsrötterna
Studien undersökte också cancerstamceller, identifierade med ytmarkörer CD44 och CD133, vilka är kopplade till läkemedelsresistens och kontroll av ferroptos. I de mest läkemedelsresistenta cellinjerna var dessa stamliknande celler vanliga, bildade robusta 3D "spheroider" och genererade många kolonier. Salinomycin minskade kraftigt andelen celler med dessa markörer, förminskade eller eliminerade spheroider och blockerade koloniutveckling, vilket indikerar att det angriper de celler som mest sannolikt orsakar återfall. När teamet applicerade det ferroptosrelaterade genmönstret på stora patientdatamängder kunde de separera grupper med olika överlevnadsutsikter, vilket visar att detta molekylära fingeravtryck har prognostiskt värde i verkliga sammanhang.
Testa metoden i patientlika mini-tumörer
För att komma närmare klinisk tillämpning testade forskarna salinomycin på patientderiverade magsäckscancerorganoider—små 3D-strukturer odlade från mänskliga tumörprov som efterliknar många egenskaper hos verkliga tumörer. I samtliga organoidmodeller minskade salinomycin livskraften och störde strukturen. I de flesta fall aktiverades apoptotiska enzymer; i en modell som inte visade apoptos utlöstes i stället kännetecken för ferroptos, inklusive förändringar i mitokondriell aktivitet och förlust av skyddande ferroptosproteiner. Autofagi ökade i alla modeller, vilket förstärker dess roll som ett gemensamt tidigt steg i salinomycininducerad celldöd.
Vad detta kan innebära för framtida behandling
Sammantaget skildrar detta arbete salinomycin som en "dödsströmbrytare" som kan få magsäckscancerceller att gå in i antingen apoptotisk eller ferroptotisk självförintelse, med autofagi som en gemensam förspel. Genom att samtidigt slå mot bulk-tumören och dess stamliknande kärna, och genom att erbjuda en alternativ dödsväg när den vanliga är blockerad, kan salinomycin hjälpa till att övervinna multidrogresistens. Det ferroptosbaserade gensignatur som utvecklats här skulle kunna hjälpa läkare att identifiera vilka patienter som sannolikt gynnas, och därigenom öppna dörren för mer personligt anpassade och hållbara behandlingsstrategier för magsäckscancer.
Citering: Laurenziello, P., Luongo, M., Lospinoso Severini, F. et al. Salinomycin as a death switch: how gastric cancer cells choose their demise. Cell Death Discov. 12, 171 (2026). https://doi.org/10.1038/s41420-026-03058-2
Nyckelord: magsäckscancer, salinomycin, cancerstamceller, ferroptos, läkemedelsresistens