Clear Sky Science · ar
السالينوميسين كمفتاح للموت: كيف تختار خلايا سرطان المعدة مصيرها
لماذا تهمّ هذه الدراسة المرضى
لا يزال سرطان المعدة واحداً من أخطر السرطانات في العالم، ويرجع ذلك إلى حد كبير إلى أن العديد من الأورام تتعلم تجاهل الأدوية القياسية. جزء كبير من المشكلة هو أن الورم يتكوّن من أنواع خلايا متنوعة، بما في ذلك مجموعة صغيرة لكنها عنيدة تُدعى الخلايا الجذعية السرطانية التي يمكنها إعادة تشغيل المرض بعد العلاج. تستقصي هذه الدراسة ما إذا كان يمكن تحويل دواء بيطري قديم، السالينوميسين، إلى سلاح جديد ضد سرطان المعدة عن طريق إجبار هذه الخلايا على الموت عبر أكثر من مسار واحد.
دواء قديم لوظيفة جديدة
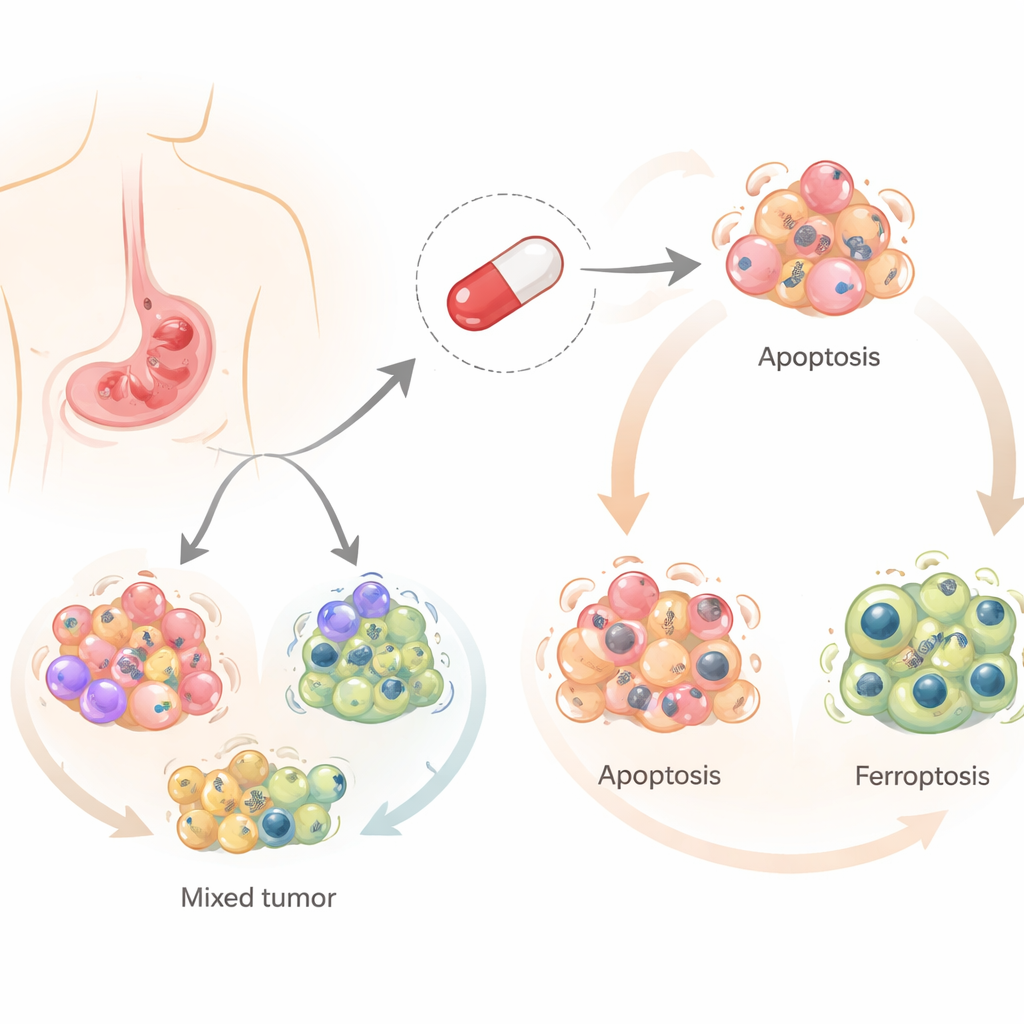
طُوّر السالينوميسين أصلاً لمنع العدوى في الحيوانات المزارعية، لكن خلال العقد الماضي لفت الانتباه بقدرته على قتل الخلايا السرطانية، لا سيما الخلايا الجذعية السرطانية. على عكس معظم أدوية العلاج الكيميائي التي تعتمد عادة على مسار رئيسي واحد لقتل الخلايا، يمكن للسالينوميسين أن يفعّل عدة أشكال منظمة للموت الخلوي. ركّز الباحثون على ثلاثة من هذه المسارات: الموت المبرمج الكلاسيكي (الاستماتة أو apoptosis)، وعملية إعادة التدوير الخلوية (الالتهام الذاتي أو autophagy)، ونوع أحدث من الموت المعتمد على الحديد وينجم عن تلف الدهون (الفيروبتوزيس). فهم أي من هذه المسارات يُفعّل في سرطان المعدة مهم، لأن الأورام التي تتفادى مسارًا واحدًا قد تظل عرضة لمسار آخر.
كيف تختار خلايا الورم طريقها إلى الموت
اختبر الفريق السالينوميسين على أربع سلالات خلوية بشرية لسرطان المعدة تمثل التنوع المرصود لدى المرضى. وجدوا أن الدواء نفسه دفع خلايا مختلفة نحو مصائر مختلفة. في سلالتين خلويتين، تسبب السالينوميسين أساساً في الاستماتة، حيث تفكك الخلايا نفسها بهدوء. في السلالتين الأخريين، دفع نحو الفيروبتوزيس، وهو موت أكثر انفجاراً مرتبط بالحديد وجزيئات الأكسدة التفاعلية وتلف المكونات الدهنية في الخلية. في كل الحالات، اندلع الالتهام الذاتي مبكراً، مما يشير إلى نقطة انطلاق مشتركة تُوجّه منها الخلايا نحو أحد مسارات الموت أو الآخر.
الإشارات التي توجه قرار الموت
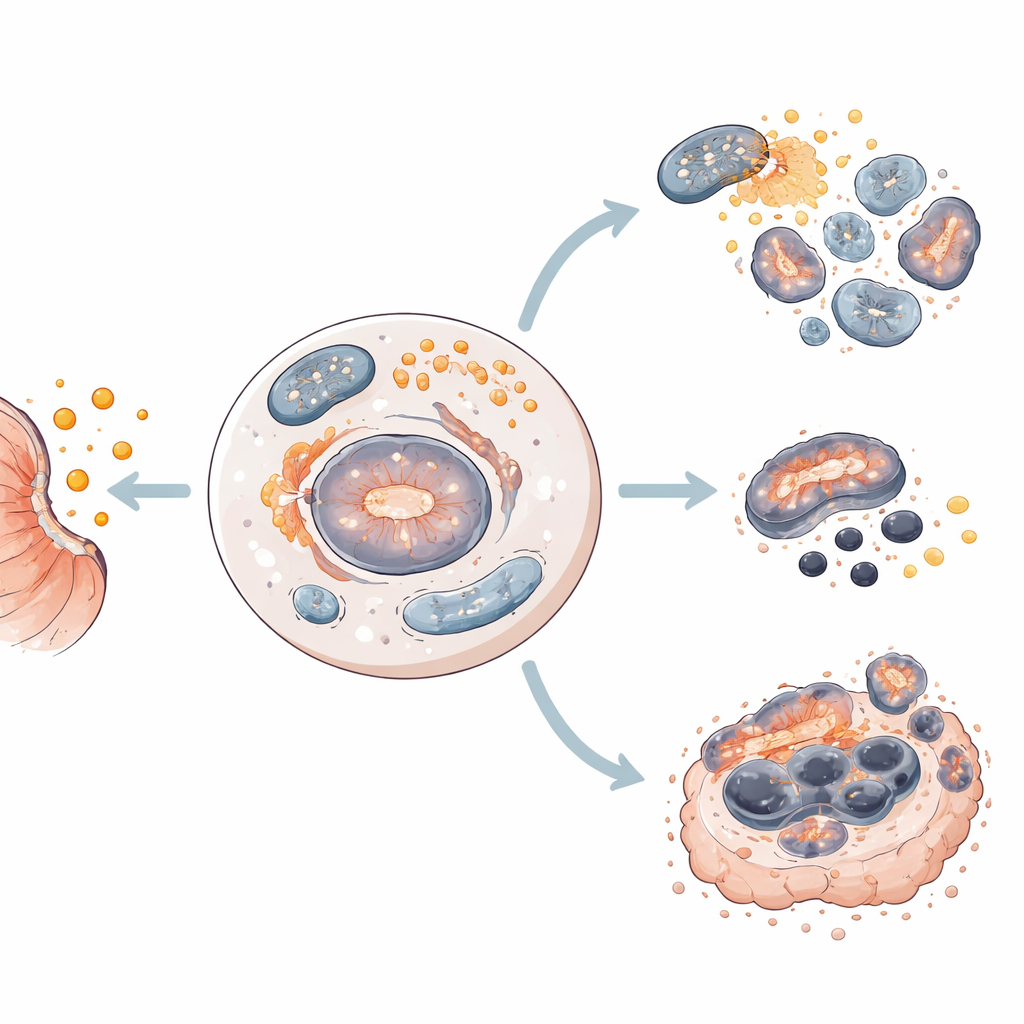
بتعمّق أكبر، قاس الباحثون بروتينات رئيسية تعمل كإشارات مرورية داخل الخلية. في الخلايا المتجهة نحو الاستماتة، قلّل السالينوميسين إشارات النمو والبقاء (مثل mTOR وsurvivin) وفعّل بروتينات تقطع محتويات الخلية وتلحق أضراراً بالميتوكندريا، محطات طاقة الخلية. في الخلايا التي تخضع للفيروبتوزيس، خفّض الدواء أيضاً mTOR وsurvivin، لكنه قمع أيضاً حامين مهمين ضد تلف الدهون، SLC7A11 وGPX4. من خلال تحليل بيانات تعبير الجينات، حدّدوا نمطًا مكونًا من 20 جينًا يميّز الخلايا الميّالة نحو الفيروبتوزيس بدلاً من الاستماتة، ما يشير إلى أن "الأسلاك" الجزيئية لكل ورم تساعد في تحديد كيف ستنهار استجابةً للعلاج.
استهداف جذور الانتكاس
فحصت الدراسة أيضاً الخلايا الجذعية السرطانية، المحدّدة بواسطة علامات سطحية CD44 وCD133، المرتبطة بمقاومة الأدوية وتنظيم الفيروبتوزيس. في أكثر السلالات مقاومة للأدوية، كانت هذه الخلايا الشبيهة بالجذور منتشرة، كونت "كرات" ثلاثية الأبعاد متينة، وأنشأت مستعمرات كثيرة. قلّل السالينوميسين بشكل حاد من نسبة الخلايا الحاملة لهذه العلامات، صغّر أو قضى على الكرات، وعرقل نمو المستعمرات، مما يشير إلى أنه يهاجم الخلايا الأكثر احتمالاً للتسبب في الانتكاس. عندما طبّق الفريق نمط الجينات المرتبط بالفيروبتوزيس على مجموعات بيانات كبيرة للمرضى، تمكنوا من فصل مجموعات لها توقعات بقاء مختلفة، مما يظهر أن بصمة الجينات هذه لها قيمة توقعية في العالم الحقيقي.
اختبار الطريقة في أورام مصغرة شبيهة بالمرضى
للاقتراب من التطبيق السريري، اختبر الباحثون السالينوميسين على أورغانويدات مأخوذة من مرضى بسرطان المعدة — هياكل ثلاثية الأبعاد صغيرة مزروعة من عينات أورام بشرية تحاكي الكثير من خصائص الأورام الحقيقية. عبر جميع نماذج الأورغانويد، قلّل السالينوميسين من الحيوية وعرّض البنية للتشوه. في معظم الحالات فعّل إنزيمات الاستماتة؛ في نموذج واحد لم يظهر الاستماتة، أطلق بدلاً من ذلك علامات الفيروبتوزيس، بما في ذلك تغيّرات في نشاط الميتوكندريا وفقدان بروتينات الحماية من الفيروبتوزيس. ازداد الالتهام الذاتي في جميع النماذج، مما يعزّز دوره كخطوة مبكرة مشتركة في موت الخلايا المستحث بالسالينوميسين.
ماذا قد يعني هذا للعلاج المستقبلي
بشكل إجمالي، يصور هذا العمل السالينوميسين كمفتاح "للموت" يمكنه قلب خلايا سرطان المعدة نحو تدمير ذاتي إما باستيماتة أو بفيروبتوزيس، مع الالتهام الذاتي كمقدمة مشتركة. من خلال استهداف كل من الورم الكتلي وجذره الشبيه بالخلايا الجذعية، ومن خلال توفير مسار موت بديل عندما يُحجب المسار المعتاد، قد يساعد السالينوميسين على التغلب على مقاومة الأدوية المتعددة. يمكن أن يساعد توقيع الجينات القائم على الفيروبتوزيس المطوّر هنا الأطباء في تحديد المرضى الأكثر احتمالاً للاستفادة، فاتحًا الباب أمام استراتيجيات علاجية أكثر تخصيصًا وديمومة لسرطان المعدة.
الاستشهاد: Laurenziello, P., Luongo, M., Lospinoso Severini, F. et al. Salinomycin as a death switch: how gastric cancer cells choose their demise. Cell Death Discov. 12, 171 (2026). https://doi.org/10.1038/s41420-026-03058-2
الكلمات المفتاحية: سرطان المعدة, السالينوميسين, خلايا سرطان جذعية, الفيروبتوزيس, مقاومة الأدوية