Clear Sky Science · zh
α2δ4功能障碍通过扰乱突触线粒体与钙信号互作导致光感受器退化
这项眼科研究为何重要
由视网膜退化引起的视力丧失通常是永久性的,能真正保护眼睛感光细胞的治疗手段仍然稀缺。本研究提出了一个根本性问题:视网膜中细胞连接处的微小问题如何逐步累积,最终导致这些细胞死亡并引发失明?通过追踪在某些遗传性视力障碍患者中发现的一种特定基因缺陷,作者揭示了一个出人意料的元凶——位于光感受器神经末梢的小型能量工厂(线粒体)——并描绘了突触处受扰乱的钙信号如何逐步破坏整个细胞的健康。
从夜间视力缺陷到感光器死亡
这项工作聚焦于将光转化为电信号的光感受器——杆细胞和锥细胞。在细胞基部,这些细胞形成专门的突触,持续向下游神经元释放化学信号。名为α2δ4的蛋白有助于在这些突触处组装并稳定一种钙通道复合体(Cav1.4),其基因突变已与人类视网膜营养不良有关。患者通常早期出现从光感受器到双极细胞的信号传递问题,但许多年内光感受器数量并不会大幅减少。研究人员使用敲除α2δ4的小鼠,旨在理解表面上“局部”的突触缺陷如何最终导致含有光感受器细胞体的层缓慢变薄。
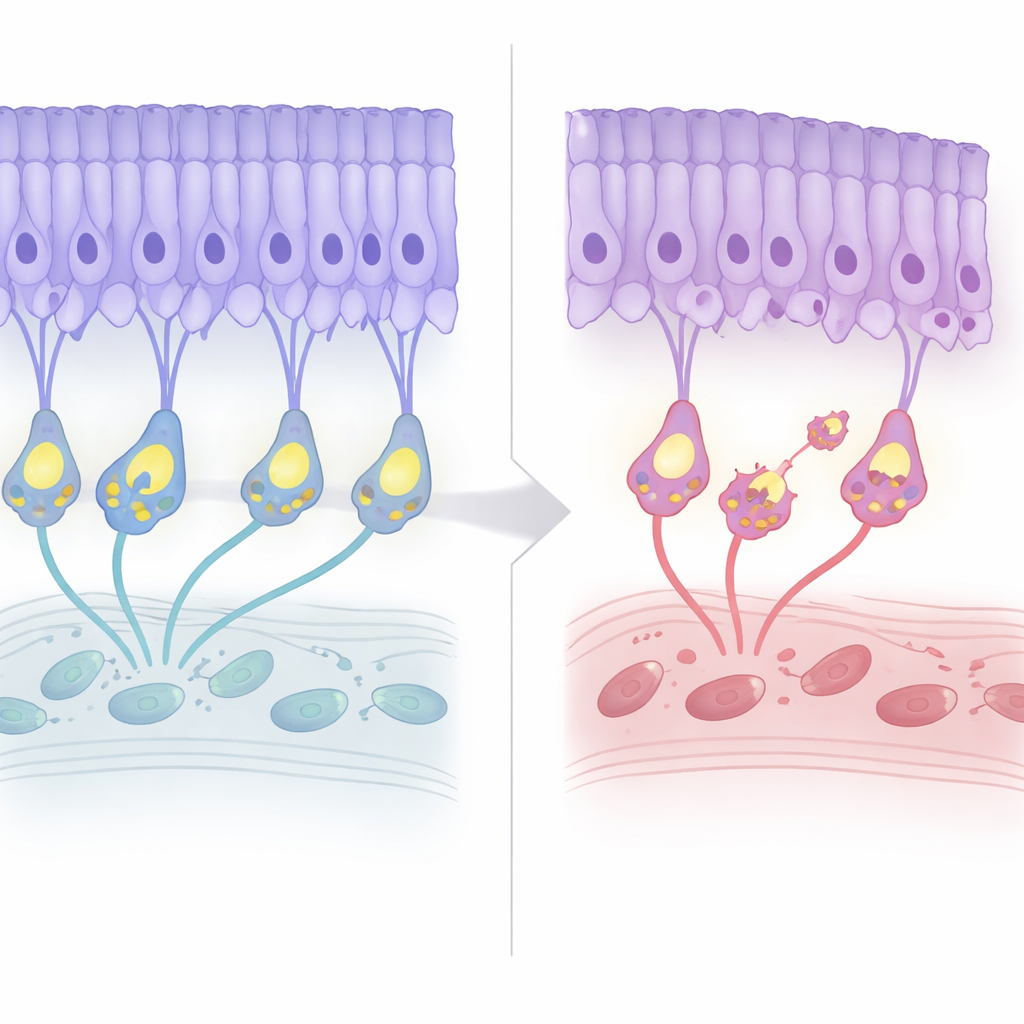
缓慢的结构衰退与早期预警信号
研究组在小鼠整个寿命期内追踪其视网膜。头几个月总体结构看起来正常,电生理记录也表明光的感知在很大程度上保持完整。然而在大约七个月龄时,光感受器细胞核所在的层开始变薄约20%,随后趋于平台期,这与患者中观察到的轻度、起病较晚的退化相呼应。有趣的是,程序性细胞死亡的标志物较早出现,早于明显的细胞丧失。与此同时,“接线”发生重组:光感受器突触端从其常处的层回缩,双极细胞的树突向上生长以与之接触,形成异位连接。尽管发生了这种重塑,突触传递效率——以下游与上游电信号的比值判断——保持稳定但较差,并未随年龄显著恶化。
突触处的能量工厂承受压力
为探查细胞死亡前发生了什么,作者比较了年轻突变体与正常视网膜的蛋白组成。最显著的早期变化是三羧酸(TCA)循环组成成分的广泛下降,TCA循环是产生能量的核心通路。显微镜观察证实,承载该循环的细胞器——线粒体,在光感受器突触处受到尤其严重的影响。在健康小鼠中,这些突触端有显著的线粒体;而在缺失α2δ4的动物中,突触线粒体明显更小、数量更少,尤其是在锥细胞突触端,这种变化远在大范围退化之前就已出现。突触层中的线粒体标志物下降,有些线粒体似乎被错位到光感受器细胞核所在层。相比之下,细胞的内节——光感受器的主要代谢枢纽——中的线粒体在早期相对保存,突显了突触线粒体的特殊脆弱性。
细胞区室之间破碎的钙“对话”
因为α2δ4是钙通道复合体的一部分,研究组检验了钙处理异常是否可能是线粒体问题的根源。在健康光感受器中,通过突触处Cav1.4通道进入的钙与内质网(ER)的储存与释放以及线粒体的摄取紧密协调,形成将电活动与能量供应连接起来的微电路。在突变小鼠中,从ER释放钙的蛋白(例如Ryanodine受体RYR2)和关键的线粒体钙转运蛋白(MCU)在突触层中特异性减少。内质网应激的标志上升,表明该区室也承受压力。这些变化共同指向在突触发生信号传递的部位,细胞膜、内质网与线粒体之间局部钙“互通”发生了崩溃。
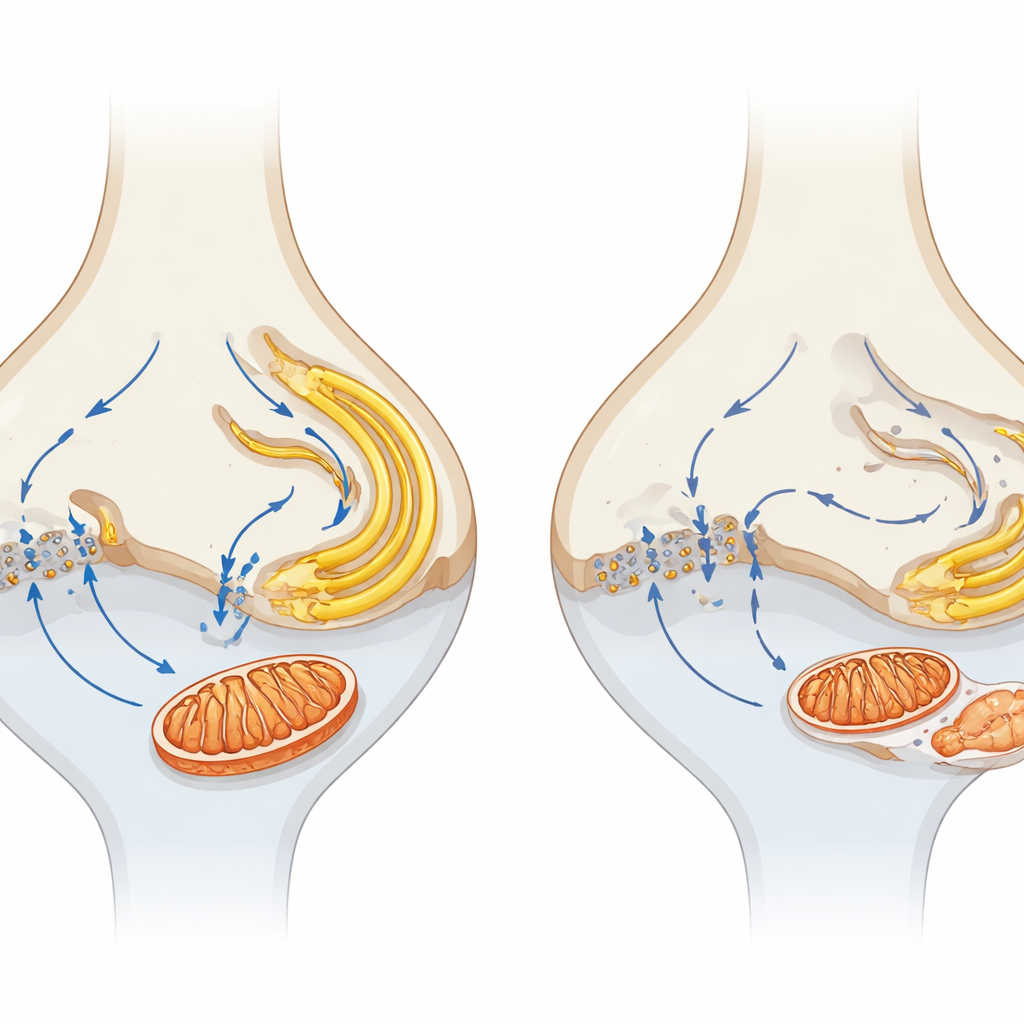
将微小突触缺陷与长期视力丧失连接起来
通过比较α2δ4敲除小鼠与完全缺失Cav1.4通道的动物,作者发现更严重的通道破坏会导致更快且更强的退化,强化了钙进入的核心作用。他们提出了一个模型:α2δ4的丧失削弱了Cav1.4的功能,扰乱了突触处的钙流并使其与附近的内质网和线粒体解耦。随着时间推移,这导致突触线粒体受损、能量生成受损以及内膜应激,这些共同使光感受器逐步陷入缓慢的进行性死亡。对非专业读者来说,关键见解是健康视力不仅依赖于光感受器的存在,还依赖于维持其细小突触“发电厂”和钙信号的精细调控;针对这些早期、局部的变化可能为保存多种视网膜疾病中的视力提供新的策略。
引用: Amieghemen, C.I., Ung, T.T., Huskin, G.N. et al. Dysfunction of α2δ4 leads to photoreceptor degeneration through disrupted synaptic mitochondria and calcium crosstalk. Cell Death Dis 17, 337 (2026). https://doi.org/10.1038/s41419-026-08587-3
关键词: 视网膜退化, 光感受器, 线粒体, 钙信号, 突触功能障碍