Clear Sky Science · pl
Dysfunkcja α2δ4 prowadzi do degeneracji fotoreceptorów przez zaburzone mitochondria synaptyczne i krzyżowanie sygnałów wapniowych
Dlaczego te badania nad oczami są istotne
Utrata wzroku wskutek degeneracji siatkówki jest zwykle nieodwracalna, a skuteczne terapie chroniące komórki światłoczułe oka wciąż są nieliczne. W badaniu postawiono podstawowe pytanie: w jaki sposób drobne problemy na połączeniach między komórkami w siatkówce mogą stopniowo eskalować i prowadzić do śmierci tych komórek, a ostatecznie do ślepoty? Śledząc konkretną wadę genetyczną występującą u niektórych osób z dziedzicznymi zaburzeniami wzroku, autorzy ujawniają niespodziewanego winowajcę — małe elektrownie na zakończeniach nerwowych fotoreceptorów — i odtwarzają, jak zaburzone sygnały wapniowe w synapsach mogą stopniowo podkopywać zdrowie całej komórki.
Od wad widzenia nocnego do obumierających detektorów światła
Praca koncentruje się na fotoreceptorach — pręcikach i czopkach, które przekształcają światło w sygnały elektryczne. U ich podstaw komórki te tworzą wyspecjalizowane synapsy, które nieustannie uwalniają sygnały chemiczne do neuronów następnych stopni. Białko o nazwie α2δ4 pomaga składać i stabilizować kompleks kanału wapniowego (Cav1.4) w tych synapsach, a mutacje w jego genie powiązano z ludzkimi dystrofiami siatkówki. Pacjenci często mają wczesne trudności z przekazywaniem sygnałów od fotoreceptorów do komórek bipolarowych, ale przez wiele lat mogą nie tracić znacznej liczby fotoreceptorów. Używając myszy zmodyfikowanych tak, by brakowało im α2δ4, badacze postanowili zrozumieć, jak pozornie „lokalna” wada synaptyczna prowadzi ostatecznie do powolnego przerzedzenia warstwy zawierającej ciała komórek fotoreceptorów.
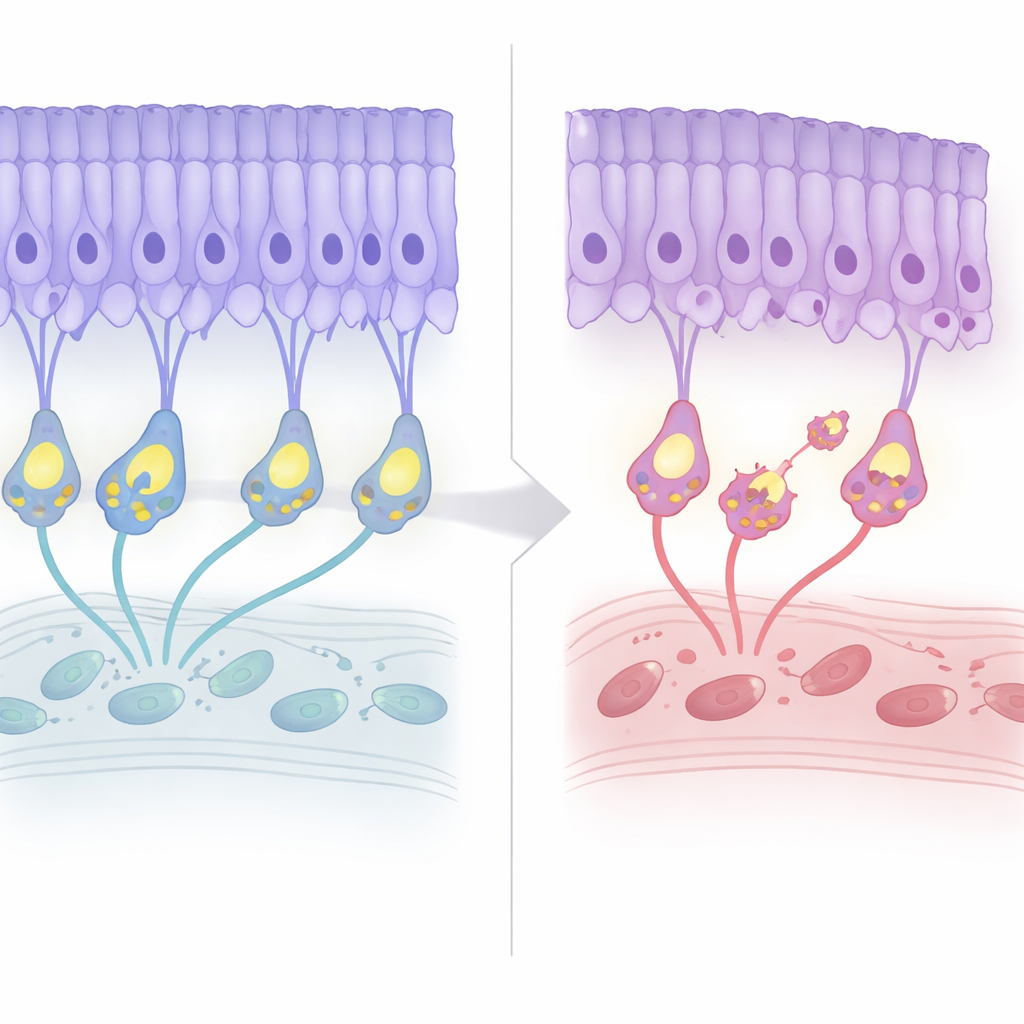
Powolny spadek strukturalny z wczesnymi ostrzeżeniami
Zespół śledził siatkówki tych myszy przez całe ich życie. Przez pierwsze kilka miesięcy ogólna architektura wydawała się normalna, a zapisy elektryczne sugerowały, że samo wykrywanie światła pozostawało w dużej mierze nienaruszone. Około siódmego miesiąca życia jednak warstwa jąder fotoreceptorów zaczęła się przerzedzać o około 20 procent, a następnie ustabilizowała się, odzwierciedlając łagodną degenerację o późnym początku obserwowaną u pacjentów. Co ciekawe, markery zaprogramowanej śmierci komórkowej pojawiały się wcześniej, zanim nastąpiła oczywista utrata komórek. W tym samym czasie „okablowanie” zostało przeorganizowane: zakończenia fotoreceptorów cofały się z ich zwykłej warstwy, a dendryty komórek bipolarowych wydłużały się ku górze, by się z nimi zetknąć, tworząc ektopowe połączenia. Pomimo tej przebudowy wydajność transmisji synaptycznej — mierzona stosunkiem sygnałów zstępujących do wstępujących — pozostawała trwale niska, lecz nie pogarszała się z biegiem wieku.
Elektrownie synaptyczne pod stresem
Aby zbadać, co dzieje się przed śmiercią komórek, autorzy porównali skład białkowy młodych siatkówk mutantów i normalnych myszy. Najbardziej uderzającą wczesną zmianą był szeroki spadek komponentów cyklu kwasu trójkarboksylowego (TCA), kluczowej ścieżki wytwarzania energii. Mikroskopia potwierdziła, że mitochondria — organelle, w których zachodzi ten cykl — były szczególnie dotknięte w synapsach fotoreceptorów. U zdrowych myszy te zakończenia zawierają wyraźne mitochondria; u zwierząt pozbawionych α2δ4 mitochondria synaptyczne były wyraźnie mniejsze i rzadsze, szczególnie w zakończeniach czopków, na długo przed szeroko zakrojoną degeneracją. Markery mitochondriów w warstwie synaptycznej spadły, a niektóre mitochondria wydawały się przesunięte do warstwy jąder fotoreceptorów. Dla kontrastu, mitochondria w segmencie wewnętrznym — głównym centrum metabolicznym fotoreceptora — były relatywnie zachowane we wczesnym okresie, co podkreśla szczególną podatność mitochondriów synaptycznych.
Złamane „rozmowy” wapniowe między przedziałami komórkowymi
Ponieważ α2δ4 jest częścią kompleksu kanału wapniowego, zespół sprawdził, czy zaburzone gospodarowanie wapniem może leżeć u podstaw problemów z mitochondriami. W zdrowych fotoreceptorach wapń wchodzący przez kanały Cav1.4 w synapsie jest ściśle skoordynowany z magazynowaniem i uwalnianiem wapnia przez siateczkę endoplazmatyczną (ER) oraz wychwytem przez mitochondria, tworząc mikroukład łączący aktywność elektryczną z dostawą energii. U myszy mutantów białka odpowiadające za uwalnianie wapnia z ER (takie jak receptor ryanodynowy RYR2) oraz kluczowy transporter wapnia mitochondrialnego (MCU) były specyficznie zmniejszone w warstwie synaptycznej. Markery stresu w ER były podwyższone, co sugeruje, że ten przedział także był pod obciążeniem. Razem te zmiany wskazują na załamanie lokalnego „krzyżowania” sygnałów wapniowych między błoną komórkową, ER i mitochondriami dokładnie tam, gdzie odbywa się przekazywanie synaptyczne.
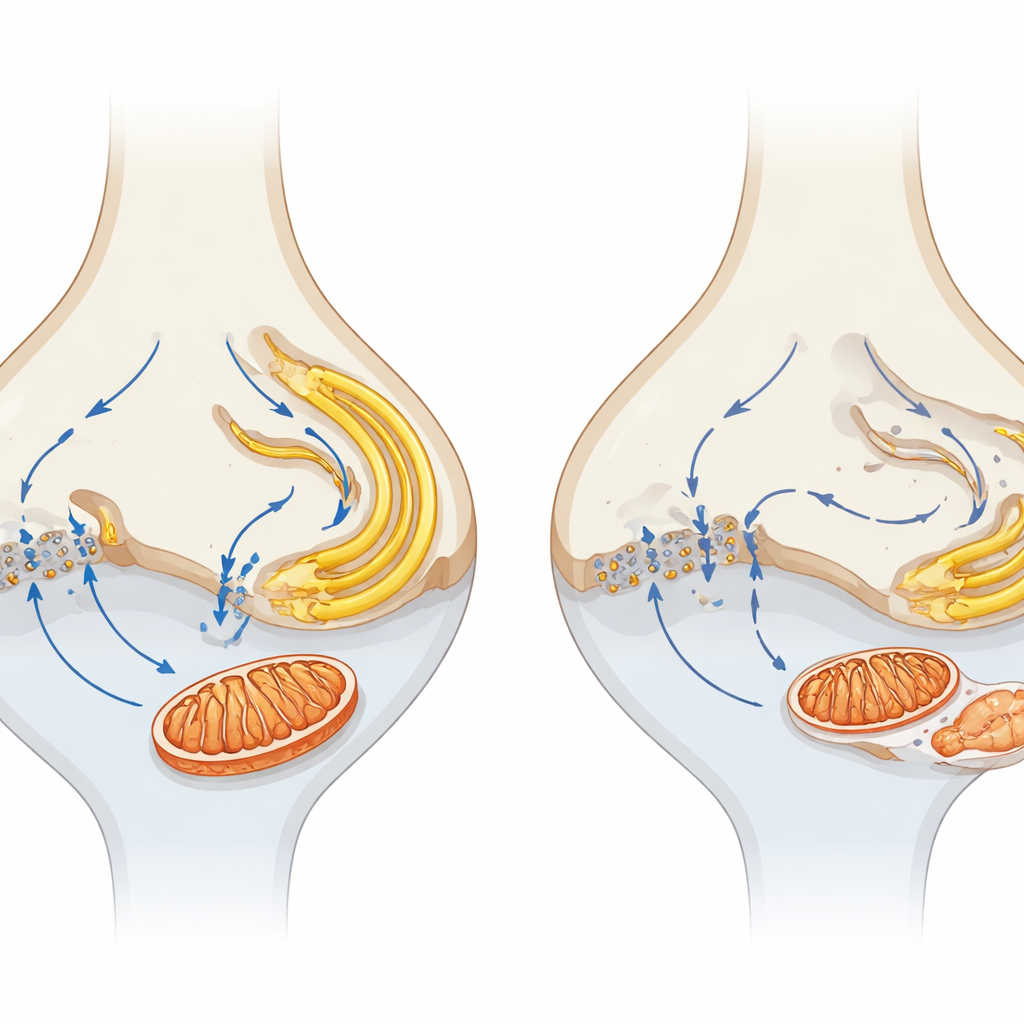
Łączenie malutkich synaps ze długoterminową utratą wzroku
Porównując myszy z wyciętym genem α2δ4 z osobnikami całkowicie pozbawionymi kanału Cav1.4, autorzy stwierdzili, że bardziej poważne zaburzenie kanału prowadzi do szybszej i silniejszej degeneracji, co wzmacnia centralną rolę napływu wapnia. Proponują model, w którym utrata α2δ4 osłabia funkcję Cav1.4, zaburzając przepływ wapnia w synapsie i rozłączając go z pobliskim ER i mitochondriami. Z czasem prowadzi to do uszkodzenia mitochondriów synaptycznych, upośledzenia produkcji energii i stresu wewnętrznych błon, które łącznie predysponują fotoreceptory do powolnej, postępującej śmierci. Dla czytelnika nietechnicznego kluczowy wniosek jest taki, że zdrowe widzenie zależy nie tylko od obecności fotoreceptorów, lecz także od utrzymania ich małych, synaptycznych elektrowni i precyzyjnych sygnałów wapniowych; ukierunkowanie na te wczesne, lokalne zmiany może otworzyć nowe strategie zachowania wzroku w szerokim spektrum chorób siatkówki.
Cytowanie: Amieghemen, C.I., Ung, T.T., Huskin, G.N. et al. Dysfunction of α2δ4 leads to photoreceptor degeneration through disrupted synaptic mitochondria and calcium crosstalk. Cell Death Dis 17, 337 (2026). https://doi.org/10.1038/s41419-026-08587-3
Słowa kluczowe: degeneracja siatkówki, fotoreceptory, mitochondria, sygnalizacja wapniowa, dysfunkcja synaptyczna