Clear Sky Science · es
La disfunción de α2δ4 provoca degeneración de los fotorreceptores mediante la alteración de las mitocondrias sinápticas y el intercambio de calcio
Por qué importa esta investigación ocular
La pérdida de visión por degeneración retiniana suele ser irreversible, y los tratamientos que protegen realmente a las células sensibles a la luz del ojo siguen siendo escasos. Este estudio plantea una pregunta fundamental: ¿cómo pueden pequeños problemas en las conexiones entre las células de la retina convertirse lentamente en la muerte de esas células y, en última instancia, en ceguera? Siguiendo un defecto genético concreto presente en algunas personas con trastornos visuales hereditarios, los autores revelan a un culpable inesperado: pequeñas centrales energéticas en las terminaciones nerviosas de los fotorreceptores, y trazan cómo las señales de calcio perturbadas en las sinapsis pueden socavar gradualmente la salud de toda la célula.
De la visión nocturna defectuosa a la muerte de los sensores de luz
El trabajo se centra en los fotorreceptores, los bastones y conos que convierten la luz en señales eléctricas. En su base, estas células forman sinapsis especializadas que liberan continuamente señales químicas hacia las neuronas siguientes. Una proteína llamada α2δ4 ayuda a ensamblar y estabilizar un complejo de canales de calcio (Cav1.4) en estas sinapsis, y las mutaciones en su gen se han asociado con distrofias retinianas humanas. Los pacientes a menudo muestran problemas tempranos en la transmisión de las señales desde los fotorreceptores a las células bipolares, pero pueden no perder un gran número de fotorreceptores durante muchos años. Usando ratones diseñados para carecer de α2δ4, los investigadores buscaron comprender cómo un defecto sináptico aparentemente “local” conduce con el tiempo al adelgazamiento lento de la capa que contiene los cuerpos celulares de los fotorreceptores.
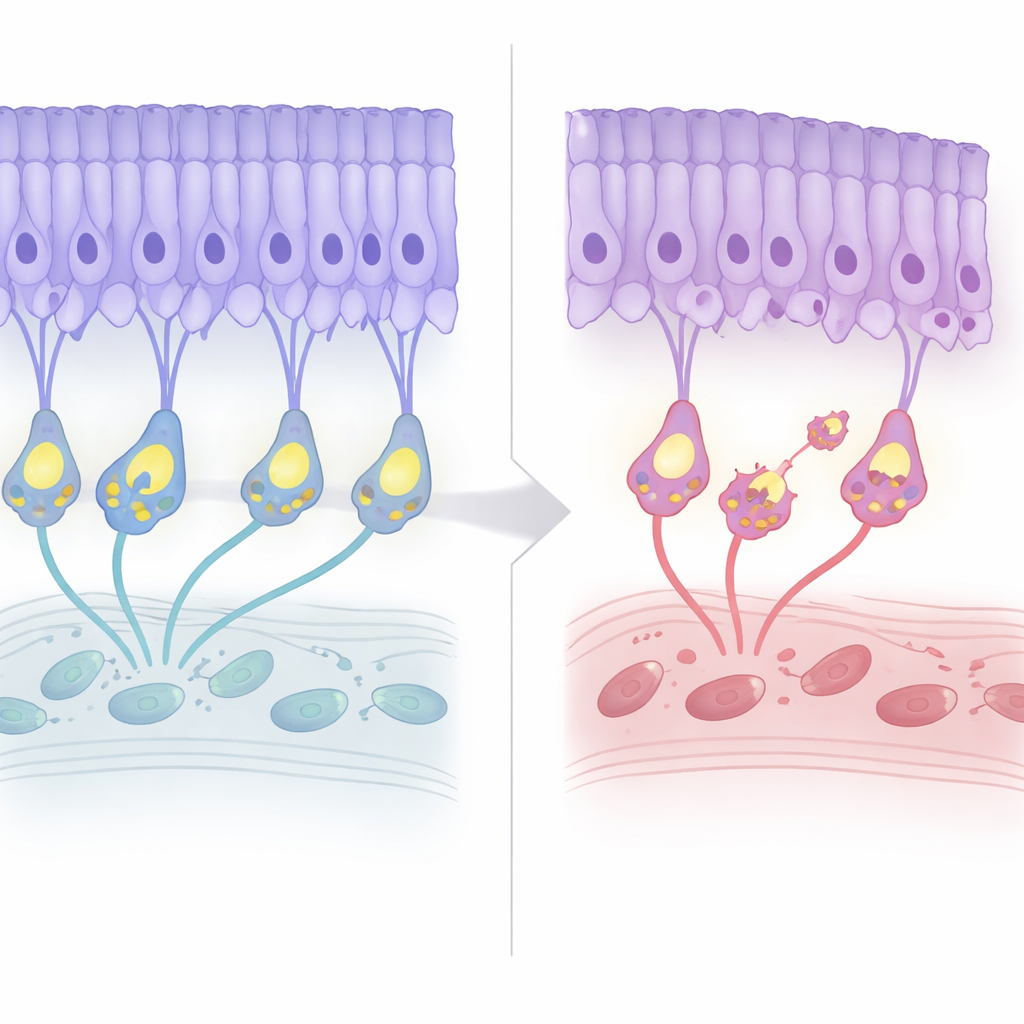
Declive estructural lento con señales de advertencia tempranas
El equipo siguió las retinas de estos ratones a lo largo de su vida. Durante los primeros meses, la arquitectura general parecía normal y los registros eléctricos sugerían que la detección de la luz permanecía en gran medida intacta. Sin embargo, alrededor de los siete meses de edad, la capa de núcleos de los fotorreceptores comenzó a adelgazar en aproximadamente un 20 por ciento y luego se estabilizó, reflejando la degeneración leve y de aparición tardía observada en pacientes. Curiosamente, los marcadores de muerte celular programada aparecieron antes, antes de la pérdida celular evidente. Al mismo tiempo, el “cableado” se reorganizó: las terminales de los fotorreceptores se retiraron de su capa habitual y las dendritas de las células bipolares brotaron hacia arriba para encontrarlas, formando conexiones ectópicas. A pesar de este remodelado, la eficiencia de la transmisión sináptica —según la proporción de señales eléctricas aguas abajo frente a aguas arriba— permaneció de forma persistentemente baja pero no empeoró con la edad.
Las centrales energéticas sinápticas bajo estrés
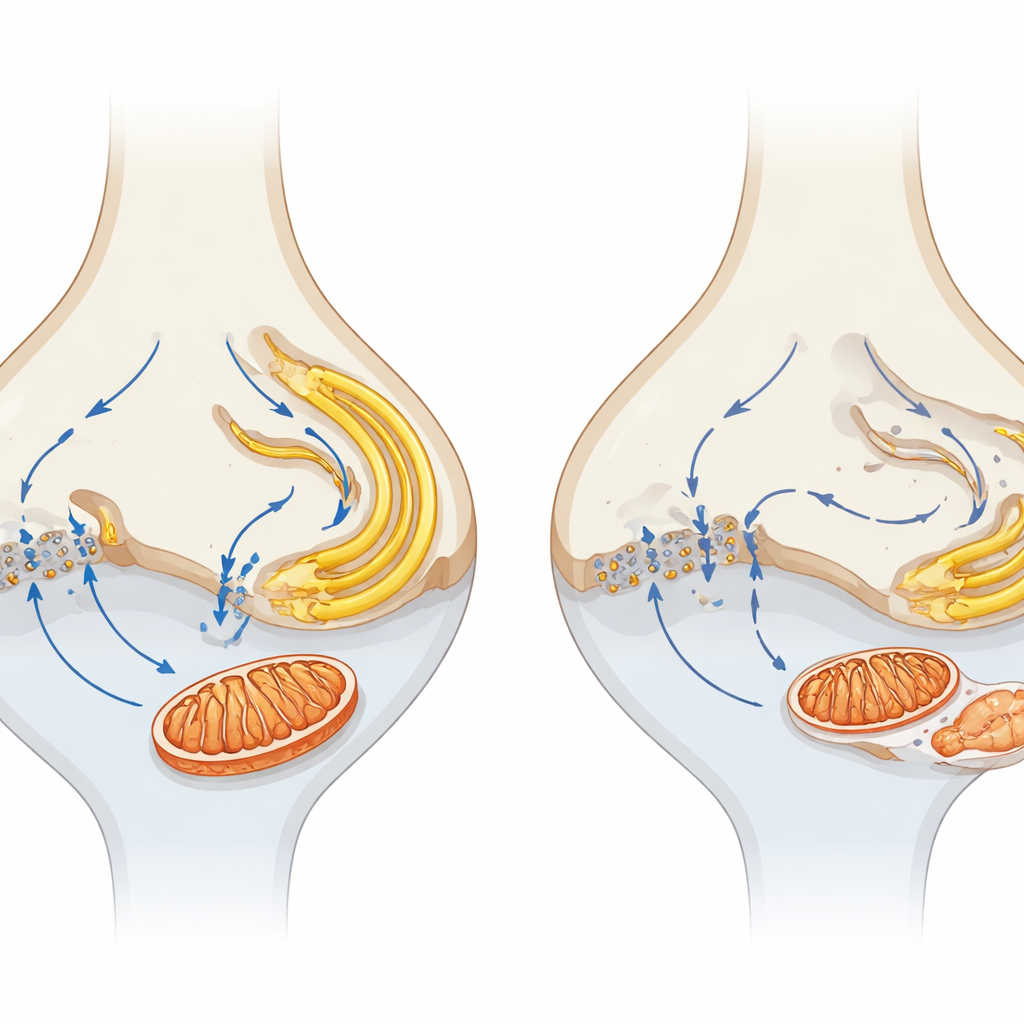
Para sondear qué ocurre antes de que las células mueran, los autores compararon la composición proteica de retinas jóvenes mutantes y normales. El cambio temprano más llamativo fue una disminución generalizada en componentes del ciclo de los ácidos tricarboxílicos (TCA), una vía central para generar energía. La microscopía confirmó que las mitocondrias, los orgánulos que albergan este ciclo, se vieron especialmente afectadas en las sinapsis de los fotorreceptores. En ratones sanos, estas terminales contienen mitocondrias prominentes; en animales deficientes en α2δ4, las mitocondrias sinápticas eran notablemente más pequeñas y menos numerosas, especialmente en las terminales de los conos, mucho antes de que se produjera una degeneración generalizada. Los marcadores mitocondriales en la capa sináptica disminuyeron y algunas mitocondrias parecieron desplazadas hacia la capa de núcleos de los fotorreceptores. En contraste, las mitocondrias en el segmento interno —el principal centro metabólico del fotorreceptor— se conservaron relativamente en las etapas tempranas, subrayando una vulnerabilidad especial de las mitocondrias sinápticas.
Conversaciones de calcio rotas entre compartimentos celulares
Dado que α2δ4 forma parte de un complejo de canales de calcio, el equipo comprobó si el manejo alterado del calcio podría subyacer a los problemas mitocondriales. En fotorreceptores sanos, el calcio que entra por los canales Cav1.4 en la sinapsis está estrechamente coordinado con el almacenamiento y la liberación de calcio por el retículo endoplásmico (RE) y la captación por las mitocondrias, creando un microcircuito que vincula la actividad eléctrica con el suministro de energía. En los ratones mutantes, proteínas que liberan calcio del RE (como el receptor de ryanodina RYR2) y un transportador mitocondrial clave de calcio (MCU) se redujeron específicamente en la capa sináptica. Los marcadores de estrés en el RE estaban elevados, lo que sugiere que este compartimento también estaba bajo tensión. En conjunto, estos cambios apuntan a una ruptura en el “intercambio” local de calcio entre la membrana celular, el RE y las mitocondrias precisamente donde se produce la señalización sináptica.
Conectar sinapsis diminutas con la pérdida de visión a largo plazo
Al comparar ratones nulo para α2δ4 con animales que carecen por completo del canal Cav1.4, los autores hallaron que una alteración más severa del canal conduce a una degeneración más rápida y pronunciada, reforzando el papel central de la entrada de calcio. Proponen un modelo en el que la pérdida de α2δ4 debilita la función de Cav1.4, perturba el flujo de calcio en la sinapsis y lo desacopla del RE y las mitocondrias cercanas. Con el tiempo, esto conduce a mitocondrias sinápticas dañadas, producción de energía deficiente y estrés en las membranas internas, que en conjunto predisponen a los fotorreceptores a una muerte lenta y progresiva. Para un lector no especializado, la idea clave es que la visión sana depende no solo de tener fotorreceptores, sino de mantener afinadas sus pequeñas centrales energéticas sinápticas y las señales de calcio; actuar sobre estos cambios locales y tempranos podría ofrecer nuevas estrategias para preservar la vista en una amplia variedad de enfermedades retinianas.
Cita: Amieghemen, C.I., Ung, T.T., Huskin, G.N. et al. Dysfunction of α2δ4 leads to photoreceptor degeneration through disrupted synaptic mitochondria and calcium crosstalk. Cell Death Dis 17, 337 (2026). https://doi.org/10.1038/s41419-026-08587-3
Palabras clave: degeneración retiniana, fotorreceptores, mitocondrias, señalización del calcio, disfunción sináptica