Clear Sky Science · it
La disfunzione di α2δ4 porta alla degenerazione dei fotorecettori attraverso la compromissione dei mitocondri sinaptici e del cross-talk del calcio
Perché questa ricerca sull'occhio è importante
La perdita della vista dovuta alla degenerazione retinica è di solito permanente, e le terapie che proteggono davvero le cellule fotosensibili dell'occhio rimangono scarse. Questo studio pone una domanda fondamentale: come possono piccoli problemi alle connessioni tra le cellule della retina accumularsi gradualmente fino a provocare la morte di quelle cellule e, in ultima analisi, la cecità? Seguendo un difetto genetico specifico riscontrato in alcune persone con disturbi visivi ereditari, gli autori rivelano un colpevole inatteso — piccole centrali energetiche alle terminazioni nervose dei fotorecettori — e tracciano come segnali di calcio perturbati alle sinapsi possano gradualmente compromettere la salute dell'intera cellula.
Dalla visione notturna alterata ai sensori di luce che muoiono
Il lavoro si concentra sui fotorecettori, bastoncelli e coni che convertono la luce in segnali elettrici. Alla loro base, queste cellule formano sinapsi specializzate che rilasciano in modo continuo segnali chimici ai neuroni successivi. Una proteina chiamata α2δ4 aiuta ad assemblare e stabilizzare un complesso di canali del calcio (Cav1.4) a queste sinapsi, e mutazioni nel suo gene sono state collegate a distrofie retiniche umane. I pazienti spesso mostrano problemi precoci nella trasmissione dei segnali dai fotorecettori alle cellule bipolari, ma possono non perdere grandi numeri di fotorecettori per molti anni. Usando topi geneticamente modificati per non esprimere α2δ4, i ricercatori hanno cercato di capire come un apparente difetto sinaptico “locale” porti alla lenta riduzione dello strato che contiene i corpi cellulari dei fotorecettori.
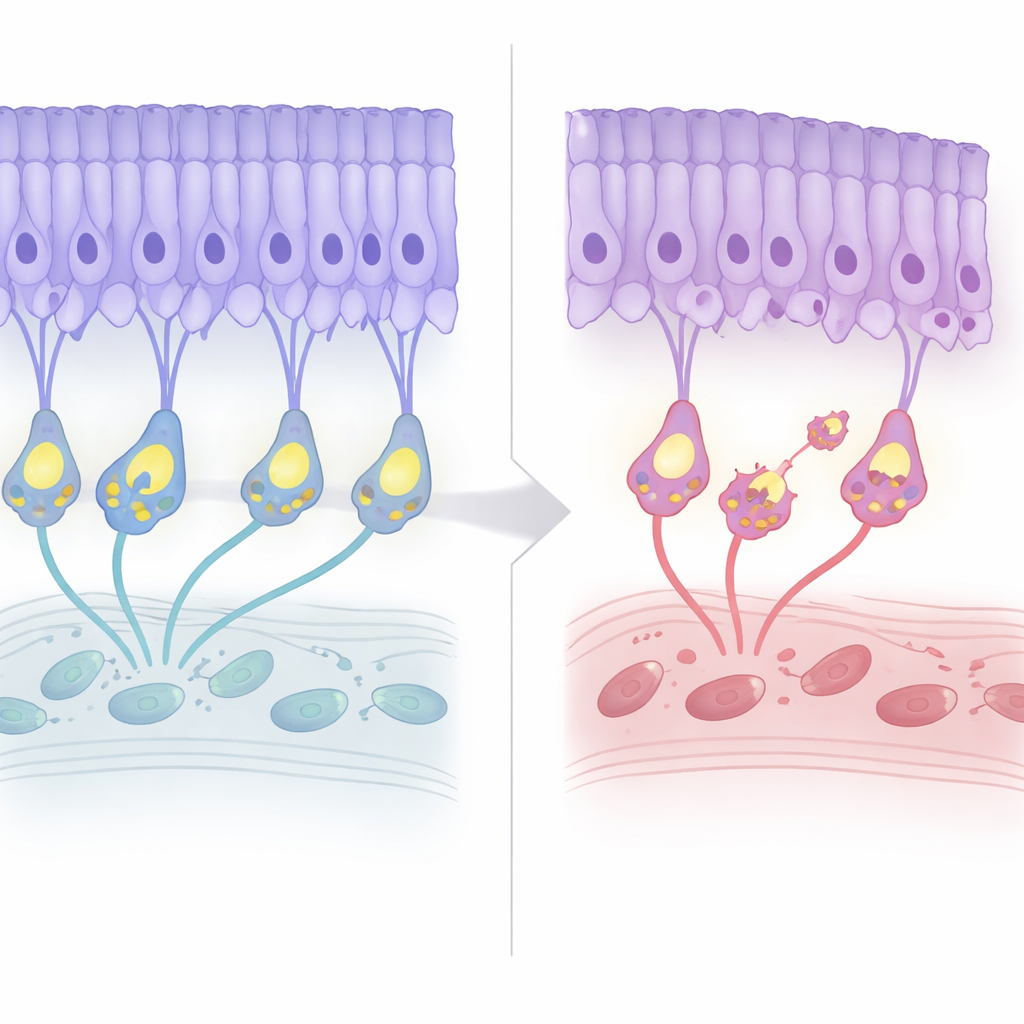
Declino strutturale lento con segnali di allarme precoci
Il gruppo ha seguito le retine di questi topi lungo il loro arco di vita. Per i primi mesi, l'architettura generale appariva normale e le registrazioni elettriche suggerivano che la rilevazione della luce restava in gran parte intatta. Intorno ai sette mesi di età, tuttavia, lo strato dei nuclei dei fotorecettori cominciò a ridursi di circa il 20 percento per poi stabilizzarsi, rispecchiando la degenerazione lieve e a insorgenza tardiva osservata nei pazienti. Interessante notare che i marcatori della morte cellulare programmata apparivano prima, prima della perdita cellulare evidente. Allo stesso tempo, il “cablaggio” si riorganizzò: le terminazioni dei fotorecettori si ritirarono dal loro strato abituale e i dendriti delle cellule bipolari crebbero verso l'alto per incontrarli, formando connessioni ectopiche. Nonostante questo rimodellamento, l'efficienza della trasmissione sinaptica — giudicata dal rapporto tra i segnali elettrici a valle e a monte — rimase costantemente scarsa ma non peggiorò con l'età.
Le centrali energetiche sinaptiche sotto stress
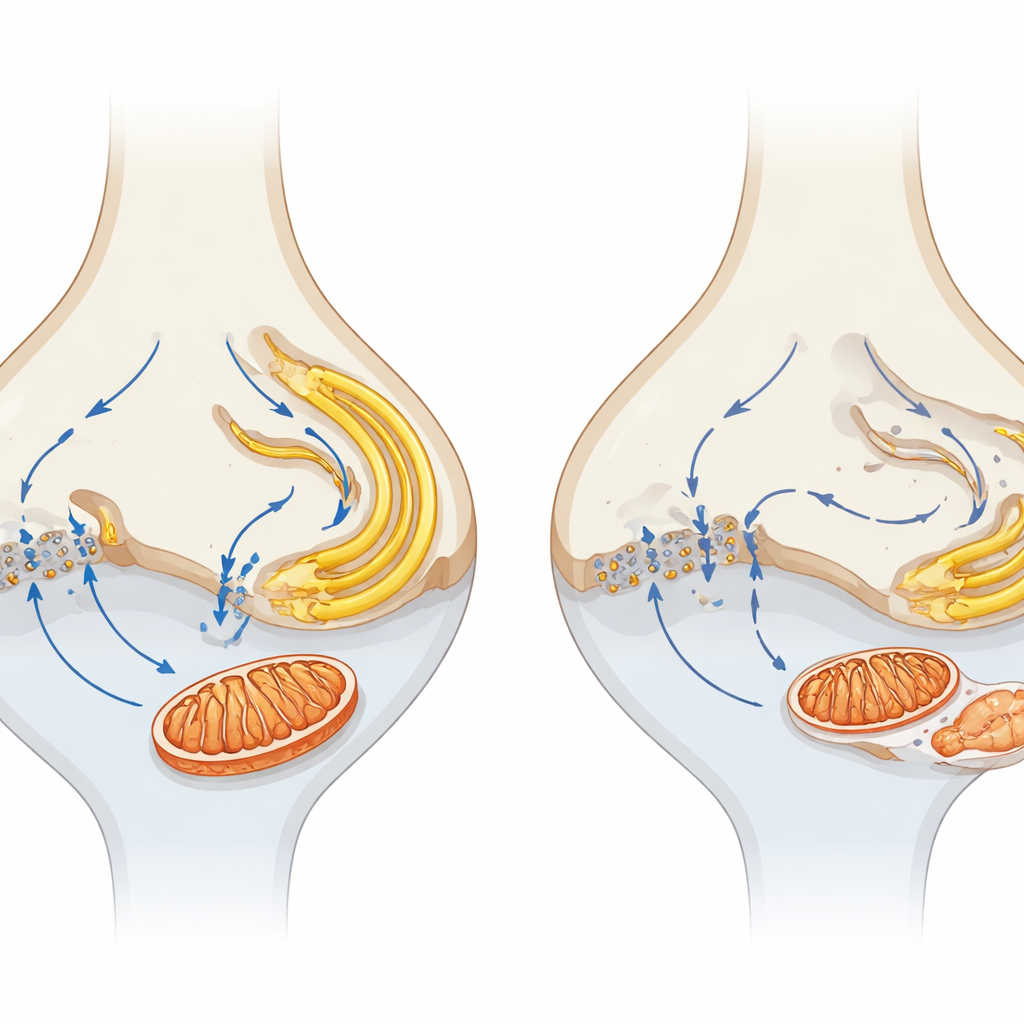
Per sondare cosa accade prima che le cellule muoiano, gli autori hanno confrontato il profilo proteico di retine giovani mutanti e normali. Il cambiamento precoce più evidente fu un calo diffuso dei componenti del ciclo degli acidi tricarbossilici (TCA), una via centrale per la produzione di energia. La microscopia confermò che i mitocondri, gli organelli che ospitano questo ciclo, erano particolarmente colpiti alle sinapsi dei fotorecettori. Nei topi sani, queste terminazioni contengono mitocondri prominenti; negli animali privi di α2δ4, i mitocondri sinaptici risultarono notevolmente più piccoli e meno numerosi, in particolare nelle terminazioni dei coni, molto prima della degenerazione diffusa. I marcatori mitocondriali nello strato sinaptico diminuirono e alcuni mitocondri apparvero spostati nello strato dei nuclei dei fotorecettori. Per contrasto, i mitocondri nel segmento interno — il principale snodo metabolico del fotorecettore — rimasero relativamente preservati nelle fasi iniziali, evidenziando una vulnerabilità particolare dei mitocondri sinaptici.
Conversazioni del calcio interrotte tra i compartimenti cellulari
Poiché α2δ4 fa parte di un complesso di canali del calcio, il gruppo ha testato se una gestione del calcio perturbata potesse essere alla base dei problemi mitocondriali. Nei fotorecettori sani, il calcio che entra attraverso i canali Cav1.4 alla sinapsi è strettamente coordinato con l'immagazzinamento e il rilascio di calcio da parte del reticolo endoplasmatico (RE) e con l'assorbimento da parte dei mitocondri, creando un microcircuito che collega l'attività elettrica alla fornitura di energia. Nei topi mutanti, le proteine che rilasciano calcio dal RE (come il recettore alla rianodina RYR2) e un importante trasportatore mitocondriale del calcio (MCU) risultarono specificamente ridotte nello strato sinaptico. I marcatori di stress nel RE erano elevati, suggerendo che anche questo compartimento era sotto sforzo. Nel loro insieme, questi cambiamenti indicano un guasto nel “cross-talk” locale del calcio tra membrana plasmatica, RE e mitocondri proprio dove avviene la segnalazione sinaptica.
Collegare sinapsi minuscole alla perdita di vista a lungo termine
Confrontando i topi knockout per α2δ4 con animali privi completamente del canale Cav1.4, gli autori hanno constatato che una perturbazione più severa del canale porta a una degenerazione più rapida e marcata, rafforzando il ruolo centrale dell'ingresso di calcio. Propongono un modello in cui la perdita di α2δ4 indebolisce la funzione di Cav1.4, disturbando il flusso di calcio alla sinapsi e disaccoppiandolo dal RE e dai mitocondri vicini. Col tempo, questo porta a mitocondri sinaptici danneggiati, produzione energetica compromessa e stress nelle membrane interne, che insieme predispongono i fotorecettori a una morte lenta e progressiva. Per il lettore non specialistico, l'intuizione chiave è che una visione sana dipende non solo dalla presenza dei fotorecettori, ma dal mantenimento delle loro minuscole centrali sinaptiche e dei segnali del calcio finemente sintonizzati; intervenire su questi cambiamenti locali e precoci potrebbe offrire nuove strategie per preservare la vista in un'ampia gamma di malattie retiniche.
Citazione: Amieghemen, C.I., Ung, T.T., Huskin, G.N. et al. Dysfunction of α2δ4 leads to photoreceptor degeneration through disrupted synaptic mitochondria and calcium crosstalk. Cell Death Dis 17, 337 (2026). https://doi.org/10.1038/s41419-026-08587-3
Parole chiave: degenerazione retinica, fotorecettori, mitocondri, segnalazione del calcio, disfunzione sinaptica