Clear Sky Science · ja
α2δ4の異常はシナプスのミトコンドリアとカルシウムの相互作用を乱し、網膜光受容体の変性を引き起こす
この眼科研究が重要な理由
網膜変性による視力喪失は通常不可逆であり、目の光を感知する細胞を真に保護する治療法は乏しいままです。本研究は基本的な問いを投げかけます:網膜内の細胞間接続における小さな不具合が、どのようにして徐々に細胞死へ、そして最終的には失明へと発展するのか?遺伝性の視覚障害を持つ一部の人に見られる特定の遺伝子欠陥を追うことで、著者らは予期せぬ犯人――光受容体の神経終末にある小さなエネルギー工場(ミトコンドリア)――を明らかにし、シナプスでの乱れたカルシウム信号がどのようにして細胞全体の健全性を徐々に損なうかをたどります。
夜間視力の障害から光センサーの死へ
本研究は光を電気信号に変換する杆体と錐体という光受容体に焦点を当てています。これらの細胞は基部に特化したシナプスを形成し、下流のニューロンへ継続的に化学信号を放出します。α2δ4というタンパク質は、これらのシナプスでカルシウムチャネル複合体(Cav1.4)の組み立てと安定化を助け、その遺伝子の変異はヒトの網膜ジストロフィーと関連づけられています。患者はしばしば光受容体から双極細胞への信号伝達に早期の問題を示しますが、多くの光受容体が失われるのは何年も後という場合があります。α2δ4を欠損させたマウスを用いて、研究者らは一見“局所的”なシナプス欠陥がいかにして光受容体細胞体の層のゆっくりとした消耗につながるのかを明らかにしようとしました。
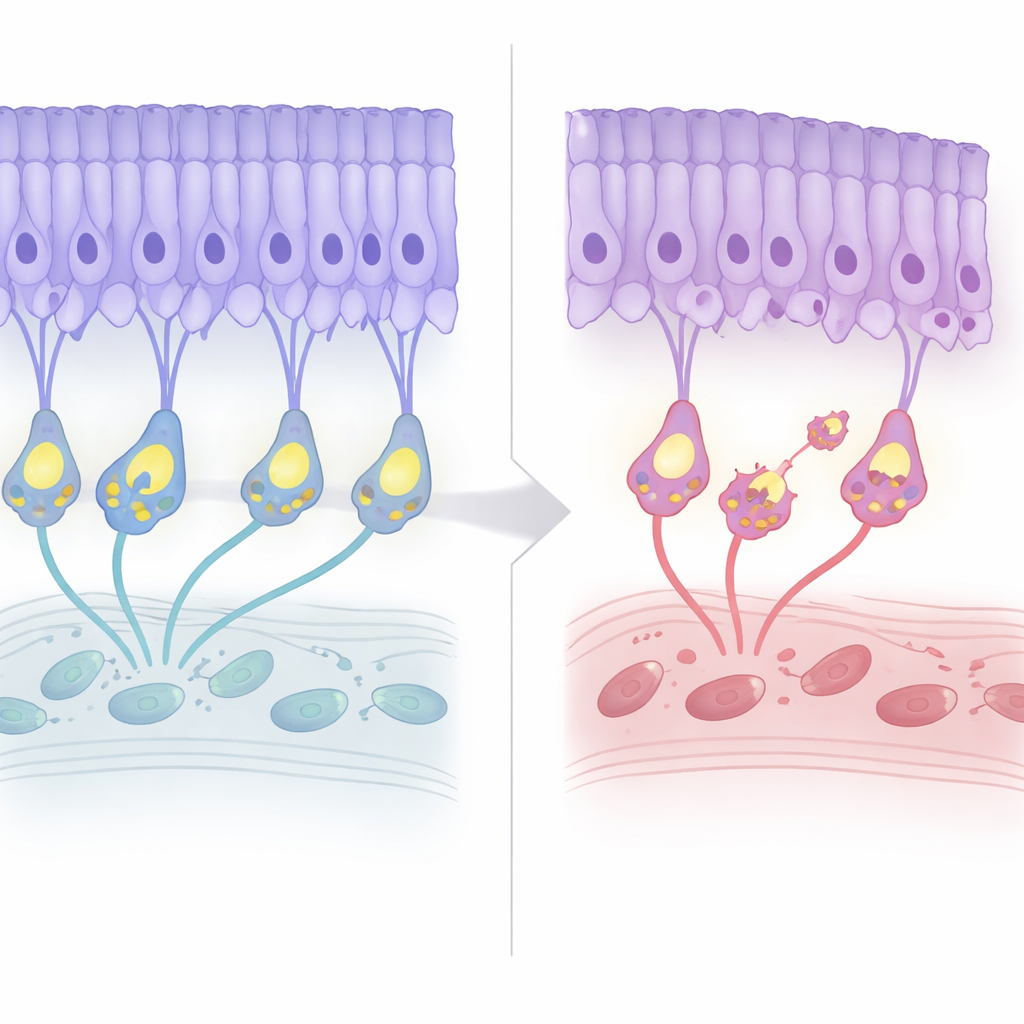
初期の警告サインを伴うゆっくりとした構造的衰退
チームはこれらのマウスの網膜を寿命にわたって追跡しました。最初の数か月間は全体の構造は正常に見え、電気的記録も光の検出自体は大部分保たれていることを示していました。しかし生後約7か月頃から、光受容体核の層が約20パーセント薄くなり、その後横ばいになりました。これは患者で見られる軽度で遅発性の変性を反映しています。興味深いことに、プログラムされた細胞死のマーカーは明らかな細胞喪失の前に早期に現れていました。同時に“配線”の再編が起き、光受容体のターミナルが通常の層から後退し、双極細胞の樹状突起が上方へ伸びてこれらと出会い、異所性の接続を形成しました。このリモデリングにもかかわらず、下流対上流の電気信号の比率で評価されるシナプス伝達の効率は一貫して低いままで、年齢とともにさらに悪化することはありませんでした。
シナプスのエネルギー工場がストレスを受ける
細胞死の前に何が起きるかを調べるため、著者らは若齢の変異体と正常網膜のタンパク質構成を比較しました。最も顕著な初期変化は、エネルギー生成の中心経路である三酸酸回路(TCA回路)の構成要素の広範な低下でした。顕微鏡観察は、TCA回路を担うミトコンドリアが特に光受容体のシナプスで影響を受けていることを裏付けました。健康なマウスでは、これらのターミナルには目立つミトコンドリアが存在しますが、α2δ4欠損動物ではシナプスのミトコンドリアは著しく小さく、数も減少しており、広範な変性が起きるずっと前に特に錐体終端で顕著でした。シナプス層のミトコンドリアマーカーは減少し、一部のミトコンドリアは光受容体核の層へ移動しているように見えました。対照的に、光受容体の主要な代謝ハブである内節のミトコンドリアは初期には比較的保持されており、シナプスミトコンドリアが特別に脆弱であることを示しています。
細胞区画間のカルシウムのやり取りが破綻
α2δ4がカルシウムチャネル複合体の一部であることから、研究チームはカルシウム処理の乱れがミトコンドリア問題の根底にあるかを検証しました。正常な光受容体では、シナプスのCav1.4チャネルを通って入るカルシウムは、小胞体(ER)による貯蔵と放出、そしてミトコンドリアによる取り込みと密接に連携し、電気活動をエネルギー供給に結びつけるマイクロ回路を形成します。変異マウスでは、ERからカルシウムを放出するタンパク質(例:リアノジン受容体RYR2)や主要なミトコンドリアカルシウム輸送体(MCU)がシナプス層で特異的に減少していました。ERのストレスマーカーも上昇しており、この区画も負荷を受けていることが示唆されます。これらの変化は、細胞膜、ER、ミトコンドリアの間でシナプス部位における局所的なカルシウム“クロストーク”が破綻していることを示しています。
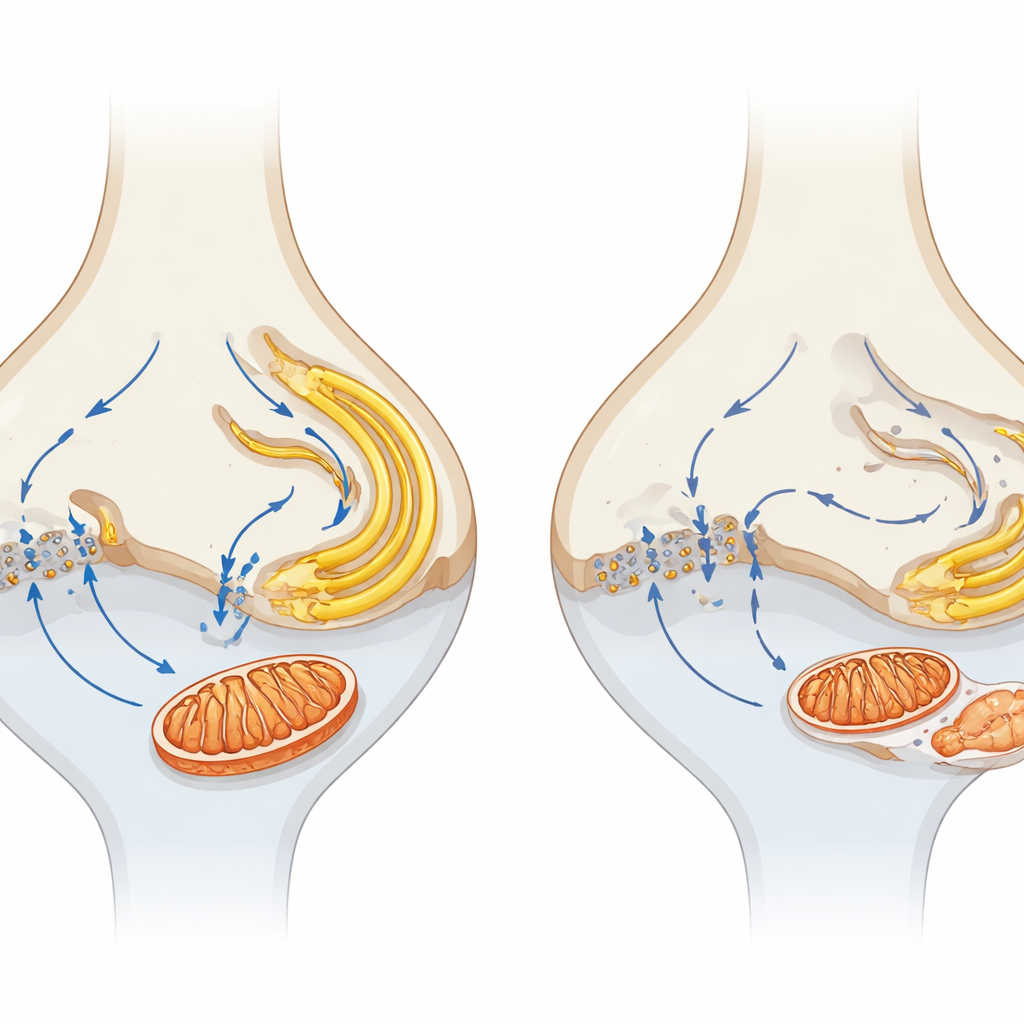
小さなシナプスから長期的な視力低下へのつながり
α2δ4ノックアウトマウスとCav1.4チャネルを完全に欠く動物を比較すると、より深刻なチャネル障害はより速く強い変性をもたらし、カルシウム流入の中心的役割が補強されました。著者らは、α2δ4の喪失がCav1.4機能を弱め、シナプスでのカルシウム流を乱して近傍のERやミトコンドリアとの結びつきを切断するとするモデルを提案します。時間とともにこれがシナプスミトコンドリアの損傷、エネルギー産生の障害、内部膜のストレスを引き起こし、これらが合わさって光受容体をゆっくりと進行する死へと傾けます。一般読者にとっての主要な洞察は、健全な視力は単に光受容体が存在することだけでなく、これらの小さなシナプスのエネルギー供給装置とカルシウム信号が精密に調整されていることに依存しているという点です。これらの早期かつ局所的な変化を標的にすることが、幅広い網膜疾患で視力を保存するための新たな戦略を提供する可能性があります。
引用: Amieghemen, C.I., Ung, T.T., Huskin, G.N. et al. Dysfunction of α2δ4 leads to photoreceptor degeneration through disrupted synaptic mitochondria and calcium crosstalk. Cell Death Dis 17, 337 (2026). https://doi.org/10.1038/s41419-026-08587-3
キーワード: 網膜変性, 光受容体, ミトコンドリア, カルシウムシグナリング, シナプス機能障害