Clear Sky Science · ar
خلل في α2δ4 يؤدي إلى تنكس الخلايا الضوئية عبر تعطيل متداخلة الكالسيوم والميتوكوندريا المشبكية
لماذا تهم هذه الأبحاث العينية
فقدان البصر الناتج عن تنكس الشبكية عادةً يكون دائمًا، والعلاجات التي تحمي فعليًا خلايا الاستشعار الضوئية في العين ما زالت نادرة. تطرح هذه الدراسة سؤالًا أساسيًا: كيف يمكن لمشكلات صغيرة عند الاتصالات بين الخلايا في الشبكية أن تتفاقم تدريجيًا إلى موت تلك الخلايا وفي النهاية العمى؟ من خلال تتبُّع خلل جيني محدد موجود لدى بعض الأشخاص المصابين باضطرابات بصرية وراثية، يكشف المؤلفون عن سبب غير متوقع — مصانع طاقة صغيرة عند نهايات الأعصاب في الخلايا الضوئية — ويتعقبون كيف أن إشارات الكالسيوم المضطربة في المشابك يمكن أن تقوّض صحة الخلية بأكملها بمرور الوقت.
من ضعف الرؤية الليلية إلى موت مستقبلات الضوء
تتركز الدراسة على الخلايا الضوئية، القضبان والمخاريط التي تحول الضوء إلى إشارات كهربائية. عند قاعدتها، تشكل هذه الخلايا مشابكًا متخصصة تطلق باستمرار إشارات كيميائية إلى الخلايا العصبية التالية. يساعد بروتين يُسمى α2δ4 في تجميع وتثبيت مركب قناة الكالسيوم (Cav1.4) عند هذه المشابك، وقد ارتبطت طفرات في جينه باضطرابات شبكية وراثية لدى البشر. يُظهر المرضى غالبًا مشاكل مبكرة في نقل الإشارات من الخلايا الضوئية إلى خلايا البايبولار، لكن قد لا يفقدون أعدادًا كبيرة من الخلايا الضوئية لسنوات. باستخدام فئران مهندسة جينيًا تفتقر إلى α2δ4، سعى الباحثون لفهم كيف يمكن لعيب «محلي» ظاهر في المشبك أن يؤدي في النهاية إلى ترقق بطئ في الطبقة التي تحتوي على أجسام خلايا الضوئية.
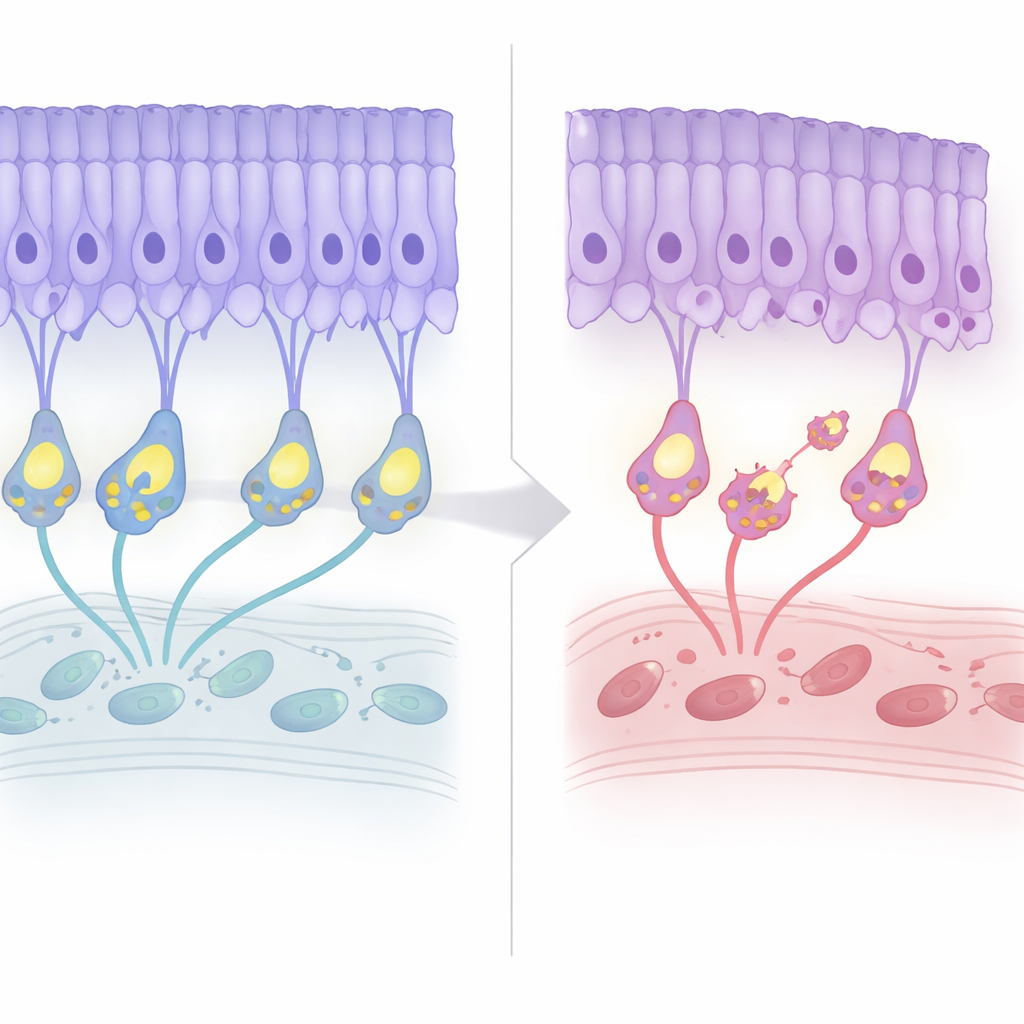
تدهور بنيوي بطيء مع علامات إنذار مبكرة
تابع الفريق شبكيات هذه الفئران على مدار حياتها. خلال الأشهر القليلة الأولى، بدا البناء العام طبيعيًا، وأشارت القياسات الكهربائية إلى أن كشف الضوء نفسه ظل سليمًا إلى حد كبير. لكن حوالي عمر سبعة أشهر، بدأت طبقة نوى الخلايا الضوئية في الترقق بحوالي 20 في المئة ثم استقرت، مما يعكس التنكس الخفيف ذي المظهر المتأخر الذي يُرى لدى المرضى. ومن المثير للاهتمام أن علامات موت الخلايا المبرمج ظهرت مبكرًا، قبل فقدان الخلايا بشكل واضح. وفي الوقت نفسه، أعيد تنظيم «الأسلاك»: تراجعت نهايات الخلايا الضوئية من طبقتها المعتادة، ونمت تفرعات خلايا البايبولار صعودًا للالتقاء بها، مُشكِّلة وصلات غير طبيعية. بالرغم من هذا إعادة التشكيل، بقيت فعالية النقل المشبكي — كما يُقاس بنسبة الإشارات الكهربائية الهابطة إلى الصاعدة — ضعيفة بثبات لكنها لم تتفاقم مع التقدم في العمر.
مصانع الطاقة المشبكية تحت الضغط
لفحص ما يحدث قبل موت الخلايا، قارن المؤلفون تركيبة البروتين في شبكيات صغيرة السن الطافرة والطبيعية. كان التغير المبكر الأكثر لفتًا هو انخفاض واسع في مكونات دورة حمض الثلاثي الكربوكسيل (TCA)، وهي مسار مركزي لتوليد الطاقة. أكدت الميكروسكوبات أن الميتوكوندريا، العضيات التي تحتضن هذه الدورة، كانت متأثرة بشكل خاص عند المشابك في الخلايا الضوئية. في الفئران السليمة، تحوي هذه النهايات ميتوكوندريا بارزة؛ أما في الحيوانات المنقوصة من α2δ4، فكانت الميتوكوندريا المشبكية أصغر بكثير وأقل عددًا، خصوصًا في نهايات المخاريط، وذلك قبل حدوث تنكس واسع النطاق بكثير. انخفضت علامات الميتوكوندريا في الطبقة المشبكية، وظهرت بعض الميتوكوندريا مزيحة إلى طبقة نوى الخلايا الضوئية. بالمقابل، كانت ميتوكوندريا المقطع الداخلي — المركز الأيضي الرئيسي للخلايا الضوئية — محفوظة نسبيًا في المراحل المبكرة، مما يبرز هشاشة خاصة لميتوكوندريا المشابك.
انقطاع محادثات الكالسيوم بين مقاطع الخلية
نظرًا لأن α2δ4 جزء من مركب قناة الكالسيوم، اختبر الفريق ما إذا كان اضطراب تعامل الكالسيوم قد يكون سببًا للمشاكل الميتوكوندرية. في الخلايا الضوئية السليمة، يرتبط الكالسيوم الداخل عبر قنوات Cav1.4 عند المشبك ارتباطًا وثيقًا مع تخزين وإطلاق الكالسيوم من الشبكة الإندوبلازمية وامتصاصه بواسطة الميتوكوندريا، ما يخلق دائرة صغيرة تربط النشاط الكهربائي بإمداد الطاقة. في الفئران الطافرة، كانت البروتينات التي تطلق الكالسيوم من الشبكة الإندوبلازمية (مثل مستقبل الريانودين RYR2) وناقلة الكالسيوم الميتوكوندرية الأساسية (MCU) منخفضة بشكل خاص في الطبقة المشبكية. كما ارتفعت علامات الإجهاد في الشبكة الإندوبلازمية، مما يشير إلى أن هذا المنقسَم الداخلي كان أيضًا تحت ضغط. مجتمعة، تشير هذه التحولات إلى انهيار في «التبادل» الموضعي للكالسيوم بين غشاء الخلية والشبكة الإندوبلازمية والميتوكوندريا تمامًا عند موقع الإشارة المشبكية.
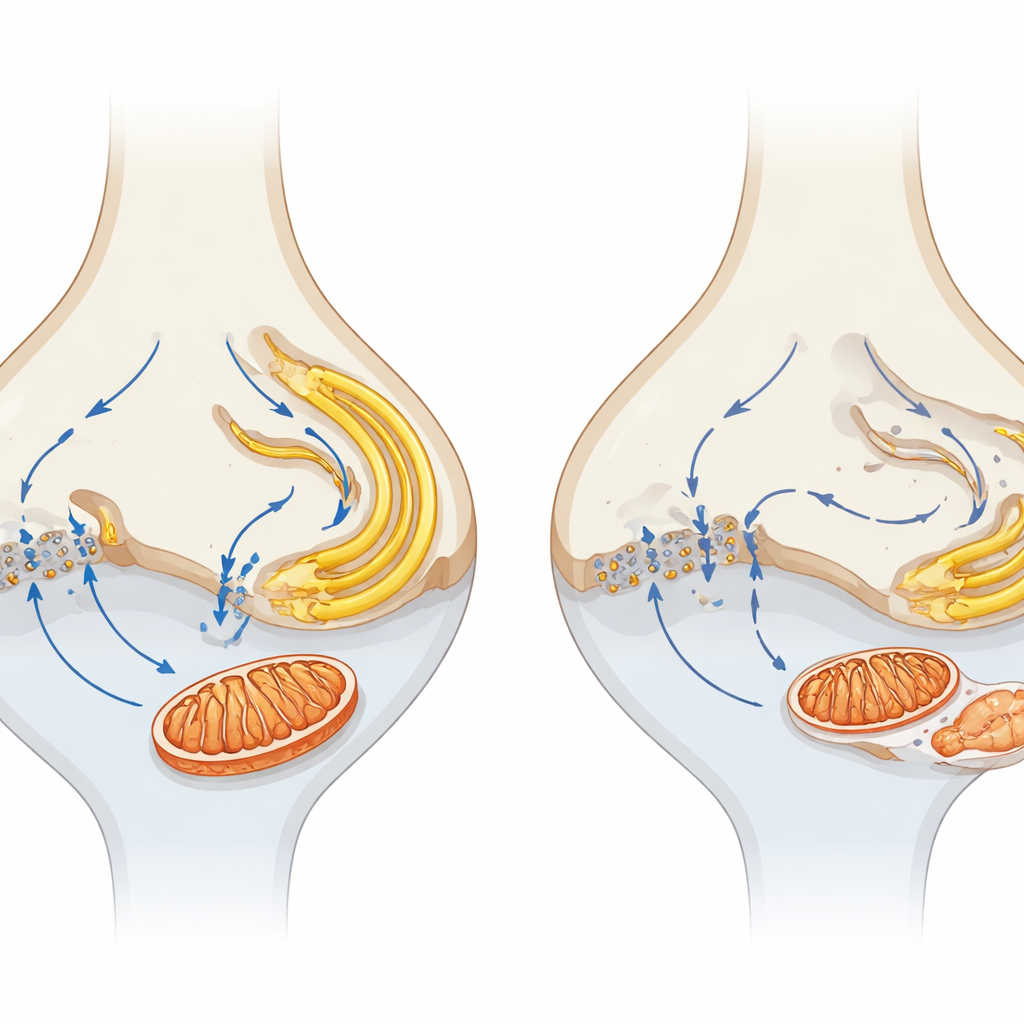
ربط المشابك الصغيرة بفقدان البصر طويل الأمد
بالمقارنة بين فئران معطلة α2δ4 وحيوانات تفتقر تمامًا إلى قناة Cav1.4، وجد المؤلفون أن تعطيل القناة بشكل أشد يؤدي إلى تنكس أسرع وأقوى، مما يعزز الدور المركزي لدخول الكالسيوم. يقترحون نموذجًا يفيد أن فقدان α2δ4 يضعف وظيفة Cav1.4، معطلاً تدفق الكالسيوم عند المشبك وفصله عن الشبكة الإندوبلازمية والميتوكوندريا المجاورة. مع مرور الوقت، يؤدي ذلك إلى تلف الميتوكوندريا المشبكية، وضعف إنتاج الطاقة، وإجهاد الأغشية الداخلية، مما يمهد للخلايا الضوئية لموت بطيء وتقدمي. للخلاصة العامة للقارئ العادي: الرؤية السليمة تعتمد ليس فقط على وجود خلايا ضوئية، بل على الحفاظ على مصانع الطاقة المشبكية الصغيرة وإشارات الكالسيوم مضبوطة بدقة؛ استهداف هذه التغيرات المحلية المبكرة قد يوفر استراتيجيات جديدة للحفاظ على البصر في مجموعة واسعة من أمراض الشبكية.
الاستشهاد: Amieghemen, C.I., Ung, T.T., Huskin, G.N. et al. Dysfunction of α2δ4 leads to photoreceptor degeneration through disrupted synaptic mitochondria and calcium crosstalk. Cell Death Dis 17, 337 (2026). https://doi.org/10.1038/s41419-026-08587-3
الكلمات المفتاحية: تنكس شبكية العين, الخلايا الضوئية, الميتوكوندريا, إشارات الكالسيوم, خلل المشبك