Clear Sky Science · sv
Funktionstörning i α2δ4 leder till fotoreceptordegeneration genom störda synaptiska mitokondrier och kalciumkorsprat
Varför denna ögonforskning är viktig
Synförlust vid retinal degeneration är oftast bestående, och behandlingar som verkligen skyddar ögats ljuskänsliga celler är fortfarande få. Denna studie ställer en grundläggande fråga: hur kan små problem vid kopplingarna mellan celler i näthinnan långsamt växa till att döda dessa celler och i slutänden orsaka blindhet? Genom att följa en specifik genetisk defekt som finns hos vissa med ärftliga synstörningar identifierar författarna en oväntad bov — små energifabriker vid fotoreceptorernas nervändar — och spårar hur rubbade kalciumsignaler i synapser kan gradvis undergräva hela cellens hälsa.
Från felaktig nattseende till döende ljussensorer
Arbetet fokuserar på fotoreceptorerna, stavarna och konerna som omvandlar ljus till elektriska signaler. Vid deras bas bildar dessa celler specialiserade synapser som kontinuerligt frigör kemiska signaler till efterföljande neuroner. Ett protein kallat α2δ4 hjälper till att montera och stabilisera en kalciumkanalskomplex (Cav1.4) vid dessa synapser, och mutationer i dess gen har kopplats till mänskliga retinala dystrofier. Patienter visar ofta tidiga problem med att överföra signaler från fotoreceptorer till bipolära celler men kan sakna omfattande förlust av fotoreceptorer under många år. Genom att använda möss konstruerade att sakna α2δ4 försökte forskarna förstå hur ett till synes ”lokalt” synaptiskt fel så småningom leder till den långsamma uttunningen av lagret som innehåller fotoreceptorernas cellkärnor.
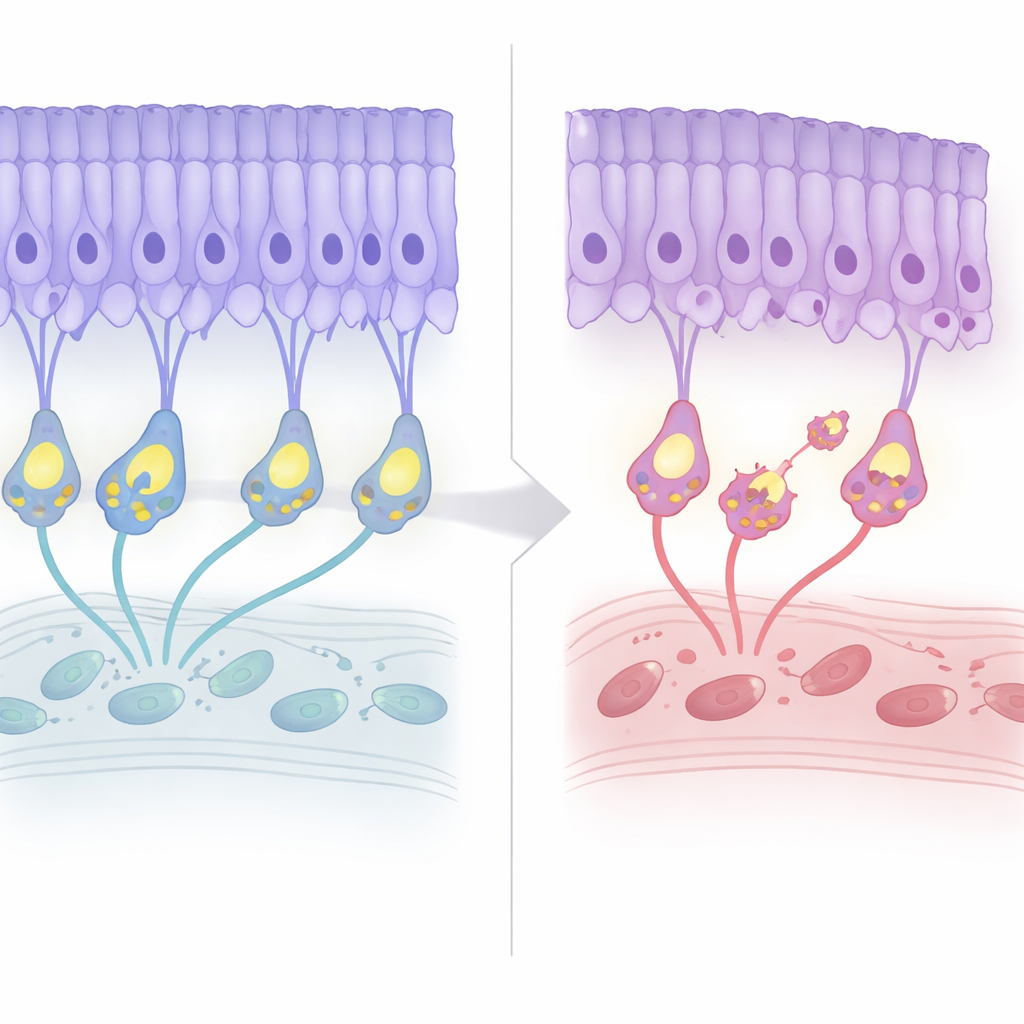
Långsam strukturell försämring med tidiga varningssignaler
Teamet följde dessa möss näthinnor över deras livstid. Under de första månaderna såg den övergripande arkitekturen normal ut, och elektriska inspelningar antydde att ljusdetektionen i stort sett förblev intakt. Runt sju månaders ålder började emellertid lagret med fotoreceptorkärnor tunnas ut med ungefär 20 procent och nådde sedan en platå, vilket speglar den milda, sena degenerationen som ses hos patienter. Intressant nog dök markörer för programmerad celldöd upp tidigare, innan uppenbar cellförlust. Samtidigt omorganiserades ”kopplingarna”: fotoreceptorernas terminaler drog sig tillbaka från sitt vanliga lager, och de bipolära cellernas dendriter sköt uppåt för att möta dem och bildade onormala kopplingar. Trots denna ombyggnad förblev effektiviteten i synaptisk överföring — bedömd som förhållandet mellan efterföljande och föregående elektriska signaler — stadigt dålig men försämrades inte med åldern.
Energi fabrikerna vid synapsen under stress
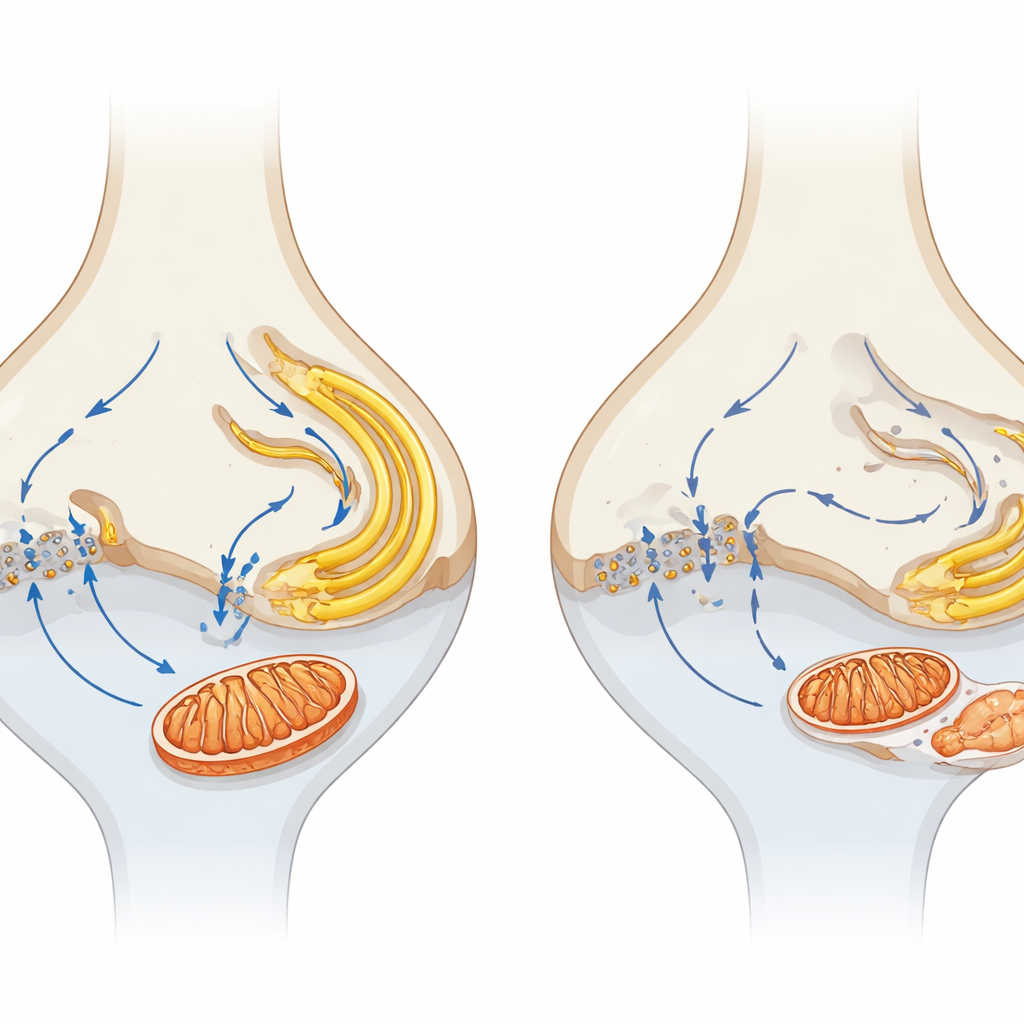
För att undersöka vad som händer innan cellerna dör jämförde författarna proteininnehållet i unga mutanta och normala näthinnor. Den mest slående tidiga förändringen var en bred nedgång i komponenter av trikarboxylsyracykeln (TCA), en central väg för energiproduktion. Mikroskopi bekräftade att mitokondrierna, organellerna som huserar denna cykel, var särskilt påverkade vid fotoreceptorernas synapser. I friska möss rymmer dessa terminaler framträdande mitokondrier; i α2δ4-defekta djur var de synaptiska mitokondrierna avsevärt mindre och färre till antalet, särskilt i konterminaler, långt innan utbredd degeneration. Mitokondriella markörer i det synaptiska lagret sjönk och vissa mitokondrier verkade förflyttade in i lagret med fotoreceptorkärnor. Däremot var mitokondrierna i det inre segmentet — fotoreceptorernas huvudsakliga metabola nav — relativt bevarade tidigt, vilket belyser en särskild sårbarhet hos synaptiska mitokondrier.
Brutna kalciumkonversationer mellan cellkompartment
Eftersom α2δ4 är del av ett kalciumkanalskomplex testade teamet om störd kalciumhantering kunde ligga bakom mitokondrieproblemen. I friska fotoreceptorer koordineras kalcium som kommer in genom Cav1.4-kanaler vid synapsen nära med kalciumlagring och -frigörelse från endoplasmatiska retiklet (ER) och upptag av mitokondrier, vilket skapar ett mikrokretslopp som länkar elektrisk aktivitet till energiförsörjning. Hos de mutanta mössen var proteiner som frigör kalcium från ER (såsom ryanodinreceptorn RYR2) och en viktig mitokondriell kalciumtransportör (MCU) specifikt reducerade i det synaptiska lagret. Markörer för stress i ER var förhöjda, vilket tyder på att även detta kompartment var belastat. Tillsammans pekar dessa förändringar på ett sammanbrott i det lokala kalcium ”korspratet” mellan cellmembranet, ER och mitokondrier just där synaptisk signalering sker.
Koppla ihop små synapser med långsiktig synförlust
Genom att jämföra α2δ4-knockout-möss med djur som helt saknar Cav1.4-kanalen fann författarna att kraftigare kanalstörning leder till snabbare och starkare degeneration, vilket stärker kalciuminfluxens centrala roll. De föreslår en modell där förlust av α2δ4 försvagar Cav1.4-funktionen, stör kalciumflödet vid synapsen och lossar kopplingen till närliggande ER och mitokondrier. Med tiden leder detta till skadade synaptiska mitokondrier, nedsatt energiproduktion och stress i interna membran, vilket tillsammans förbereder fotoreceptorerna för en långsam, progressiv död. För en lekmannaläsare är huvudinsikten att god syn inte bara kräver fotoreceptorer utan också att deras små synaptiska kraftverk och kalciumsignaler hålls välavvägda; att rikta in sig på dessa tidiga, lokala förändringar kan ge nya strategier för att bevara synen vid ett brett spektrum av retinala sjukdomar.
Citering: Amieghemen, C.I., Ung, T.T., Huskin, G.N. et al. Dysfunction of α2δ4 leads to photoreceptor degeneration through disrupted synaptic mitochondria and calcium crosstalk. Cell Death Dis 17, 337 (2026). https://doi.org/10.1038/s41419-026-08587-3
Nyckelord: retinal degeneration, fotoreceptorer, mitokondrier, kalciumsignalering, synaptisk dysfunktion