Clear Sky Science · tr
α2δ4 disfonksiyonu, bozulmuş sinaptik mitokondri ve kalsiyum etkileşimi yoluyla fotoreseptör dejenerasyonuna yol açar
Bu göz araştırması neden önemli
Retinal dejenerasyondan kaynaklanan görme kaybı genellikle kalıcıdır ve gözün ışığı algılayan hücrelerini gerçekten koruyan tedaviler hâlâ nadirdir. Bu çalışma temel bir soruyu gündeme getiriyor: retinadaki hücreler arasındaki bağlantılardaki küçük kusurlar nasıl yavaşça büyüyüp bu hücrelerin ölümü ve nihayetinde körlüğe yol açabilir? Mirasla geçen görme bozukluğu bulunan bazı insanlarda tespit edilen belirli bir genetik kusuru takip ederek, yazarlar beklenmedik bir suçluyu ortaya koyuyor—fotoreseptörlerin sinir uçlarındaki küçük enerji fabrikaları—ve sinapstaki bozulmuş kalsiyum sinyallerinin tüm hücrenin sağlığını zamanla nasıl zayıflatabildiğini izliyor.
Hatalı gece görüşünden ölen ışık algılayıcılarına
Çalışma, ışığı elektrik sinyallerine dönüştüren çubuk ve konileri yani fotoreseptörlere odaklanıyor. Bu hücrelerin tabanında, aşağı yönlü nöronlara sürekli kimyasal sinyaller salan özelleşmiş sinapslar bulunur. α2δ4 adlı bir protein, bu sinapslarda bir kalsiyum kanalı kompleksi (Cav1.4) kurmaya ve stabil hale getirmeye yardımcı olur ve genindeki mutasyonlar insan retinal distrofileriyle ilişkilendirilmiştir. Hastalar genellikle fotoreseptörlerden bipolar hücrelere iletimde erken sorunlar gösterir, ancak yıllarca çok sayıda fotoreseptör kaybetmeyebilirler. α2δ4 eksikliği olan genetik olarak tasarlanmış fareleri kullanarak, araştırmacılar görünüşte “yerel” bir sinaptik kusurun sonunda nasıl fotoreseptör hücre gövdelerinin bulunduğu katmanın yavaş incelmesine yol açtığını anlamayı amaçladılar.
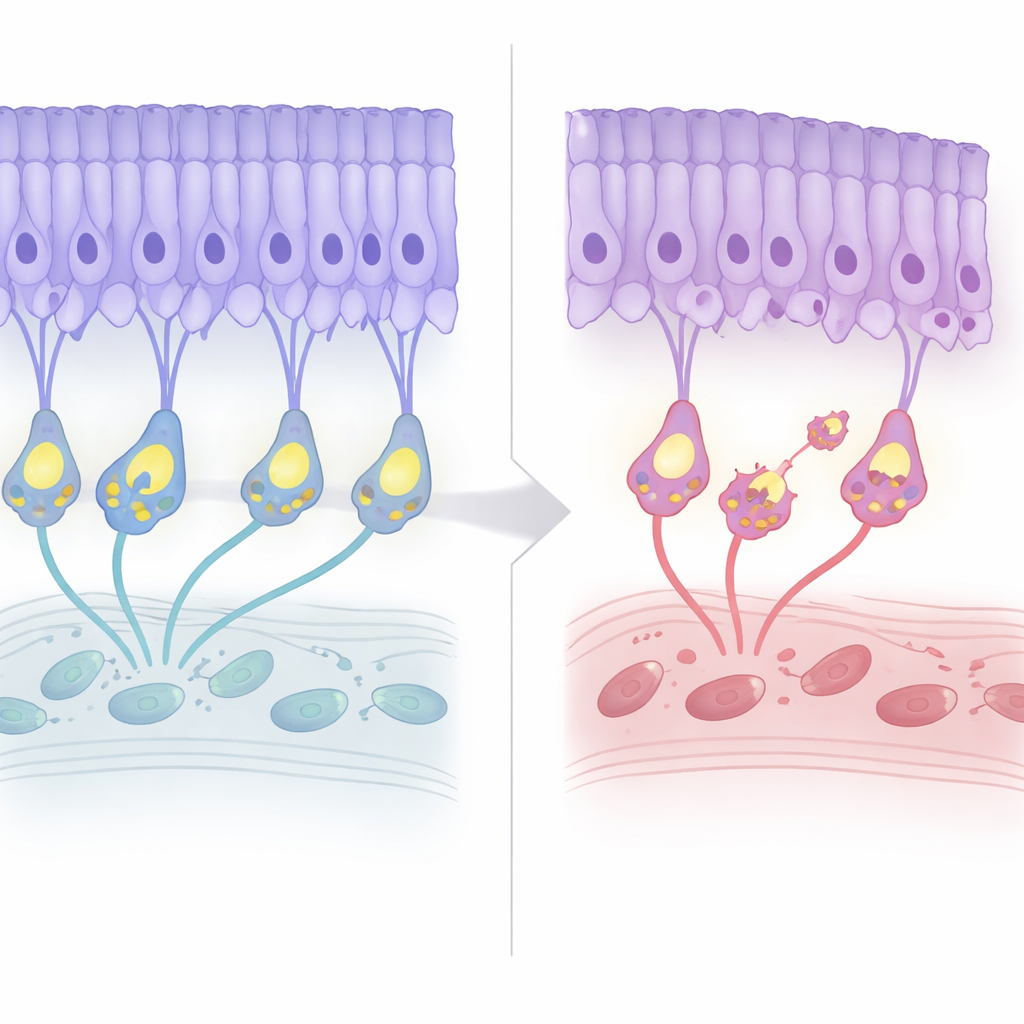
Erken uyarı işaretleriyle yavaş yapısal çöküş
Ekip, bu farelerin retinalarını yaşamları boyunca izledi. İlk birkaç ay boyunca genel mimari normal görünüyordu ve elektrik kayıtları ışık algısının büyük ölçüde korunduğunu düşündürdü. Ancak yedi aylık civarında, fotoreseptör çekirdeklerinin bulunduğu katman yaklaşık yüzde 20 incelmeye başladı ve ardından plato yaptı; bu, hastalarda görülen hafif, geç başlangıçlı dejenerasyonu yansıtıyordu. İlginç bir şekilde programlanmış hücre ölümü göstergeleri bariz hücre kaybından önce daha erken ortaya çıktı. Aynı zamanda “kablolama” yeniden düzenlendi: fotoreseptör terminalleri olağan katmanlarından geri çekildi ve bipolar hücrelerin dendritleri yukarı doğru uzanıp onlarla anormal bağlantılar kurdu. Bu yeniden düzenlemeye rağmen, sinaptik iletimin verimliliği—aşağı akımdan yukarı akıma elektrik sinyallerinin oranına göre değerlendirilince—istikrarlı biçimde düşüktü, ancak yaşla kötüleşmedi.
Sinapstaki enerji fabrikaları baskı altında
Hücreler ölmeden önce ne olduğunu araştırmak için yazarlar genç mutant ve normal retinaların protein bileşimlerini karşılaştırdı. En çarpıcı erken değişiklik, enerji üretiminin merkezi yollarından biri olan trikarboksilik asit (TCA) döngüsünün bileşenlerinde yaygın bir düşüştü. Mikroskopi, bu döngünün gerçekleştiği organeller olan mitokondrilerin özellikle fotoreseptör sinapslarında etkilendiğini doğruladı. Sağlıklı farelerde bu terminaller belirgin mitokondriler barındırırken; α2δ4 eksikliğine sahip hayvanlarda sinaptik mitokondriler belirgin şekilde daha küçük ve sayıca daha azdı, özellikle koni terminallerinde ve yaygın dejenerasyondan çok önce. Sinaptik katmandaki mitokondri belirteçleri azaldı ve bazı mitokondriler fotoreseptör çekirdekleri katmanına kaymış görünüyordu. Buna karşılık, fotoreseptörün ana metabolik merkezi olan iç segmentteki mitokondriler erken dönemde nispeten korunmuştu; bu da sinaptik mitokondrilerin özel bir savunmasızlığını vurguluyor.
Hücre bölümleri arasında kırılmış kalsiyum konuşmaları
α2δ4 bir kalsiyum kanalı kompleksinin parçası olduğundan, ekip mitokondri sorunlarının altında bozulmuş kalsiyum yönetiminin olup olmadığını test etti. Sağlıklı fotoreseptörlerde sinapstan Cav1.4 kanalları aracılığıyla giren kalsiyum, endoplazmik retikulum (ER) tarafından depolama ve salım ile mitokondri tarafından alım ile yakından koordine edilir; bu, elektriksel aktiviteyi enerji arzına bağlayan bir mikrodevre oluşturur. Mutant farelerde ER'den kalsiyum salan proteinler (örneğin ryanodin reseptörü RYR2) ve önemli bir mitokondri kalsiyum taşıyıcısı (MCU) özellikle sinaptik katmanda azalmıştı. ER'deki stres göstergeleri artmıştı; bu da bu bölmenin de gerilim altında olduğunu düşündürüyordu. Birlikte, bu değişimler sinaptik iletişimin gerçekleştiği yerde hücre zarı, ER ve mitokondriler arasındaki yerel kalsiyum "etkileşiminin" bozulduğuna işaret ediyor.
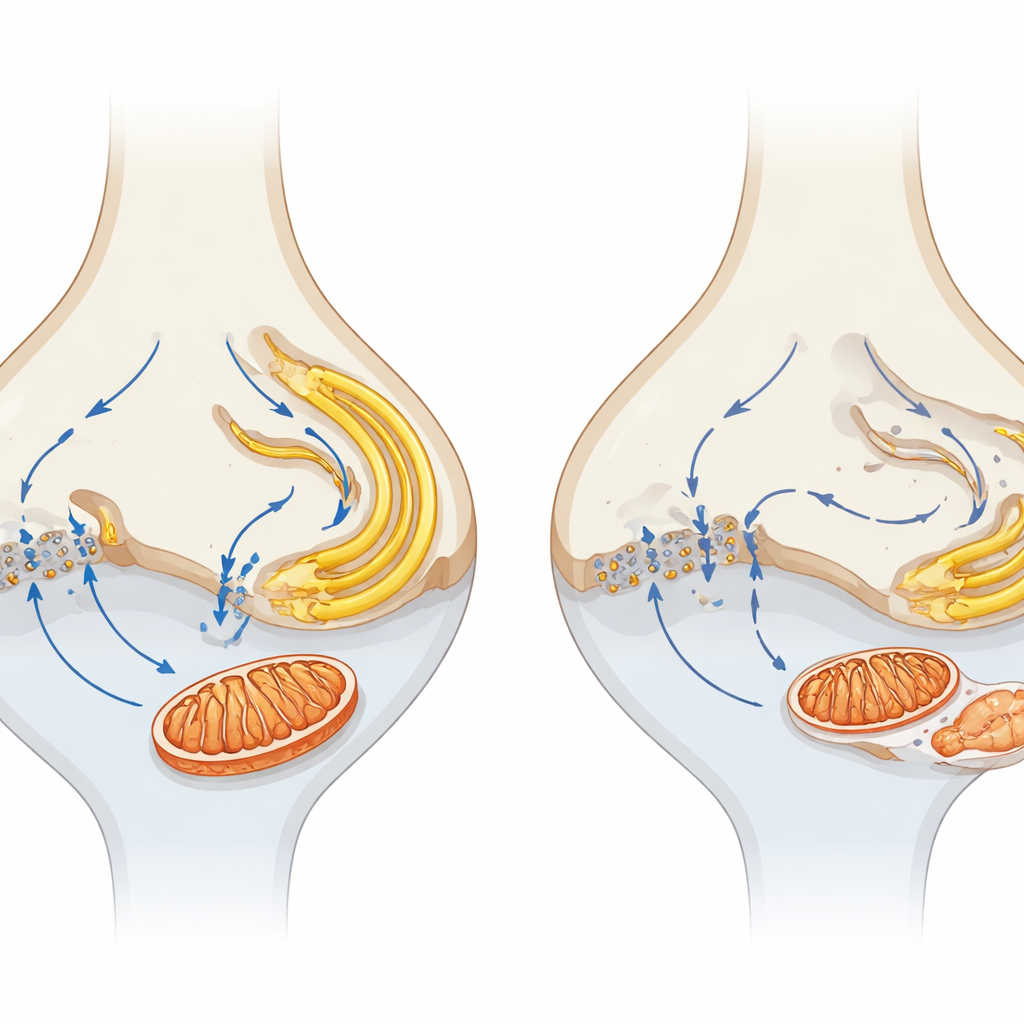
Küçük sinapsları uzun vadeli görme kaybına bağlamak
α2δ4 yok edilen fareleri Cav1.4 kanalından tamamen yoksun hayvanlarla karşılaştırarak, yazarlar daha şiddetli kanal bozukluğunun daha hızlı ve daha güçlü dejenerasyona yol açtığını buldu; bu da kalsiyum girişinin merkezi rolünü güçlendiriyor. Bir modeli şöyle öneriyorlar: α2δ4 kaybı Cav1.4 işlevini zayıflatır, sinapstek kalsiyum akışını bozarak onu yakındaki ER ve mitokondrilerden ayırır. Zamanla bu, sinaptik mitokondrilerin zarar görmesine, enerji üretiminin bozulmasına ve iç zarların stres altına girmesine yol açar; bunlar birlikte fotoreseptörleri yavaş, ilerleyici ölüme hazırlar. Bir okuyucu için ana çıkarım şudur: sağlıklı görme yalnızca fotoreseptörlerin varlığına değil, aynı zamanda onların küçük sinaptik enerji santrallerinin ve kalsiyum sinyallerinin hassas ayarına da bağlıdır; bu erken, yerel değişiklikleri hedeflemek, geniş bir yelpazedeki retinal hastalıklarda görmeyi korumak için yeni stratejiler sunabilir.
Atıf: Amieghemen, C.I., Ung, T.T., Huskin, G.N. et al. Dysfunction of α2δ4 leads to photoreceptor degeneration through disrupted synaptic mitochondria and calcium crosstalk. Cell Death Dis 17, 337 (2026). https://doi.org/10.1038/s41419-026-08587-3
Anahtar kelimeler: retinal dejenerasyon, fotoreseptörler, mitokondri, kalsiyum sinyalleşmesi, sinaptik disfonksiyon