Clear Sky Science · pt
Disfunção de α2δ4 leva à degeneração de fotorreceptores por meio da interrupção da comunicação entre mitocôndrias sinápticas e cálcio
Por que essa pesquisa ocular é importante
A perda de visão por degeneração retiniana costuma ser permanente, e tratamentos que realmente protejam as células sensíveis à luz do olho ainda são raros. Este estudo investiga uma questão fundamental: como pequenos problemas nas conexões entre células na retina podem, gradualmente, culminar na morte dessas células e, por fim, na cegueira? Ao acompanhar um defeito genético específico encontrado em algumas pessoas com doenças visuais hereditárias, os autores revelam um culpado inesperado — pequenas usinas de energia nas terminações nervosas dos fotorreceptores — e traçam como sinais de cálcio perturbados nas sinapses podem, ao longo do tempo, comprometer a saúde de toda a célula.
Da visão noturna falha aos sensores de luz moribundos
O trabalho centra-se nos fotorreceptores, os bastonetes e cones que convertem luz em sinais elétricos. Na base dessas células, formam-se sinapses especializadas que liberam continuamente sinais químicos para neurônios downstream. Uma proteína chamada α2δ4 ajuda a montar e estabilizar um complexo de canais de cálcio (Cav1.4) nessas sinapses, e mutações em seu gene têm sido associadas a distrofias retinianas humanas. Pacientes frequentemente apresentam problemas precoces na transmissão dos sinais dos fotorreceptores para as células bipolares, mas podem não perder grandes quantidades de fotorreceptores por muitos anos. Usando camundongos geneticamente modificados para não expressar α2δ4, os pesquisadores buscaram entender como um defeito sináptico aparentemente “local” acaba levando ao afinamento lento da camada que contém os corpos celulares dos fotorreceptores.
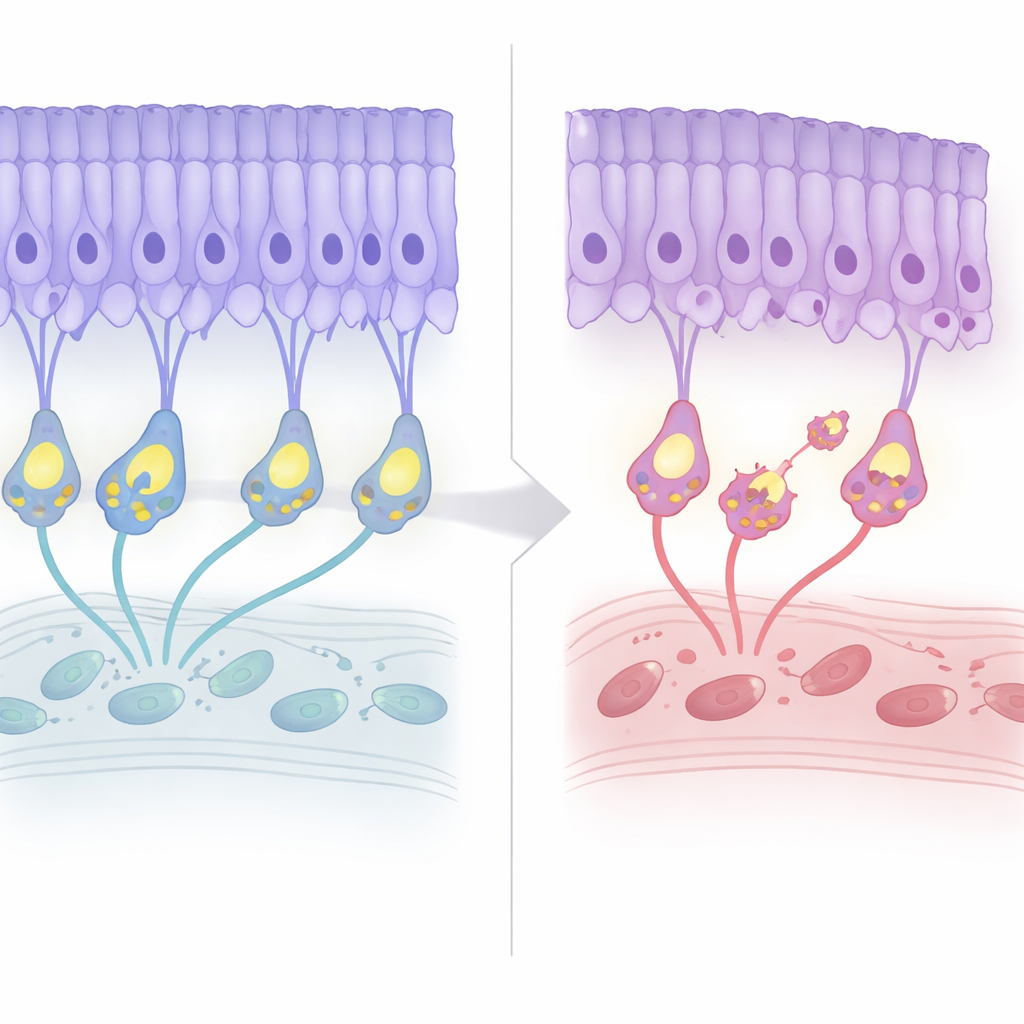
Declínio estrutural lento com sinais de aviso precoces
A equipe acompanhou as retinas desses camundongos ao longo da vida. Nos primeiros meses, a arquitetura geral parecia normal, e gravações elétricas sugeriam que a detecção de luz em si permanecia amplamente intacta. Por volta de sete meses de idade, contudo, a camada de núcleos dos fotorreceptores começou a afinar cerca de 20% e então se estabilizou, espelhando a degeneração branda de início tardio observada em pacientes. Curiosamente, marcadores de morte celular programada surgiram antes, antes da perda celular evidente. Ao mesmo tempo, a “fiação” se reorganizou: os terminais dos fotorreceptores retraíram-se de sua camada habitual, e os dendritos das células bipolares cresceram para cima para encontrá-los, formando conexões ectópicas. Apesar desse remodelamento, a eficiência da transmissão sináptica — avaliada pela razão entre sinais elétricos downstream e upstream — permaneceu consistentemente baixa, mas não piorou com a idade.
Usinas de energia na sinapse sob estresse
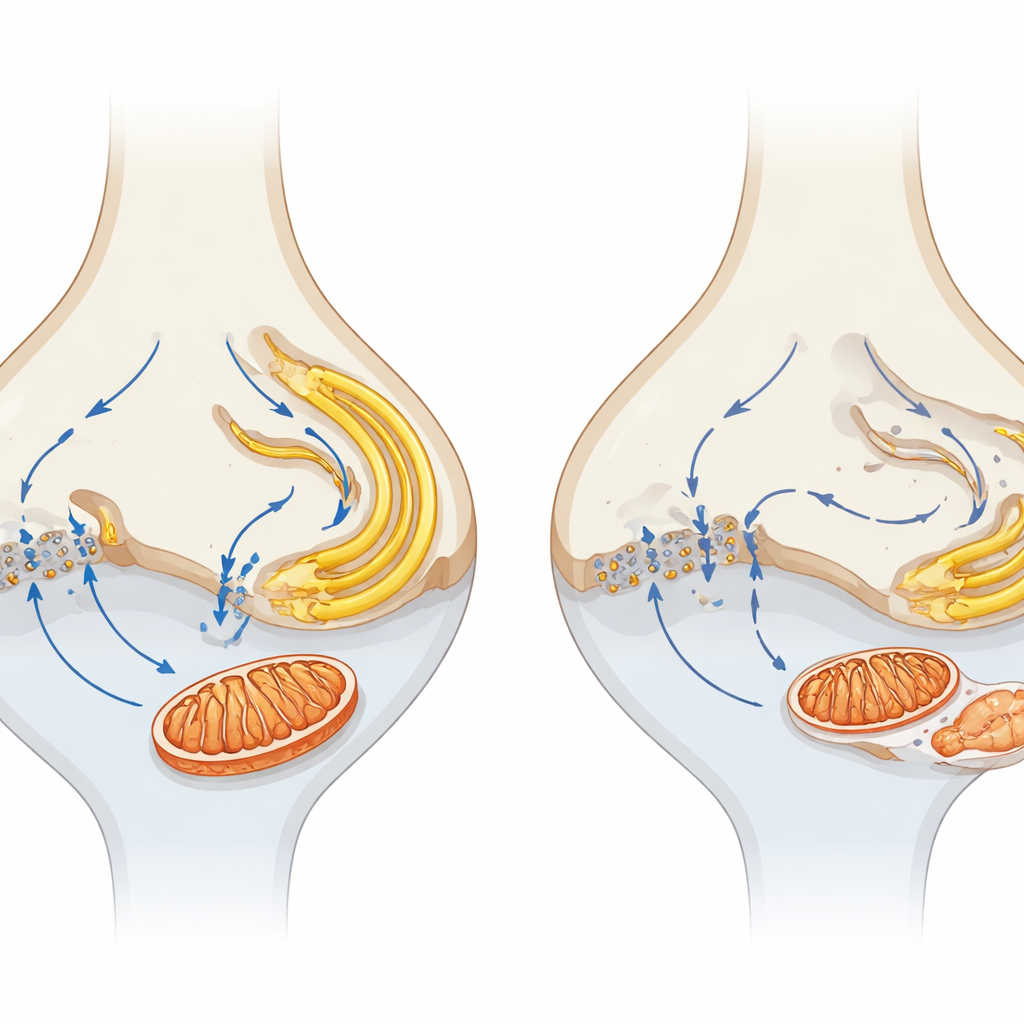
Para investigar o que acontece antes das células morrerem, os autores compararam a composição proteica de retinas jovens mutantes e normais. A mudança precoce mais marcante foi um declínio amplo em componentes do ciclo do ácido tricarboxílico (TCA), uma via central para a geração de energia. A microscopia confirmou que as mitocôndrias, os organelos que hospedam esse ciclo, foram especialmente afetadas nas sinapses dos fotorreceptores. Em camundongos saudáveis, esses terminais abrigam mitocôndrias proeminentes; em animais deficientes em α2δ4, as mitocôndrias sinápticas eram consideravelmente menores e menos numerosas, particularmente nos terminais de cones, muito antes da degeneração difundida. Marcadores mitocondriais na camada sináptica diminuíram, e algumas mitocôndrias pareceram deslocadas para a camada de núcleos dos fotorreceptores. Em contraste, as mitocôndrias no segmento interno — o principal polo metabólico do fotorreceptor — foram relativamente preservadas no início, destacando uma vulnerabilidade especial das mitocôndrias sinápticas.
Conversas de cálcio quebradas entre compartimentos celulares
Como α2δ4 faz parte de um complexo de canais de cálcio, a equipe testou se o manuseio de cálcio perturbado poderia subjacir os problemas mitocondriais. Em fotorreceptores saudáveis, o cálcio que entra pelos canais Cav1.4 na sinapse é estreitamente coordenado com o armazenamento e a liberação de cálcio pelo retículo endoplasmático (RE) e a captação pelas mitocôndrias, criando um microcircuito que liga atividade elétrica ao suprimento de energia. Nos camundongos mutantes, proteínas que liberam cálcio do RE (como o receptor de rianodina RYR2) e um transportador mitocondrial chave de cálcio (MCU) foram especificamente reduzidos na camada sináptica. Marcadores de estresse no RE estavam elevados, sugerindo que esse compartimento também estava sob tensão. Juntas, essas alterações apontam para uma quebra na “conversa” local de cálcio entre membrana celular, RE e mitocôndrias exatamente onde ocorre a sinalização sináptica.
Conectando sinapses minúsculas à perda de visão a longo prazo
Ao comparar camundongos nocaute para α2δ4 com animais que carecem completamente do canal Cav1.4, os autores descobriram que uma interrupção mais severa do canal leva a uma degeneração mais rápida e intensa, reforçando o papel central da entrada de cálcio. Eles propõem um modelo no qual a perda de α2δ4 enfraquece a função do Cav1.4, perturbando o fluxo de cálcio na sinapse e desconectando-o do RE e das mitocôndrias nas proximidades. Com o tempo, isso leva a mitocôndrias sinápticas danificadas, produção de energia comprometida e estresse em membranas internas, que em conjunto predispõem os fotorreceptores a uma morte lenta e progressiva. Para o leitor leigo, a percepção chave é que a visão saudável depende não apenas da presença de fotorreceptores, mas de manter suas pequenas usinas sinápticas e sinais de cálcio finamente ajustados; alvos que atuem nessas mudanças locais e precoces podem oferecer novas estratégias para preservar a visão em uma ampla gama de doenças retinianas.
Citação: Amieghemen, C.I., Ung, T.T., Huskin, G.N. et al. Dysfunction of α2δ4 leads to photoreceptor degeneration through disrupted synaptic mitochondria and calcium crosstalk. Cell Death Dis 17, 337 (2026). https://doi.org/10.1038/s41419-026-08587-3
Palavras-chave: degeneração retinal, fotorreceptores, mitocôndrias, sinalização por cálcio, disfunção sináptica