Clear Sky Science · ru
Дисфункция α2δ4 приводит к дегенерации фоторецепторов через нарушение митохондрий синапсов и кальциевого перекрестного взаимодействия
Почему это исследование глаза важно
Потеря зрения вследствие дегенерации сетчатки обычно необратима, а эффективных методов защиты светочувствительных клеток глаза пока немного. В этом исследовании поставлен фундаментальный вопрос: как мелкие нарушения на соединениях между клетками сетчатки со временем накапливаются и приводят к гибели клеток и, в конечном счёте, к слепоте? Проследив конкретный генетический дефект, встречающийся у некоторых людей с наследственными нарушениями зрения, авторы выявляют неожиданный виновник — небольшие энергетические «фермы» на нервных окончаниях фоторецепторов — и описывают, как нарушение кальциевой сигнализации в синапсах постепенно подрывает здоровье всей клетки.
От нарушенного ночного зрения до гибнущих светочувствительных клеток
Работа сосредоточена на фоторецепторах — палочках и колбочках, преобразующих свет в электрические сигналы. У их основания эти клетки формируют специализированные синапсы, которые постоянно выпускают химические сигналы нейронам следующего порядка. Белок α2δ4 помогает собирать и стабилизировать комплекс кальциевого канала (Cav1.4) в этих синапсах, и мутации в соответствующем гене связывают с человеческими дистрофиями сетчатки. У пациентов часто рано возникают проблемы с передачей сигналов от фоторецепторов к биполярным клеткам, хотя значительная потеря фоторецепторов может наступать лишь через годы. Используя мышей, у которых удалён α2δ4, исследователи попытались понять, как, казалось бы, «локальная» синаптическая аномалия в конечном счёте приводит к медленному истончению слоя с телами фоторецепторов.
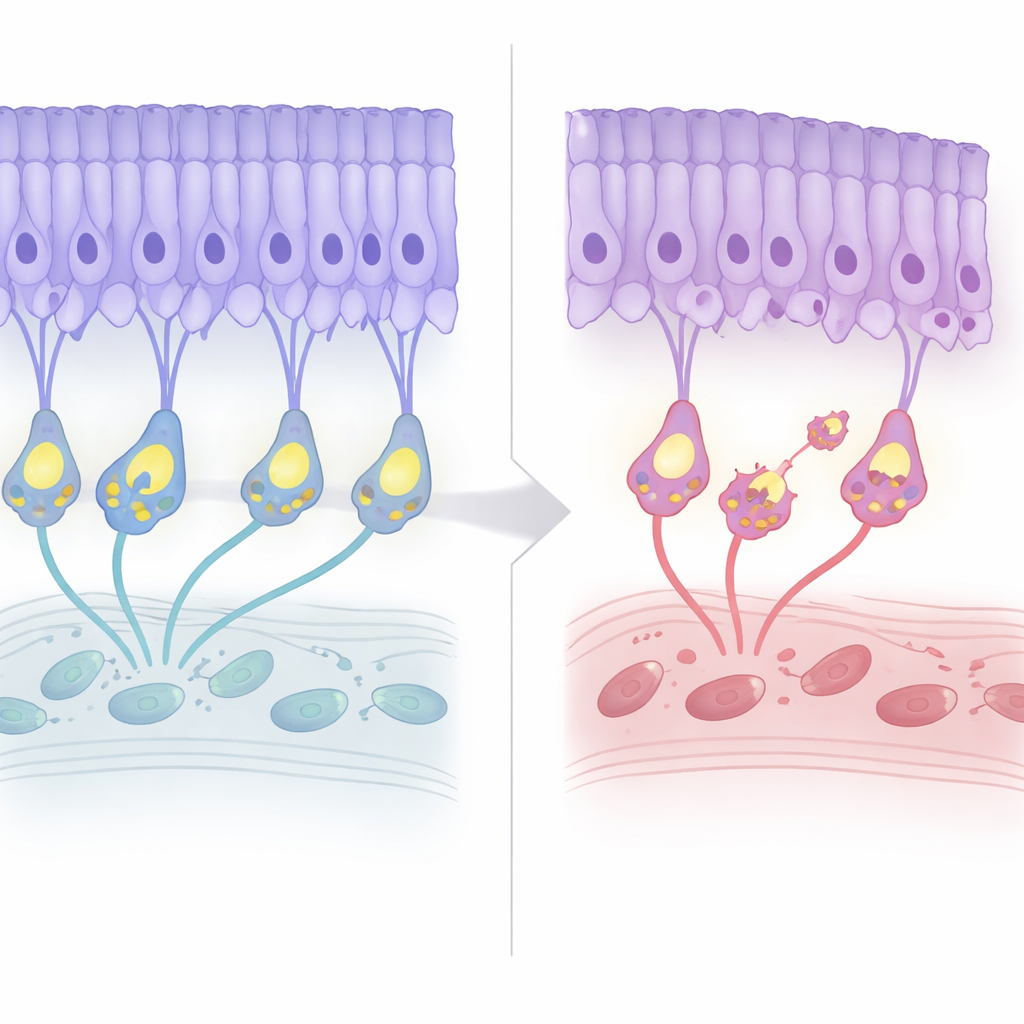
Медленный структурный упадок с ранними признаками
Команда наблюдала за сетчатками этих мышей на протяжении их жизни. В первые месяцы общая архитектоника выглядела нормально, и электрические записи указывали на то, что само обнаружение света в основном сохраняется. Однако примерно в семь месяцев слой ядер фоторецепторов начал истончаться примерно на 20 процентов и затем стабилизировался, что отражает мягкую, поздно возникающую дегенерацию, наблюдаемую у пациентов. Интересно, что маркеры программируемой клеточной гибели появлялись раньше, до явной потери клеток. Одновременно «проводка» реорганизовалась: терминали фоторецепторов оттянулись от обычного слоя, а дендриты биполярных клеток отрасли вверх, чтобы с ними встретиться, формируя эктопические соединения. Несмотря на такую реконфигурацию, эффективность синаптической передачи — судя по отношению электрических сигналов «вниз по цепочке» к «вверх по цепочке» — оставалась устойчиво низкой, но не ухудшалась с возрастом.
Энергетические «фермы» в синапсе под стрессом
Чтобы выяснить, что происходит до гибели клеток, авторы сравнили белковый состав молодых мутантных и нормальных сетчаток. Наиболее впечатляющим ранним изменением было широкое снижение компонентов цикла трикарбоновых кислот (ТКЦ), центрального пути генерации энергии. Микроскопия подтвердила, что митохондрии — органеллы, где проходит этот цикл — особенно поражены в синапсах фоторецепторов. В здоровых мышей в этих терминалях располагаются заметные митохондрии; у животных, лишённых α2δ4, синаптические митохондрии были заметно меньше и реже, особенно в конусных терминалях, задолго до широкомасштабной дегенерации. Митохондриальные маркеры в синаптическом слое уменьшались, и некоторые митохондрии казалось смещёнными в слой ядер фоторецепторов. Напротив, митохондрии во внутреннем сегменте — основном метаболическом хабе фоторецептора — относительно рано сохранялись, что подчёркивает особую уязвимость синаптических митохондрий.
Нарушённые кальциевые «разговоры» между отделами клетки
Поскольку α2δ4 является частью комплекса кальциевого канала, команда проверила, может ли нарушение кальциевого гомеостаза лежать в основе митохондриальных проблем. В здоровых фоторецепторах кальций, входящий через каналы Cav1.4 в синапсе, тесно согласован с хранением и высвобождением кальция эндоплазматическим ретикулумом (ЭР) и захватом митохондриями, образуя микросхему, которая связывает электрическую активность с энергетическим обеспечением. У мутантных мышей белки, ответственные за высвобождение кальция из ЭР (например, рианодиновый рецептор RYR2) и ключевой митохондриальный кальциевый транспортер (MCU), были специфически уменьшены в синаптическом слое. Повышались маркеры стресса в ЭР, что указывает на напряжение в этой компартменте. В совокупности эти изменения указывают на разрыв локального кальциевого «перекрёстного разговора» между мембраной клетки, ЭР и митохондриями именно там, где происходит синаптическая передача.
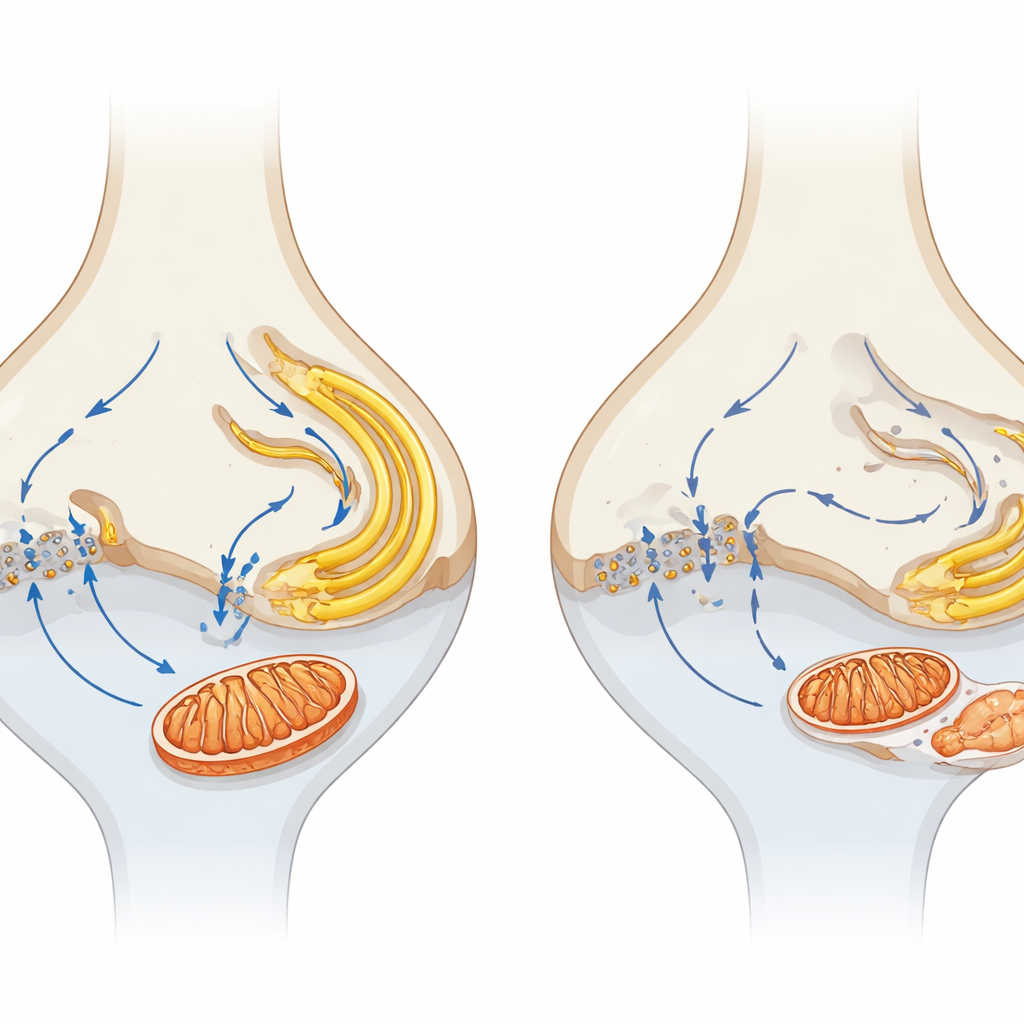
Связывание крошечных синапсов с долгосрочной потерей зрения
Сравнивая мышей с нокаутом α2δ4 и животных, полностью лишённых канала Cav1.4, авторы обнаружили, что более серьёзное нарушение канала ведёт к более быстрой и выраженной дегенерации, что усиливает центральную роль входа кальция. Они предлагают модель, при которой потеря α2δ4 ослабляет функцию Cav1.4, нарушая поток кальция в синапсе и рассоединяя его от соседних ЭР и митохондрий. Со временем это приводит к повреждению синаптических митохондрий, нарушению выработки энергии и стрессу внутренних мембран, что вместе делает фоторецепторы уязвимыми к медленной прогрессирующей гибели. Для неподготовленного читателя ключевой вывод таков: здоровое зрение зависит не только от наличия фоторецепторов, но и от поддержания их крошечных синаптических «электростанций» и тонко настроенных кальциевых сигналов; нацеливание на эти ранние локальные изменения может предложить новые стратегии сохранения зрения при широком спектре заболеваний сетчатки.
Цитирование: Amieghemen, C.I., Ung, T.T., Huskin, G.N. et al. Dysfunction of α2δ4 leads to photoreceptor degeneration through disrupted synaptic mitochondria and calcium crosstalk. Cell Death Dis 17, 337 (2026). https://doi.org/10.1038/s41419-026-08587-3
Ключевые слова: дегенерация сетчатки, фоторецепторы, митохондрии, кальциевая сигнализация, синаптическая дисфункция