Clear Sky Science · he
תפקוד לקוי של α2δ4 מוביל להידרדרות תאי הקולטנים האור דרך הפרעה במיטוכונדריה בסינפסה ובחילופי סידן
מדוע מחקר עיניים זה חשוב
אובדן ראייה כתוצאה מניוון רשתית הוא בדרך כלל קבוע, וטיפולים שמגינים באמת על תאי החישה לאור בעין עדיין נדירים. המחקר שואל שאלה בסיסית: כיצד בעיות קטנות בחיבורים בין התאים ברשתית יכולות בהדרגה להתגבר ולהביא למות התאים ואחר כך לעיוורון? בעקיבה אחרי פגם גנטי ספציפי הנמצא אצל חלק מהחולים בהפרעות ראייה תורשתיות, המחברים חושפים מטרה בלתי צפויה — תחנות ייצור אנרגיה זעירות בקצות העצבים של תאי הקולטנים לאור — ומציירים כיצד אותות סידן מופרעים בסינפסות יכולים לאט לאט לערער את בריאות התאים כולה.
מראייה לילה לקויה ועד מוות של חיישני אור
העבודה מתמקדת בתאי הקולטנים לאור, המטות והקנים שממירים אור לאותות חשמליים. בבסיסם, תאים אלה יוצרים סינפסות מיוחדות שמשחררות ברציפות אותות כימיים לתאים שעוברים איתם את המידע. חלבון שנקרא α2δ4 מסייע בהרכבה וביציבות של קומפלקס תעלות סידן (Cav1.4) בסינפסות אלה, ומוטציות בגנו נקשרו לדיסטורפיות רשתית אנושיות. אצל מטופלים נקלטים לעיתים תקלות מוקדמות בהעברת האותות מתאי הקולטנים לתאי הביפולרית אך יתכן שלא יאבדו מספר רב של תאים לאורך שנים רבות. באמצעות עכברים מהונדסים שאינם מבטאים α2δ4, החוקרים ניסו להבין כיצד פגם סינפטי שנראה "אזורי" בסופו של דבר מוביל לדילול איטי של השכבה שמכילה את גופי התאים של הקולטנים.
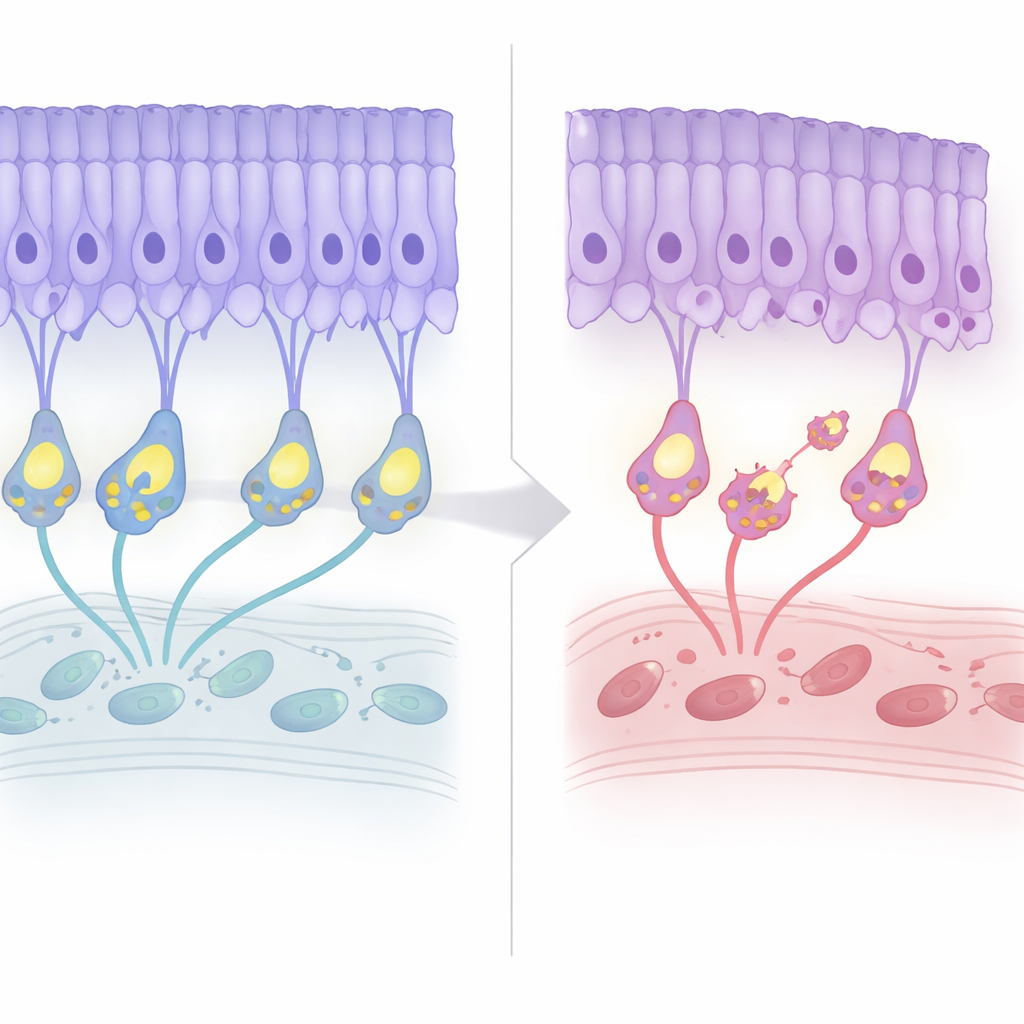
דהייה מבנית איטית עם סימני אזהרה מוקדמים
הצוות עקב אחרי הרשתיות של אותם עכברים לאורך חייהם. במהלך החודשים הראשונים המבנה הכללי נראה תקין, והרשומות החשמליות רמזו שגילוי האור עצמו נותר ברובו שלם. אולם סביב גיל שבעה חודשים החלה השכבה של גרעיני הקולטנים להדלדל בכ־20 אחוז ואז להיצמד לרמה זו, מה שמשקף את הניוון העדין בעל התחלה מאוחרת שנצפה בחולים. באופן מעניין, סמני ת programmed cell death הופיעו מוקדם יותר, לפני אובדן תאים ברור. באותו הזמן ה"חיווט" שונה: קצות התאים של הקולטנים נסוגו מהשכבה הרגילה שלהם, והדנדריטים של תאי הביפולרית צמחו מעלה כדי לפגוש אותם, ויצרו חיבורים אֶקטופיים. למרות רה־ארגון זה, היעילות של ההעברה הסינפטית — כפי שנמדדה ביחס האותות החשמליים היורדים ביחס לעלייה — נותרה גרועה בעקביות אך לא החמירה עם הגיל.
תחנות אנרגיה בסינפסה תחת לחץ
כדי לחקור מה קורה לפני מותו של התא, המחברים השוו את הרכב החלבונים של רשתיות צעירות של מוטנטים ונורמליים. השינוי המובהק המוקדם ביותר היה ירידה רחבה ברכיבי מעגל החומצה הטריקרבוקסילית (TCA), מסלול מרכזי לייצור אנרגיה. מיקרוסקופיה אישרה שמיטוכונדריה — האברונים שמארחים מסלול זה — הופיעו נפגעים במיוחד בסינפסות של תאי הקולטנים. בעכברים בריאים, טרמינלים אלה מכילים מיטוכונדריה בולטות; בחיות חסרות α2δ4, המיטוכונדריה הסינפטיות היו קטנות יותר ובמספרים פחותים באופן מובהק, ובפרט בטרמינלים של קונוסים, זמן רב לפני התדרדרות נרחבת. סמני מיטוכונדריה בשכבת הסינפסות ירדו, וחלק מהמיטוכונדריה נראו ממוינות לשכבת גרעיני הקולטנים. בניגוד לכך, המיטוכונדריה בחלק הפנימי של התא — הצומת המטבולי העיקרי של הקולטנים — נשמרו יחסית מוקדם, מה שמדגיש פגיעות מיוחדת של מיטוכונדריה סינפטית.
שיחות סידן שבורות בין רכיבי התא
מאחר שα2δ4 היא חלק מקומפלקס תעלות סידן, הקבוצה בדקה האם טיפול לא תקין בסידן עשוי לעמוד בבסיס הבעיות המיטוכונדריאליות. בתאי קולטנים בריאים, הסידן שנכנס דרך תעלות Cav1.4 בסינפסה מתואם בקפידה עם אחסון ושחרור סידן על־ידי הרשתית האנדופלזמטית (ER) ועם קליטה על־ידי מיטוכונדריה, ויוצר מיקרו־מעגל שמקשר בין פעילות חשמלית לאספקת אנרגיה. בעכברים המוטנטיים, חלבונים שמשחררים סידן מה־ER (כמו קולטן הראנודין RYR2) וטרנספורטר מפתחי סידן מיטוכונדריאלי מרכזי (MCU) הופחתו באופן ספציפי בשכבת הסינפסות. סמני לחץ ב־ER עלו, מה שמרמז שגם מתח זה הושת על המחסן התוך־תאי. יחד, השינויים הללו מצביעים על קריסה ב"שיח" המקומי של סידן בין ממברנת התא, ER והמיטוכונדריה בדיוק במקום שבו מתרחשת האיתות הסינפטי.
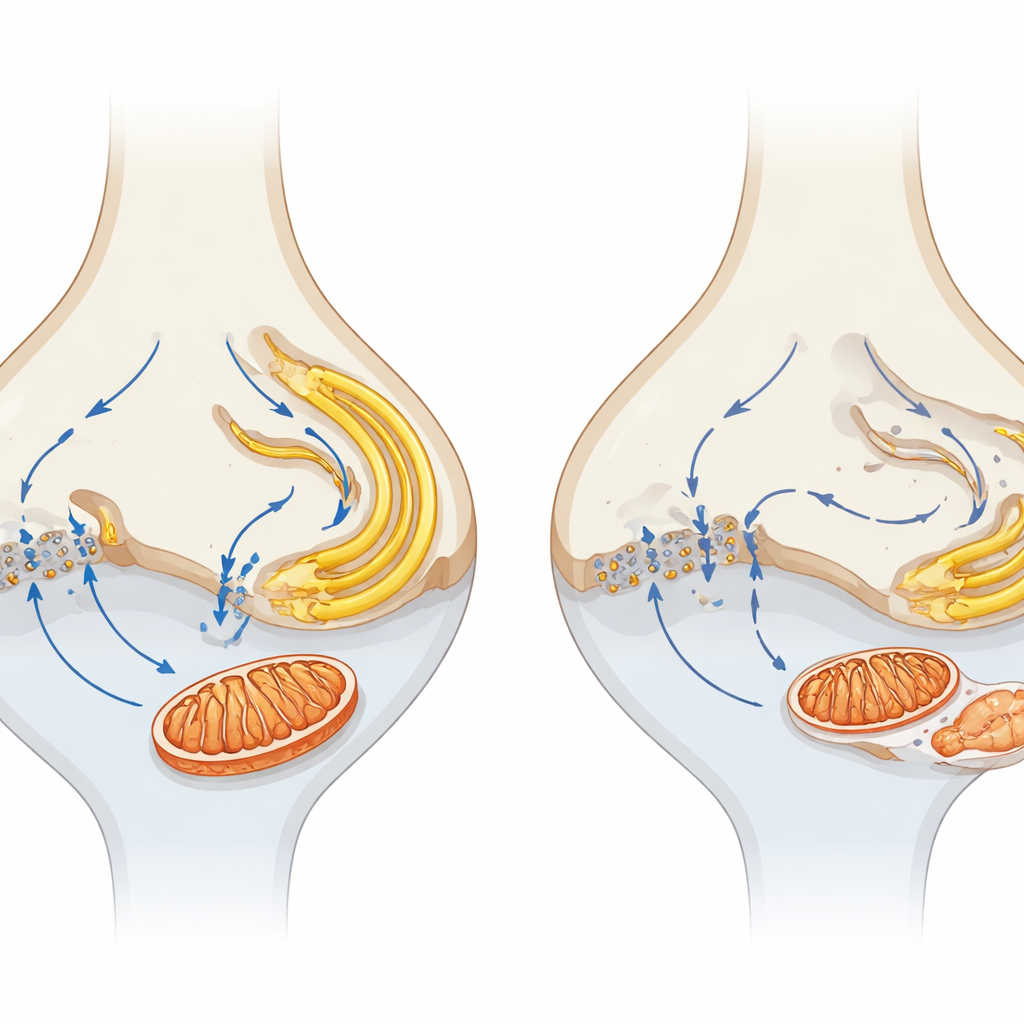
קישור בין סינפסות זעירות לאובדן ראייה לטווח הארוך
בהשוואת עכברי knockout ל־α2δ4 עם חיות שחסרות לחלוטין את תעלת Cav1.4, מצאו המחברים שהפרעה חמורה יותר בתעלה מובילה לניוון מהיר וחמור יותר, ומחזקת את התפקיד המרכזי של כניסת סידן. הם מציעים מודל שבו אובדן α2δ4 מחליש את תפקוד Cav1.4, מבלבל את זרימת הסידן בסינפסה ומנתק אותה מה־ER והמיטוכונדריה הסמוכים. עם הזמן, זה מוביל לפגיעה במיטוכונדריה הסינפטית, לפגיעה בייצור אנרגיה ולמתח בממברנות הפנימיות, שלכולם יחד מוכנים תאי הקולטנים למות איטי והתקדמותי. עבור הקורא הכללי, התובנה המרכזית היא שראייה בריאה תלויה לא רק בקיומם של תאי קולטנים, אלא בשמירה על תחנות הכוח הסינפטיות הקטנות שלהם ועל אותות הסידן מכוונים ומדויקים; פגיעה מוקדמת ומקומית אלה עשויה להציע אסטרטגיות חדשות לשימור הראייה במגוון רחב של מחלות רשתית.
ציטוט: Amieghemen, C.I., Ung, T.T., Huskin, G.N. et al. Dysfunction of α2δ4 leads to photoreceptor degeneration through disrupted synaptic mitochondria and calcium crosstalk. Cell Death Dis 17, 337 (2026). https://doi.org/10.1038/s41419-026-08587-3
מילות מפתח: ניוון רשתית, תאי קולט אור, מיטוכונדריה, אותות סידן, תפקוד סינפטי