Clear Sky Science · nl
Disfunctie van α2δ4 leidt tot degeneratie van fotoreceptoren via verstoorde synaptische mitochondriën en calcium‑crosstalk
Waarom dit oogonderzoek ertoe doet
Gezichtsverlies door retinale degeneratie is meestal blijvend en behandelingen die de lichtgevoelige cellen van het oog daadwerkelijk beschermen, zijn schaars. Deze studie stelt een fundamentele vraag: hoe kunnen kleine problemen bij de verbindingen tussen cellen in het netvlies langzaam uitgroeien tot het afsterven van die cellen en uiteindelijk tot blindheid? Door een specifiek genetisch defect te volgen dat bij sommige mensen met erfelijke visusstoornissen voorkomt, onthullen de auteurs een onverwachte schuldige—kleine energiecentrales in de zenuweinden van fotoreceptoren—en traceren ze hoe verstoorde calciumsignalen bij synapsen geleidelijk de gezondheid van de hele cel kunnen ondermijnen.
Van slecht nachtzicht naar afstervende lichtsensoren
Het werk richt zich op fotoreceptoren, de staafjes en kegeltjes die licht omzetten in elektrische signalen. Aan hun basis vormen deze cellen gespecialiseerde synapsen die continu chemische signalen naar downstream neuronen afgeven. Een eiwit genaamd α2δ4 helpt bij het samenstellen en stabiliseren van een calciumkanaalcomplex (Cav1.4) in deze synapsen, en mutaties in het bijbehorende gen zijn gekoppeld aan menselijke retinale dystrofieën. Patiënten vertonen vaak vroeg problemen met het doorgeven van signalen van fotoreceptoren naar bipolaire cellen, maar verliezen mogelijk niet gedurende vele jaren grote aantallen fotoreceptoren. Met muizen die zo zijn gefokt dat ze α2δ4 missen, wilden de onderzoekers begrijpen hoe een ogenschijnlijk „lokaal” synaptisch defect uiteindelijk leidt tot de langzame dunner wording van de laag die de cellichamen van fotoreceptoren bevat.
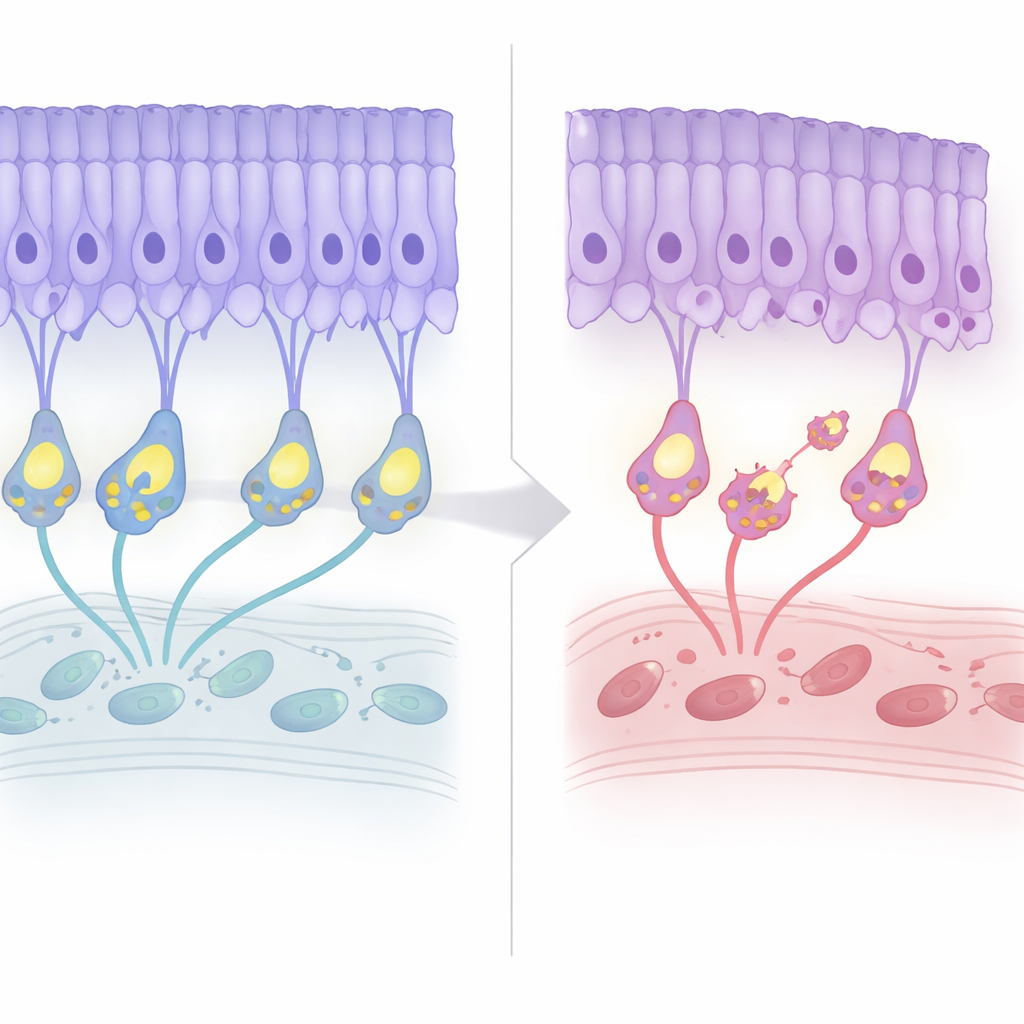
Langzame structurele achteruitgang met vroege waarschuwingssignalen
Het team volgde de netvliezen van deze muizen gedurende hun levensduur. In de eerste maanden leek de algemene architectuur normaal en suggereerden elektrische metingen dat lichtdetectie grotendeels intact bleef. Rond zeven maanden echter begon de laag met fotoreceptornuclei met ongeveer 20 procent dunner te worden en stabiliseerde daarna, wat de milde, laat optredende degeneratie die bij patiënten wordt gezien, weerspiegelt. Interessant genoeg verschenen merkers van geprogrammeerde celdood eerder, nog vóór duidelijk celverlies. Tegelijkertijd reorganiseerde de „bedrading”: fotoreceptorterminals trokken zich terug uit hun gebruikelijke laag, en de dendrieten van bipolaire cellen groeiden omhoog om ze te ontmoeten, waardoor ectopische verbindingen ontstonden. Ondanks deze herbouw bleef de efficiëntie van synaptische transmissie—gewaardeerd aan de hand van de verhouding van downstream tot upstream elektrische signalen—constant laag maar verslechterde niet met de leeftijd.
Synaptische energiecentrales onder stress
Om te onderzoeken wat er gebeurt vóórdat cellen afsterven, vergeleken de auteurs de eiwitsamenstelling van jonge mutant- en normale netvliezen. De meest opvallende vroege verandering was een brede afname van componenten van de tricarbonzuurcyclus (TCA), een centraal pad voor energieproductie. Microscopie bevestigde dat mitochondriën, de organellen die deze cyclus huisvesten, vooral getroffen waren bij fotoreceptorsynapsen. In gezonde muizen bevatten deze terminals prominente mitochondriën; bij α2δ4‑deficiënte dieren waren de synaptische mitochondriën duidelijk kleiner en talrijker minder, met name in coneterminals, lang vóór wijdverspreide degeneratie. Mitochondriale merkers in de synaptische laag daalden en sommige mitochondriën leken verplaatst naar de laag met fotoreceptornuclei. Daarentegen waren mitochondriën in het inner segment—het belangrijkste metabole knooppunt van de fotoreceptor—relatief goed bewaard in een vroeg stadium, wat wijst op een bijzondere kwetsbaarheid van synaptische mitochondriën.
Verstoorde calcium‑conversaties tussen compartimenten
Aangezien α2δ4 deel uitmaakt van een calciumkanaalcomplex, testte het team of verstoord calciumbeheer ten grondslag lag aan de mitochondriale problemen. In gezonde fotoreceptoren wordt calcium dat binnenkomt via Cav1.4‑kanalen in de synaps nauw gecoördineerd met calciumopslag en -afgifte door het endoplasmatisch reticulum (ER) en opname door mitochondriën, waarmee een microcircuit ontstaat dat elektrische activiteit koppelt aan energievoorziening. Bij de mutantmuizen waren eiwitten die calcium uit het ER vrijgeven (zoals de ryanodinereceptor RYR2) en een belangrijke mitochondriale calciumtransporter (MCU) specifiek verlaagd in de synaptische laag. Merkers van stress in het ER waren verhoogd, wat suggereert dat dit compartiment ook onder druk stond. Gezamenlijk wijzen deze verschuivingen op een afbraak van de lokale calcium‑„crosstalk” tussen celmembraan, ER en mitochondriën precies daar waar synaptische signalering plaatsvindt.
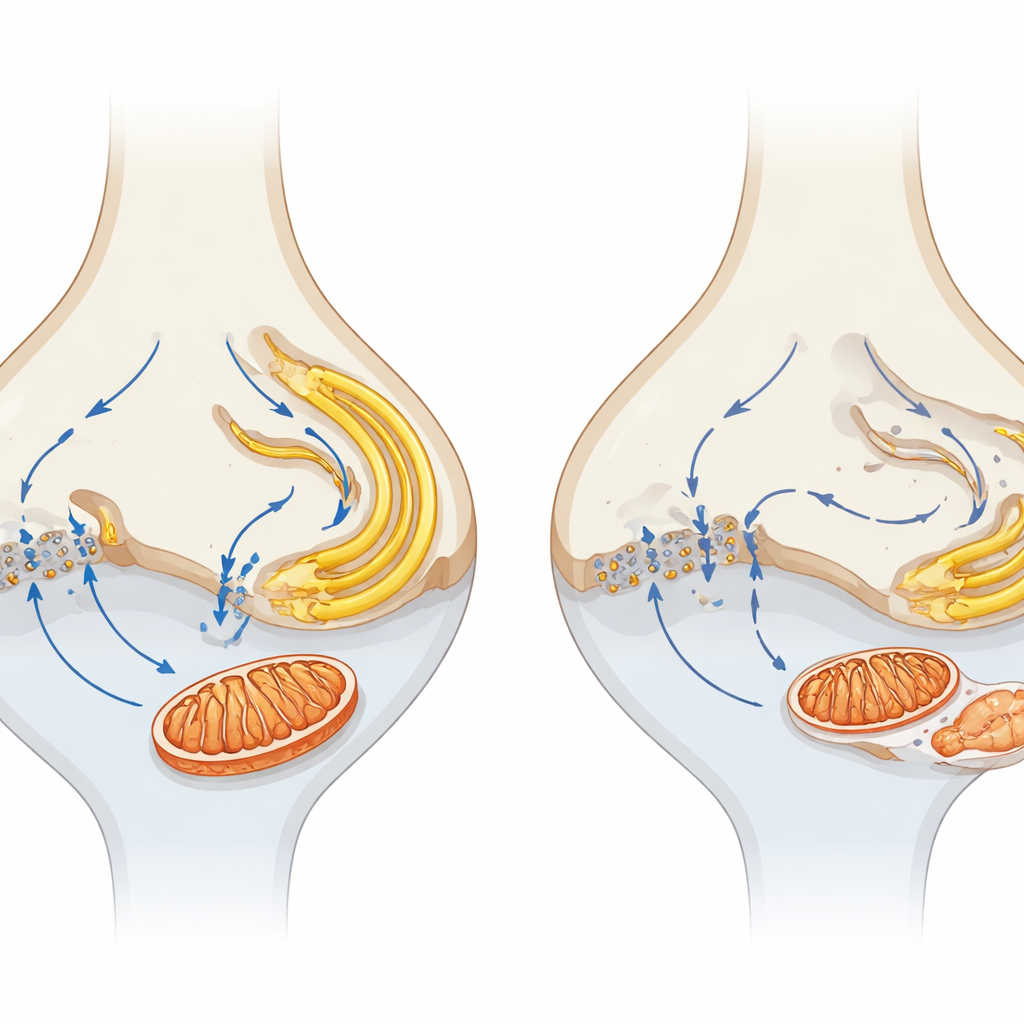
De koppeling van kleine synapsen aan langdurig verlies van zicht
Door α2δ4‑knockoutmuizen te vergelijken met dieren die het Cav1.4‑kanaal volledig missen, vonden de auteurs dat ernstiger kanaalverstoring leidt tot snellere en sterkere degeneratie, wat de centrale rol van calciuminstroom bevestigt. Ze stellen een model voor waarbij verlies van α2δ4 de Cav1.4‑functie verzwakt, de calciumstroom bij de synaps verstoort en de koppeling met nabijgelegen ER en mitochondriën ontkoppelt. In de loop van de tijd leidt dit tot beschadigde synaptische mitochondriën, verminderde energieproductie en stress in interne membranen, die samen fotoreceptoren vatbaar maken voor langzame, progressieve celdood. Voor een niet‑specialistische lezer is het belangrijkste inzicht dat gezond zicht niet alleen afhangt van het hebben van fotoreceptoren, maar van het nauwkeurig in stand houden van hun kleine synaptische energiecentrales en calcium‑signalen; het richten op deze vroege, lokale veranderingen zou nieuwe strategieën kunnen bieden om het gezichtsvermogen te behouden bij een breed scala aan retinale aandoeningen.
Bronvermelding: Amieghemen, C.I., Ung, T.T., Huskin, G.N. et al. Dysfunction of α2δ4 leads to photoreceptor degeneration through disrupted synaptic mitochondria and calcium crosstalk. Cell Death Dis 17, 337 (2026). https://doi.org/10.1038/s41419-026-08587-3
Trefwoorden: retinale degeneratie, fotoreceptoren, mitochondriën, calciumsignaalgeving, synaptische disfunctie