Clear Sky Science · zh
组蛋白乳酰化驱动的反馈回路调节嘧啶代谢以促进口腔致癌
这为何与口腔健康相关
口腔癌常以口腔内的小白斑起始,可能在无声中发展为危及生命的疾病。本研究揭示了前癌变口腔细胞在糖代谢方式上的改变如何形成一个自加速环路,推动它们向侵袭性癌变发展。通过逐步追踪这一回路,研究者发现了可能被用来预防或延缓口腔肿瘤的新分子“脆弱点”。
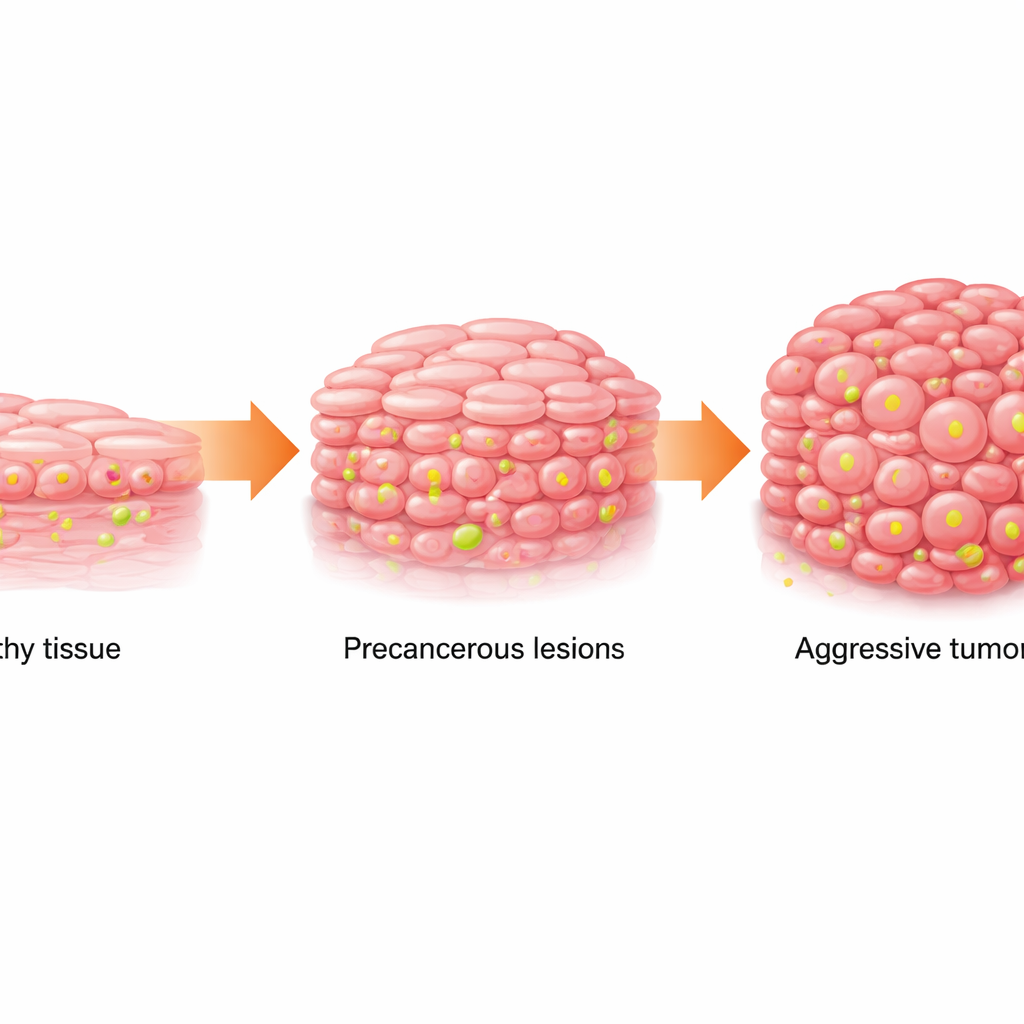
从正常组织到危险白斑
口腔鳞状细胞癌(OSCC)是常见且致命的口腔癌。它通常逐步发展:健康的上皮细胞变得异常(称为口腔白斑,表现为白色斑块),随后进展为癌。团队检验了来自正常组织、白斑和 OSCC 的人类样本,以及公共癌症数据库和单细胞测序数据。他们发现,随着组织从正常向前癌变再到癌变,其代谢发生了转变:细胞更依赖快速的糖酵解并积累更高水平的乳酸这一代谢副产物。与此同时,一种位于组蛋白上的特定化学修饰——称为 H3K18 的组蛋白乳酰化——逐渐增强。
当乳酸变为遗传开关
乳酸通常被视为代谢废物,但在这里它更像是一种信号。研究者证明,高乳酸水平促进组蛋白乳酰化,从而改变基因的开关状态。在细胞培养和舌癌小鼠模型中,阻断糖酵解或降低乳酸可减少总体组蛋白乳酰化,特别是 H3K18 修饰。这抑制了细胞生长、克隆形成以及细胞运动和侵袭能力——这些都是癌症的关键特征。在暴露于诱发舌肿瘤化合物的小鼠中,使用糖酵解抑制剂使病变面积缩小、癌变点减少,且未见明显的肝肾毒性,提示针对该轴线的干预既可能有效又可忍受。
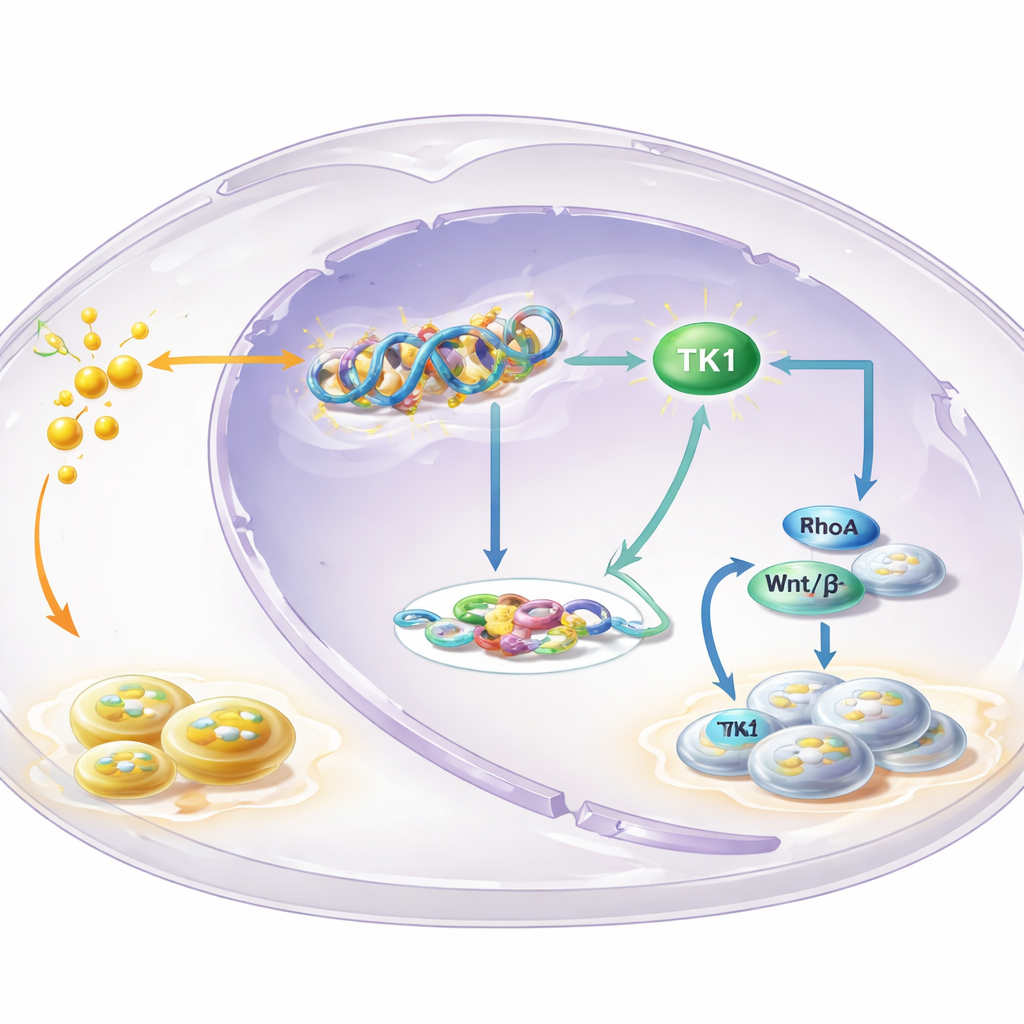
回路核心的一种关键酶
为了确定哪些基因受 H3K18 乳酰化调控,团队绘制了该标记在基因组上的分布并与基因表达数据结合分析。一个突出目标是胸苷激酶 1(TK1),这是一种参与构建 DNA 前体的酶。他们发现 H3K18 乳酰化在 TK1 基因的调控区富集,而阻断糖酵解会降低 TK1 活性和细胞内的 DNA 前体储备,尤其是 dTTP。TK1 在白斑和 OSCC 中的含量高于正常组织,且肿瘤中 TK1 水平较高的患者往往预后更差。实验性降低 TK1 可减缓细胞增殖,使细胞停滞于细胞周期的早期阶段,并在小鼠中缩小肿瘤,表明 TK1 是驱动因子而非旁观者。
TK1 如何推动信号并反馈到代谢
故事并不止于 DNA 前体。TK1 活动的产物改变了两种相关分子 GTP 与 GDP 之间的平衡,这两者控制着称为小 GTP 酶的开关。研究聚焦于其中一种开关 RhoA,RhoA 已知影响细胞形态、运动和生长。阻断糖酵解时,GTP/GDP 比率下降,RhoA 活性降低——但通过强制表达更多 TK1 可恢复这两者。反过来,这增强了 Wnt/β‑连环蛋白通路,这是一条强大的促生长信号通路。活化的 β‑连环蛋白增加 c‑Myc 和糖酵解酶 LDHA 的产生,从而进一步提高乳酸水平。更多乳酸又促进更多的组蛋白乳酰化和 TK1 激活,闭合了一个自我强化的回路,不断推动细胞走向失控生长。
不同口腔癌的不同路径
研究者还比较了 HPV 阴性与 HPV 阳性的口腔癌细胞。阻断糖酵解和乳酰化在显著减缓 HPV 阴性细胞方面效果显著,而 HPV 阳性细胞对该通路的依赖性较低,可能是由于病毒性致癌蛋白提供了替代的生长信号。在患者样本中,H3K18 乳酰化标记与肿瘤抑制蛋白 p53 的异常模式相关,p53 在 OSCC 中经常发生突变,且通常抑制糖酵解和 DNA 复制。这提示 p53 丧失与乳酸驱动回路可能协同,加速早期瘤变进程。
对未来治疗的意义
总体而言,该研究表明在早期口腔病变中,过度的糖酵解产生乳酸,乳酸并非单纯废物——它修饰组蛋白、激活 TK1、促进 DNA 前体与生长信号,并通过 Wnt 驱动的循环进一步提升乳酸产生。打破这一糖酵解–乳酰化–TK1–β‑连环蛋白的反馈回路中的任何关键环节——例如糖酵解、组蛋白乳酰化、TK1、RhoA 或 Wnt 信号——都有可能为阻止白斑向癌变转变或治疗已确诊 OSCC 提供新的策略,尤其对 HPV 阴性患者。
引用: Wang, Y., Geng, Y., Chen, Y. et al. Histone lactylation-driven feedback loop modulates pyrimidine metabolism to promote oral carcinogenesis. Cell Death Dis 17, 316 (2026). https://doi.org/10.1038/s41419-026-08580-w
关键词: 口腔癌, 肿瘤代谢, 组蛋白乳酰化, 嘧啶合成, Wnt 信号通路