Clear Sky Science · ja
ヒストンのラクトリル化駆動フィードバックループがピリミジン代謝を調節し、口腔発がんを促進する
口内の健康にとってなぜ重要か
口腔がんはしばしば口内の小さな白い斑点として始まり、静かに進行して生命を脅かす病気になることがあります。本研究は、前がん状態の口腔細胞が糖を燃やす仕組みの変化がどのように自己強化的なループを生み出し、それが細胞を完全ながんへと押し進めるかを明らかにします。このループを段階的にたどることで、腫瘍の予防や進行抑制に向けて狙える新たな分子上の「圧点」が示されます。
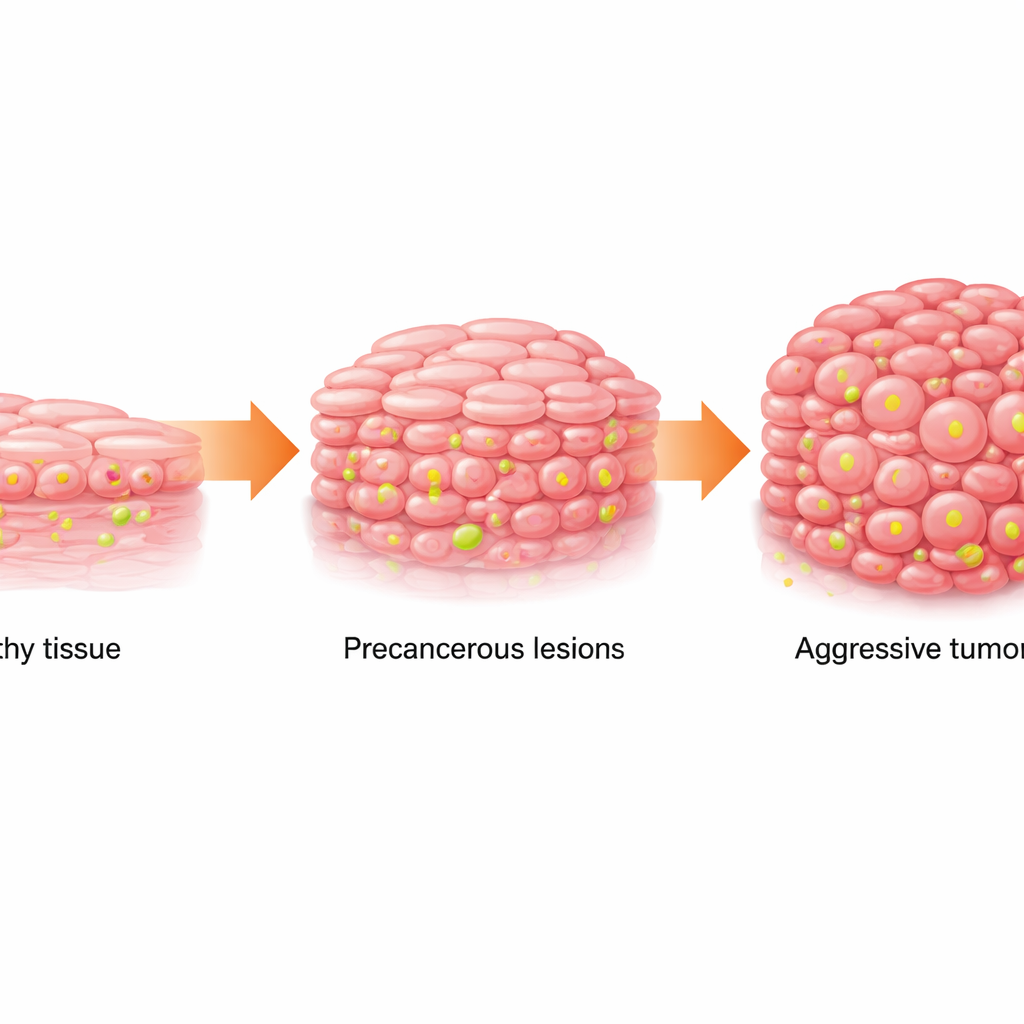
正常組織から危険な斑点へ
口腔扁平上皮癌(OSCC)は口腔に発生する一般的で致命的ながんです。通常は徐々に発生します:正常な上皮細胞が異常になり(白い斑点として現れる口腔白板症と呼ばれる状態)、そこからがんへ進行します。研究チームは正常組織、白板症、OSCCのヒトサンプルと公的がんデータベースや単一細胞解析のデータを調べました。その結果、組織が正常から前がん、がんへと移行するにつれて代謝がシフトし、細胞はより速い糖代謝(解糖)に依存し、代謝の副産物である乳酸を多く蓄積するようになっていることがわかりました。同時に、DNAを包むタンパク質(ヒストン)に付く特定の化学的修飾、H3K18と呼ばれる部位でのラクトリル化が段階的に強まっていました。
乳酸が遺伝子スイッチになるとき
乳酸は通常代謝の廃棄物と考えられがちですが、本研究ではシグナルのように働きます。高い乳酸濃度がヒストンのラクトリル化に取り込まれ、遺伝子のオン・オフを変えることが示されました。細胞培養系と舌がんのマウスモデルの双方で、解糖を阻害したり乳酸を低下させると、全体的なヒストンのラクトリル化、特にH3K18のマークが減少しました。これにより細胞増殖、コロニー形成、移動や浸潤能が抑制され、がんの主要な性質が弱まりました。舌腫瘍を誘導する化学物質に曝露されたマウスでは、解糖阻害剤で病変面積とがん性斑点の数が減少し、明らかな肝臓や腎臓の損傷は観察されませんでした。これはこの軸を標的にすることが有効かつ許容できる可能性を示唆します。
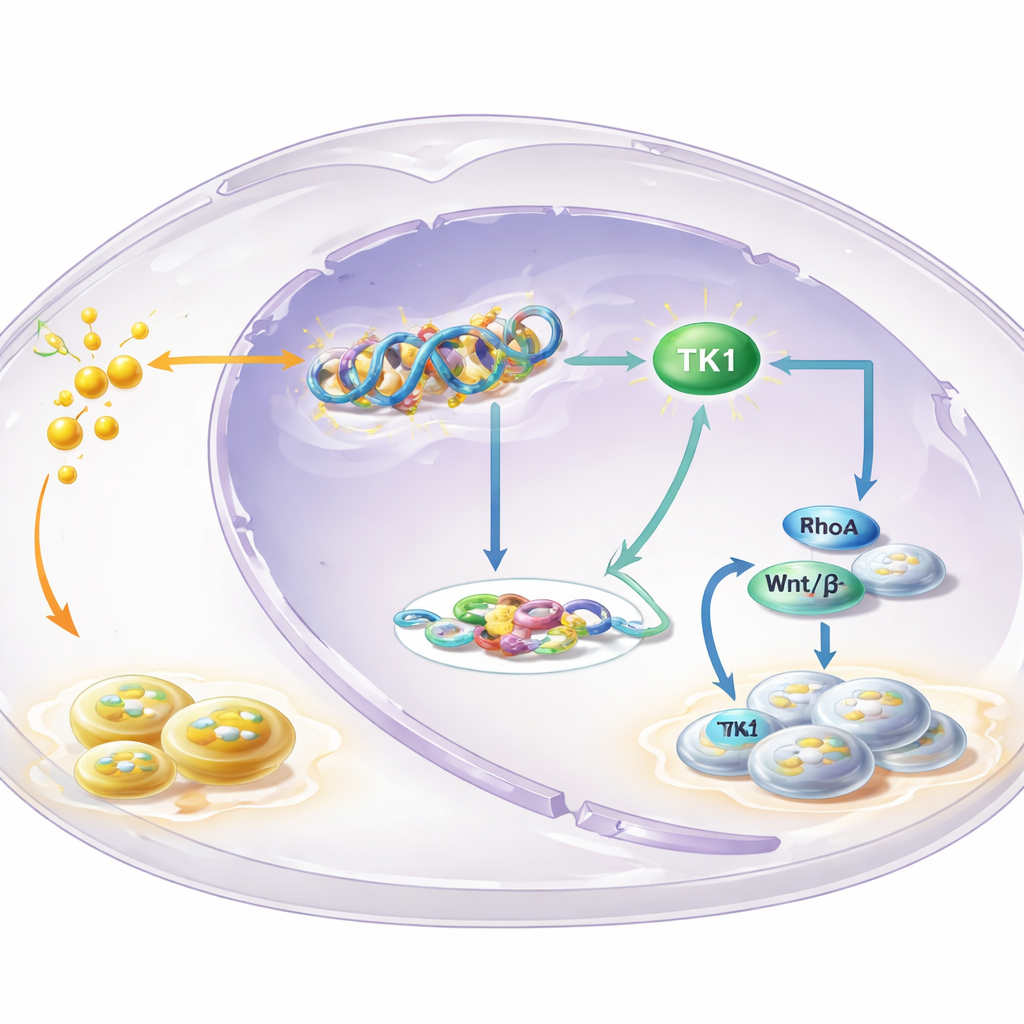
ループの中心にある主要酵素
どの遺伝子がH3K18のラクトリル化で制御されているかを特定するため、チームはこの修飾がゲノム上のどこに存在するかをマッピングし、遺伝子発現データと組み合わせました。際立っていたのがチミジンキナーゼ1(TK1)で、これはDNAの構成要素を作るのに関わる酵素です。H3K18ラクトリル化はTK1遺伝子の制御領域に濃縮しており、解糖を阻害するとTK1の活性と細胞内のDNA前駆体プール、特にdTTPが減少しました。TK1は正常組織に比べ白板症やOSCCでより豊富に存在し、腫瘍でTK1が高い患者は生存率が低い傾向にありました。実験的にTK1を減らすと細胞増殖が遅くなり、細胞周期の早期段階での停止が生じ、マウスの腫瘍は縮小しました。これによりTK1は単なる随伴因子ではなく駆動因子であることが示されます。
TK1がシグナルを押し進め代謝にフィードバックする仕組み
話はDNAの材料だけにとどまりません。TK1の活性産物はGTPとGDPという関連する二つの分子のバランスを変え、小さなGTPアーゼとして知られるスイッチ群を制御します。研究は、細胞の形状、運動、増殖に影響することが知られるRhoAというスイッチに着目しました。解糖が阻害されるとGTP/GDP比は下がりRhoAの活性は低下しましたが、TK1を増やすとこれらは回復しました。これがさらにWnt/β-カテニン経路を活性化し、強力な増殖促進シグナルとなります。活性化したβ-カテニンはc-Mycや解糖酵素LDHAの産生を増やし、これがさらに乳酸を増やします。増えた乳酸はヒストンのラクトリル化とTK1の活性化にさらに燃料を供給し、細胞を制御不能な増殖へと押し進める自己強化ループを閉じます。
異なる口腔がんでの異なる経路
研究者らはHPV陰性とHPV陽性の口腔がん細胞も比較しました。解糖やラクトリル化を阻害するとHPV陰性細胞は強く減速しましたが、HPV陽性細胞はこの経路への依存度が低く、これはウイルス由来のがん促進タンパク質が代替の増殖シグナルを供給しているためと考えられます。患者サンプルではH3K18ラクトリル化のマークは腫瘍抑制タンパク質p53の異常なパターンと相関していました。p53はOSCCでしばしば変異し、通常は解糖やDNA複製を抑える働きを持ちます。これはp53の喪失と乳酸駆動ループが協調して早期の腫瘍進展を加速している可能性を示唆します。
今後の治療にとっての意味
総じて、本研究は初期の口腔病変において過剰な糖代謝が乳酸を生み出し、それが単なる廃棄物としてとどまらずヒストンを装飾し、TK1をオンにし、DNA前駆体と増殖シグナルを高め、さらにWnt駆動のサイクルを活性化して更なる乳酸を生み出すことを示しています。この解糖–ラクトリル化–TK1–β-カテニンのフィードバックループを解糖、ヒストンのラクトリル化、TK1、RhoA、あるいはWntシグナルなどの主要な段階で断ち切ることは、白板症ががんに進展するのを防ぐ新たな方法や、確立したOSCCを治療する手段、特にHPV陰性患者に対する治療戦略を提供する可能性があります。
引用: Wang, Y., Geng, Y., Chen, Y. et al. Histone lactylation-driven feedback loop modulates pyrimidine metabolism to promote oral carcinogenesis. Cell Death Dis 17, 316 (2026). https://doi.org/10.1038/s41419-026-08580-w
キーワード: 口腔がん, 腫瘍代謝, ヒストンのラクトリル化, ピリミジン合成, Wntシグナル伝達