Clear Sky Science · tr
Histon laktilasyonu kaynaklı geri besleme döngüsü, pirimidin metabolizmasını düzenleyerek ağız karsinogenezini destekler
Ağız sağlığı için bunun önemi
Ağız kanseri genellikle ağız içinde küçük bir beyaz leke olarak başlar ve sessizce hayatı tehdit eden bir hastalığa ilerleyebilir. Bu çalışma, kanser öncesi ağız hücrelerinin şekeri yakma biçimindeki değişikliklerin, onları tam kanser hâline götüren kendi kendini güçlendiren bir döngü yarattığını ortaya koyuyor. Araştırmacılar bu döngüyü adım adım takip ederek, önleme veya ağız tümörlerini yavaşlatma amaçlı hedeflenebilecek yeni moleküler "düğüm noktalarını" ortaya koyuyorlar.
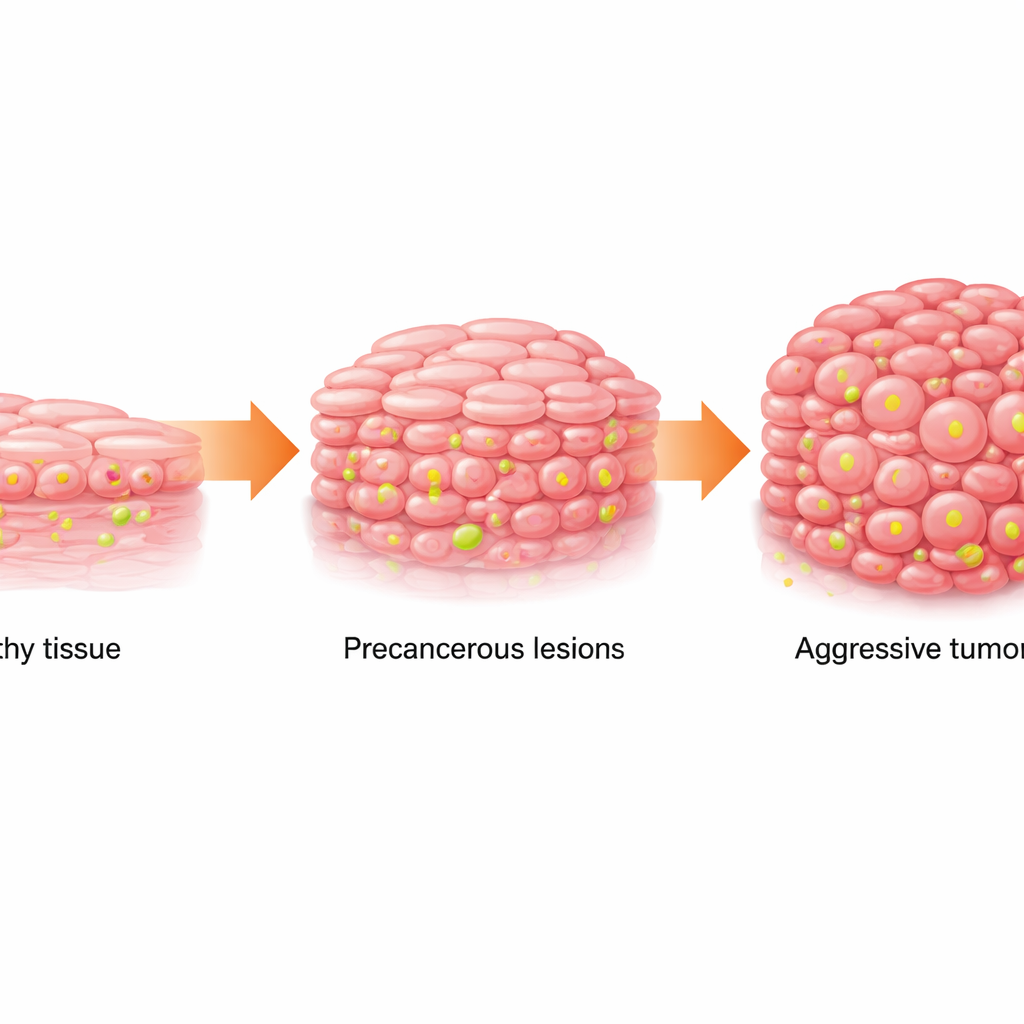
Normal dokudan tehlikeli yamalara
Ağız skuamöz hücreli karsinomu (OSCC), ağızda sık görülen ve ölümcül olabilen bir kanserdir. Genellikle kademeli olarak gelişir: sağlıklı örtü hücreleri anormal hâle gelir (ağız lökoplaki adı verilen ve beyaz yamalar olarak görülen bir durum) ve sonra kansere ilerler. Ekip normal doku, lökoplaki ve OSCC’den alınmış insan örneklerini, halka açık kanser veritabanları ve tek hücre dizileme verileriyle birlikte inceledi. Doku normalden kanser öncesine ve sonra kansere ilerledikçe metabolizmasının kaydığını; hücrelerin hızlı şeker yakımına (glikoliz) daha çok bağımlı hâle geldiğini ve laktat adlı metabolik yan ürünün seviyelerinin arttığını buldular. Aynı zamanda DNA paketleyen proteinlerdeki belirli bir kimyasal işaret, H3K18 adlı konumda histon laktilasyon, giderek güçlendi.
Laktat genetik bir anahtara dönüştüğünde
Laktat genellikle metabolik bir atık olarak düşünülür, ancak burada daha çok bir sinyal gibi davranıyor. Araştırmacılar yüksek laktat seviyelerinin histon laktilasyonunu beslediğini ve bunun genlerin açılıp kapanma biçimini değiştirdiğini gösterdiler. Hem hücre kültürlerinde hem de dil kanseri fare modelinde glikolizin engellenmesi veya laktatın düşürülmesi genel histon laktilasyonunu ve özellikle H3K18 işaretini azalttı. Bu, hücre büyümesini, koloni oluşturmayı ve hücrelerin hareket ve invazyon yeteneğini—kanserin ana özelliklerini—bastırdı. Dil tümörlerini indükleyen bir kimyasal ile muamele edilen farelerde glikoliz bloklayıcıları lezyon alanlarını küçülttü, kanserli nokta sayısını azalttı ve belirgin karaciğer veya böbrek hasarına yol açmadı; bu da bu eksenin hedeflenmesinin hem etkili hem de tolere edilebilir olabileceğini düşündürüyor.
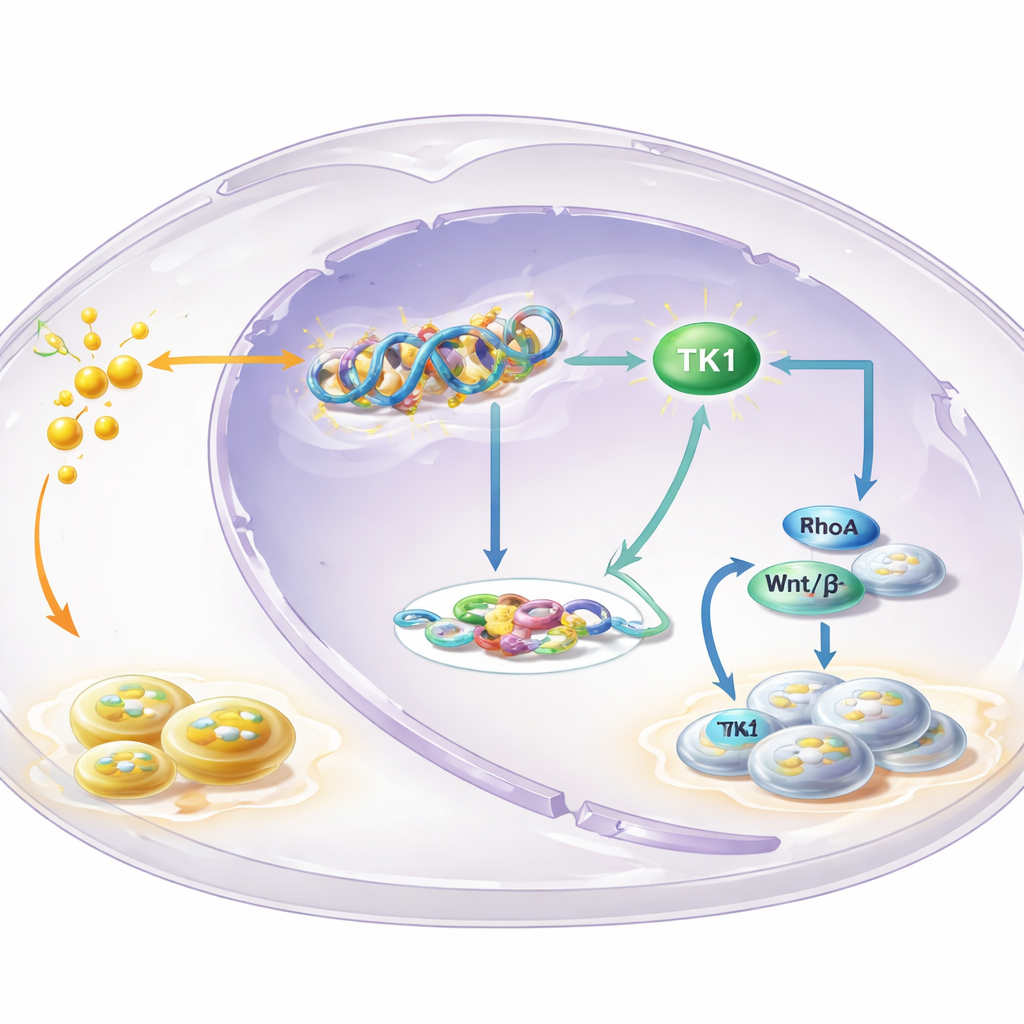
Döngünün merkezindeki ana enzim
EKip H3K18 laktilasyonunun hangi genleri kontrol ettiğini belirlemek için bu işaretin genom üzerinde nerede bulunduğunu haritaladı ve bunu gen ifadesi verileriyle birleştirdi. Öne çıkanlardan biri, DNA yapı taşlarını oluşturmaya yardımcı olan bir enzim olan timidin kinaz 1 (TK1) idi. H3K18 laktilasyonunun TK1 geninin kontrol bölgesinde zenginleştiğini ve glikolizin engellenmesinin özellikle dTTP adlı DNA öncülünün havuzu dahil olmak üzere TK1 aktivitesini azalttığını buldular. TK1 lökoplaki ve OSCC’de normal dokuya göre daha fazla bulunuyordu ve tümörlerinde daha yüksek TK1 düzeyleri olan hastaların sağkalımının genellikle daha kötü olduğu görüldü. Deneysel olarak TK1’i düşürmek hücre büyümesini yavaşlattı, hücre döngüsünde erken bir fazda duraklamaya yol açtı ve farelerde tümörleri küçülttü; bu da TK1’i seyirci değil, sürükleyici bir faktör olarak işaretliyor.
TK1 nasıl sinyalizasyonu zorlar ve metabolizmaya geri besleme yapar
Hikâye DNA yapı taşlarıyla bitmiyor. TK1 aktivitesinin ürünleri, küçük GTPazlar olarak bilinen anahtarları kontrol eden GTP ile GDP arasındaki dengeyi değiştiriyor. Çalışma, hücre şekli, hareketi ve büyümesini etkilediği bilinen RhoA adlı bu anahtarlardan birine odaklandı. Glikoliz bloklandığında GTP/GDP oranı düştü ve RhoA aktivitesi azaldı—ancak her ikisi de hücrelere daha fazla TK1 yaptırılınca geri geldi. Bu da Wnt/β‑katenin yolunu güçlendirdi; bu yol güçlü bir büyümeyi teşvik eden sinyal hattıdır. Aktif β‑katenin c‑Myc ve glikolitik enzim LDHA üretimini artırdı, bu da laktat seviyelerini daha da yükseltiyor. Daha fazla laktat ise daha fazla histon laktilasyonu ve TK1 aktivasyonu sağlıyor; böylece hücreleri kontrolsüz büyümeye iten kendi kendini güçlendiren bir döngü kapanıyor.
Farklı ağız kanserlerinde farklı yollar
Araştırmacılar ayrıca HPV negatif ve HPV pozitif ağız kanseri hücrelerini karşılaştırdı. Glikoliz ve laktilasyonun bloke edilmesi HPV negatif hücreleri güçlü şekilde yavaşlatırken, HPV pozitif hücreler bu yola daha az bağımlıydı; muhtemelen viral onkoproteinler alternatif büyüme sinyalleri sağladığı için. Hasta örneklerinde H3K18 laktilasyon işareti, sıklıkla OSCC’de mutasyona uğrayan ve normalde glikoliz ile DNA replikasyonunu sınırlayan tümör baskılayıcı protein p53’ün anormal desenleriyle korelasyon gösterdi. Bu, p53 kaybı ve laktat kaynaklı döngünün erken tümör gelişimini hızlandırmak için işbirliği yapabileceğini öne sürüyor.
Gelecek tedaviler için anlamı
Genel olarak çalışma, erken ağız lezyonlarında aşırı şeker yakımının laktat ürettiğini; laktatın sadece atık olmayıp histonları «süslediğini», TK1’i açtığını, DNA yapı taşlarını ve büyüme sinyallerini artırdığını ve daha fazla laktat üreten Wnt destekli bir döngüyü aktive ettiğini gösteriyor. Bu glikoliz–laktilasyon–TK1–β‑katenin geri besleme döngüsünü glikoliz, histon laktilasyonu, TK1, RhoA veya Wnt sinyalizasyonu gibi kilit adımların herhangi birinde kırmak, lökoplakinin kansere dönüşmesini önlemenin veya yerleşik OSCC’yi tedavi etmenin yeni yollarını sunabilir; özellikle HPV negatif hastalarda.
Atıf: Wang, Y., Geng, Y., Chen, Y. et al. Histone lactylation-driven feedback loop modulates pyrimidine metabolism to promote oral carcinogenesis. Cell Death Dis 17, 316 (2026). https://doi.org/10.1038/s41419-026-08580-w
Anahtar kelimeler: ağız kanseri, tümör metabolizması, histon laktilasyonu, pirimidin sentezi, Wnt sinyalizasyonu