Clear Sky Science · fr
La boucle de rétroaction induite par la lactylation des histones module le métabolisme des pyrimidines pour favoriser la carcinogenèse buccale
Pourquoi c’est important pour la santé buccale
Le cancer de la bouche débute souvent par une petite tache blanche et peut évoluer silencieusement vers une maladie potentiellement mortelle. Cette étude révèle comment des altérations du métabolisme du glucose dans des cellules buccales précancéreuses créent une boucle autorenforçante qui les pousse vers un cancer invasif. En retraçant cette boucle étape par étape, les chercheurs mettent au jour de nouveaux « points de pression » moléculaires qui pourraient être ciblés pour prévenir ou ralentir la croissance tumorale buccale.
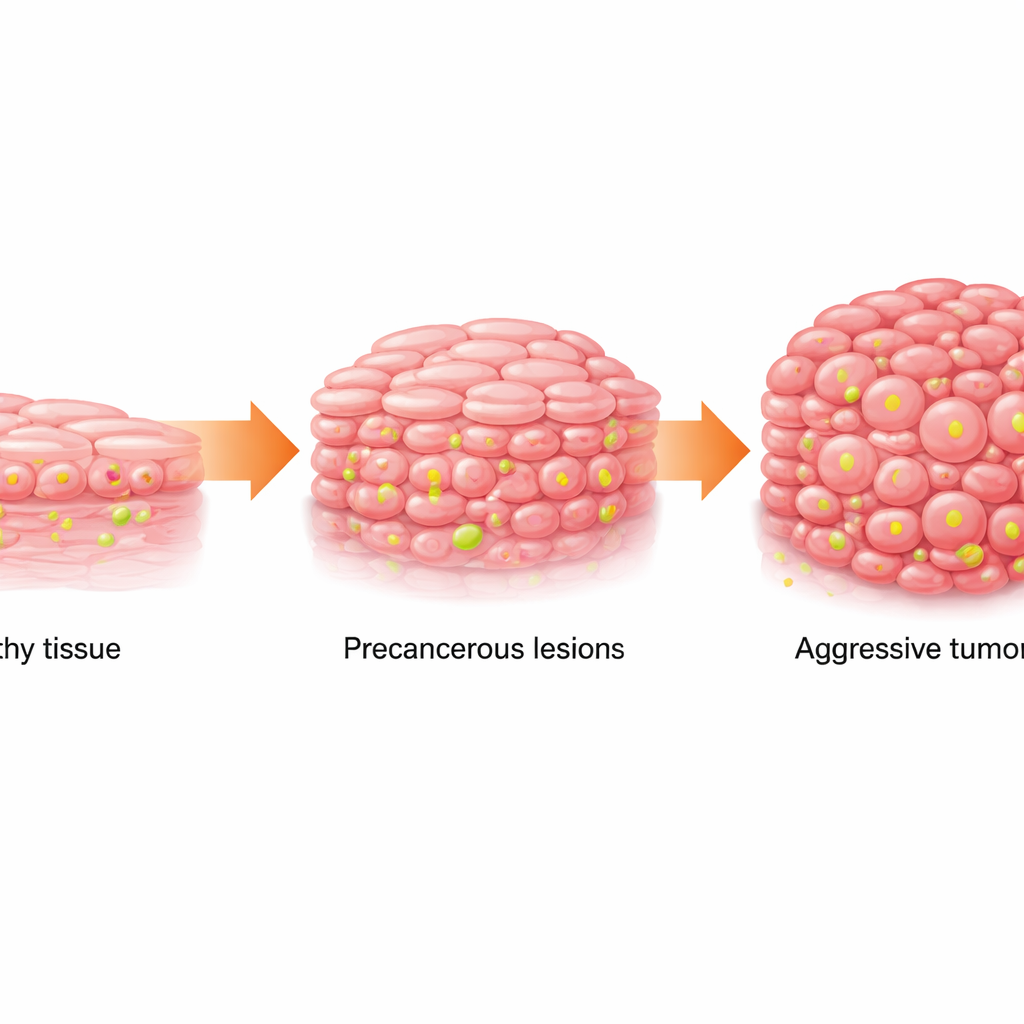
Du tissu normal aux lésions dangereuses
Le carcinome épidermoïde buccal (OSCC) est un cancer fréquent et meurtrier de la bouche. Il se développe généralement de façon progressive : les cellules de la muqueuse s’altèrent (une condition appelée leucoplasie orale, qui se présente sous forme de plaques blanches) puis évoluent vers un cancer. L’équipe a analysé des échantillons humains de tissu normal, de leucoplasie et d’OSCC, ainsi que des bases de données publiques sur le cancer et des données de séquençage unicellulaire. Ils ont constaté que, lorsque le tissu passait du normal au précancéreux puis au cancéreux, son métabolisme changeait : les cellules dépendaient davantage d’une combustion rapide du glucose (glycolyse) et accumulaient davantage de lactate, un sous‑produit métabolique. Parallèlement, une modification chimique spécifique des protéines d’emballage de l’ADN, la lactylation des histones au site nommé H3K18, devenait de plus en plus marquée.
Quand le lactate devient un interrupteur génétique
Le lactate est généralement considéré comme un déchet métabolique, mais ici il agit davantage comme un signal. Les chercheurs montrent que des niveaux élevés de lactate alimentent la lactylation des histones, qui modifie l’activation ou la répression des gènes. Dans des cultures cellulaires et un modèle murin de cancer de la langue, bloquer la glycolyse ou réduire le lactate diminuait la lactylation globale des histones et, en particulier, la marque H3K18. Cela atténuait la prolifération cellulaire, la formation de colonies et la capacité des cellules à migrer et envahir — des caractéristiques essentielles du cancer. Chez des souris exposées à un agent chimique induisant des tumeurs de la langue, un traitement par des inhibiteurs de la glycolyse réduisait la surface des lésions et le nombre de foyers cancéreux sans provoquer de dommages hépatiques ou rénaux évidents, suggérant que cibler cet axe pourrait être à la fois efficace et tolérable.
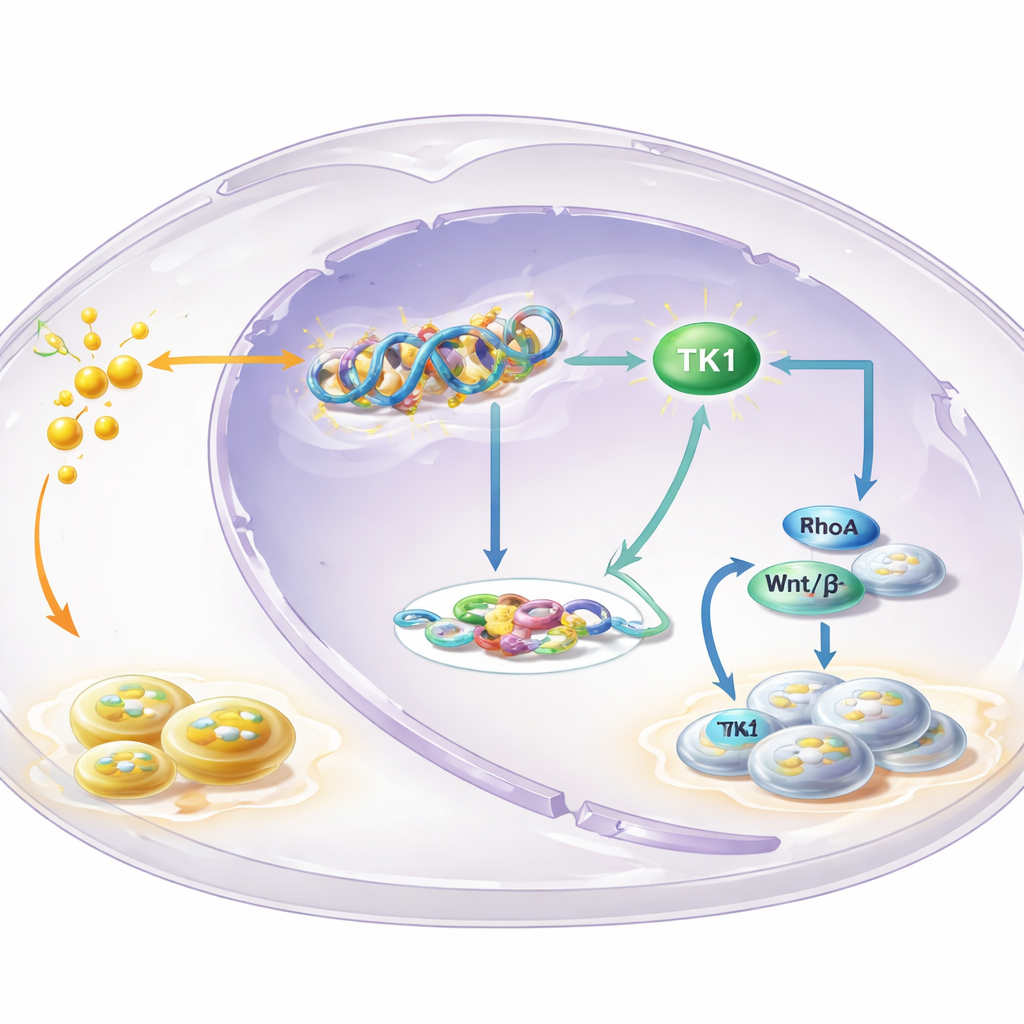
Une enzyme clé au cœur de la boucle
Pour identifier les gènes contrôlés par la lactylation en H3K18, l’équipe a cartographié la localisation de cette marque sur le génome et l’a croisée avec des données d’expression génique. Un gène a émergé : la thymidine kinase 1 (TK1), une enzyme qui participe à la synthèse des constituants de l’ADN. Ils ont trouvé que la lactylation en H3K18 était enrichie dans la région régulatrice du gène TK1 et que bloquer la glycolyse réduisait l’activité de TK1 et le pool de précurseurs d’ADN dans les cellules, en particulier le dTTP. TK1 était plus abondante dans la leucoplasie et l’OSCC que dans le tissu normal, et les patients dont les tumeurs présentaient des niveaux élevés de TK1 avaient tendance à avoir une survie plus faible. Réduire expérimentalement TK1 ralentissait la croissance cellulaire, provoquait un arrêt précoce du cycle cellulaire et réduisait la taille des tumeurs chez la souris, désignant TK1 comme un moteur plutôt qu’un simple témoin.
Comment TK1 stimule la signalisation et rétroagit sur le métabolisme
L’histoire ne s’arrête pas aux précurseurs d’ADN. Les produits de l’activité de TK1 modifient l’équilibre entre deux molécules apparentées, le GTP et le GDP, qui contrôlent des commutateurs appelés petites GTPases. L’étude s’est focalisée sur l’un de ces commutateurs, RhoA, connu pour influencer la forme, la migration et la croissance cellulaire. Lorsque la glycolyse était bloquée, le ratio GTP/GDP chutait et l’activité de RhoA diminuait — mais les deux étaient restaurés en forçant l’expression de TK1. Cela stimulait à son tour la voie Wnt/β‑caténine, une voie de signalisation puissante promotrice de croissance. La β‑caténine active augmentait la production de c‑Myc et de l’enzyme glycolytique LDHA, ce qui élève encore les niveaux de lactate. Plus de lactate alimente alors davantage la lactylation des histones et l’activation de TK1, fermant une boucle autorenforçante qui pousse continuellement les cellules vers une croissance incontrôlée.
Des chemins différents selon les cancers buccaux
Les chercheurs ont également comparé des cellules de cancers buccaux HPV‑négatifs et HPV‑positifs. Bloquer la glycolyse et la lactylation ralentissait fortement les cellules HPV‑négatives, tandis que les cellules HPV‑positives dépendaient moins de cette voie, probablement parce que des protéines virales oncogéniques fournissent des signaux de croissance alternatifs. Dans des échantillons de patients, la marque de lactylation H3K18 corrélait avec des profils anormaux de la protéine suppresseur de tumeur p53, souvent mutée dans l’OSCC et qui, normalement, freine la glycolyse et la réplication de l’ADN. Cela suggère que la perte de p53 et la boucle pilotée par le lactate peuvent coopérer pour accélérer le développement tumoral précoce.
Ce que cela implique pour les traitements futurs
Dans l’ensemble, l’étude montre que, dans les lésions buccales précoces, une glycolyse excessive produit du lactate qui ne reste pas un déchet : il marque les histones, active TK1, stimule la synthèse d’ADN et les signaux de croissance, et déclenche une boucle Wnt qui alimente encore davantage la production de lactate. Rompre cette boucle de rétroaction glycolyse–lactylation–TK1–β‑caténine à n’importe laquelle de ses étapes clés — glycolyse, lactylation des histones, TK1, RhoA ou signalisation Wnt — pourrait offrir de nouvelles stratégies pour empêcher la leucoplasie de devenir cancéreuse ou pour traiter un OSCC établi, en particulier chez les patients HPV‑négatifs.
Citation: Wang, Y., Geng, Y., Chen, Y. et al. Histone lactylation-driven feedback loop modulates pyrimidine metabolism to promote oral carcinogenesis. Cell Death Dis 17, 316 (2026). https://doi.org/10.1038/s41419-026-08580-w
Mots-clés: cancer buccal, métabolisme tumoral, lactylation des histones, synthèse des pyrimidines, signalisation Wnt