Clear Sky Science · sv
Histonlaktyliering‑driven återkopplingsslinga reglerar pyrimidinmetabolism för att främja munhålecancer
Varför detta är viktigt för munhälsan
Muncancer börjar ofta som en liten vit fläck i munnen och kan tyst utvecklas till en livshotande sjukdom. Denna studie avslöjar hur förändringar i hur för‑cancerösa celler i munnen förbränner socker skapar en självförstärkande slinga som driver dem mot fullt utvecklad cancer. Genom att följa denna slinga steg för steg visar forskarna nya molekylära ”tryckpunkter” som skulle kunna riktas mot för att förebygga eller bromsa tumörer i munnen.
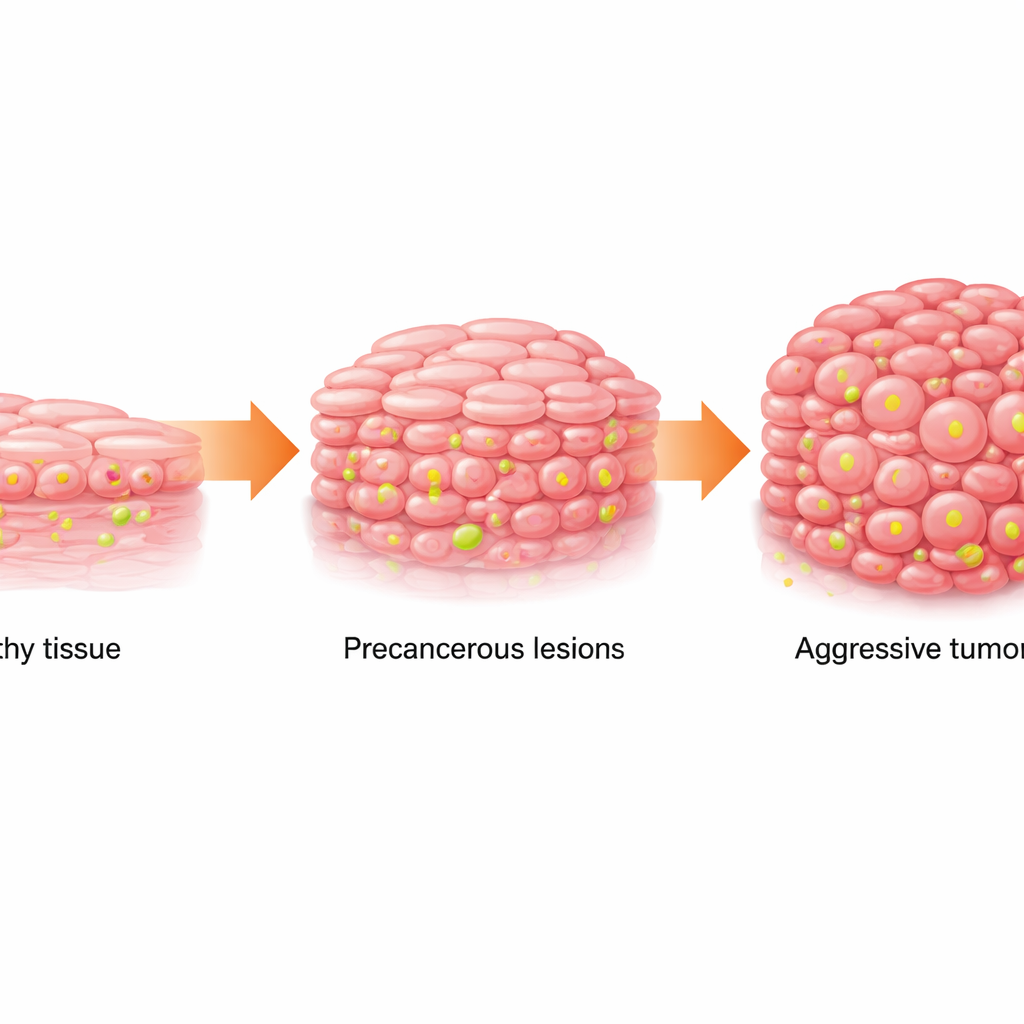
Från normal vävnad till farliga fläckar
Oral skivepitelcancer (OSCC) är en vanlig och dödlig cancer i munnen. Den utvecklas vanligtvis gradvis: friska slemhinneceller blir onormala (en tillstånd som kallas oral leukoplaki, som syns som vita fläckar) och går sedan vidare till cancer. Teamet granskade mänskliga prover från normal vävnad, leukoplaki och OSCC, samt data från offentliga cancerregister och single‑cell‑sekvensering. De fann att när vävnaden gick från normal till för‑cancerös till cancerös ändrades dess metabolism: cellerna förlitade sig mer på snabb sockerförbränning (glykolys) och samlade på sig högre nivåer av laktat, en metabolisk biprodukt. Samtidigt blev en specifik kemisk märkning på DNA‑packande proteiner, kallad histonlaktyliering vid platsen H3K18, successivt starkare.
När laktat blir en genetisk brytare
Laktat betraktas oftast som metaboliskt avfall, men här fungerar det mer som en signal. Forskarna visade att höga laktatnivåer driver på histonlaktyliering, vilket ändrar hur gener slås på eller av. Både i cellkulturer och i en musmodell för tungcancer ledde blockering av glykolys eller sänkta laktatnivåer till minskad total histonlaktyliering och särskilt H3K18‑märket. Detta dämpade celltillväxt, kolonibildning och cellernas förmåga att röra sig och invadera — nyckelfunktioner för cancer. Hos möss exponerade för ett kemiskt ämne som framkallar tungtumörer minskade behandling med glykolyshämmare lesionernas yta, antalet cancerösa fläckar och gav inga uppenbara lever‑ eller njurskador, vilket tyder på att riktning mot denna axel kan vara både effektivt och tolererbart.
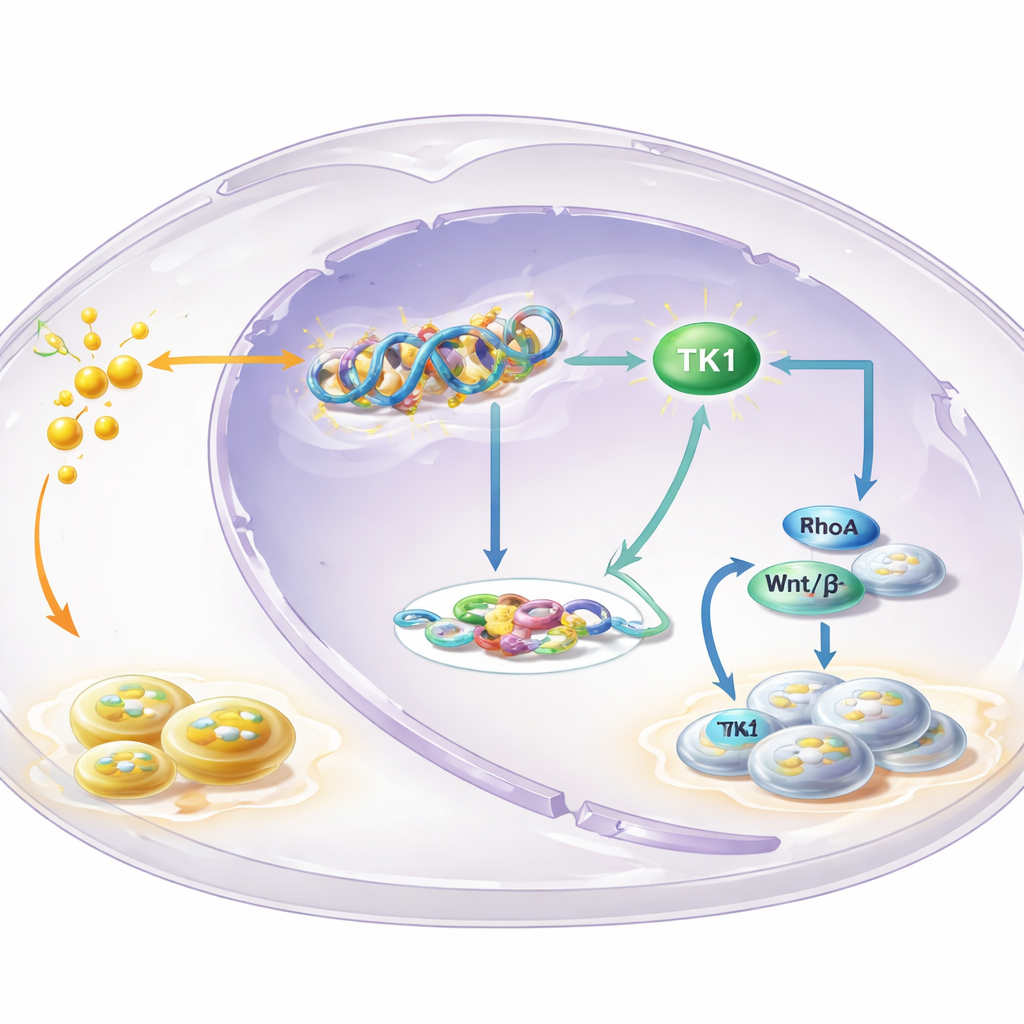
Ett nyckelenzym i slingan
För att identifiera vilka gener som styrs av H3K18‑laktyliering kartlade teamet var detta märke sitter i genomet och kombinerade det med genuttrycksdata. En framträdande gen var tymidinkinase 1 (TK1), ett enzym som hjälper till att bygga DNA:s byggstenar. De fann att H3K18‑laktyliering var rikligt förekommande vid TK1‑genens regleringsregion och att blockering av glykolys minskade TK1‑aktiviteten och poolen av DNA‑prekursorer i cellerna, särskilt dTTP. TK1 var mer förekommande i leukoplaki och OSCC än i normal vävnad, och patienter vars tumörer hade högre TK1‑nivåer tenderade att ha sämre överlevnad. Experimentellt sänkt TK1 bromsade celltillväxt, tvingade cellerna att stanna i ett tidigt cellcykelskede och krympte tumörer hos möss, vilket markerar TK1 som en drivande faktor snarare än en åskådare.
Hur TK1 driver signalering och återkopplar på metabolismen
Berättelsen slutar inte vid DNA‑byggstenarna. Produkterna av TK1:s aktivitet förändrar balansen mellan två besläktade molekyler, GTP och GDP, som styr omkopplare kända som små GTPaser. Studien fokuserade på en sådan omkopplare, RhoA, känd för att påverka cellform, rörelse och tillväxt. När glykolys blockerades föll GTP/GDP‑kvoten och RhoA‑aktiviteten minskade — men båda återställdes genom att tvångsöka cellerna att producera mer TK1. Detta förstärkte i sin tur Wnt/β‑catenin‑vägen, en kraftfull tillväxtfrämjande signalväg. Aktiv β‑catenin ökade produktionen av c‑Myc och det glykolytiska enzymet LDHA, vilket ytterligare höjer laktatnivåerna. Mer laktat driver då vidare histonlaktyliering och TK1‑aktivering, och sluter en självförstärkande slinga som kontinuerligt pressar cellerna mot okontrollerad tillväxt.
Olika vägar i olika muncancerformer
Forskarna jämförde också HPV‑negativa och HPV‑positiva muncancerceller. Medan blockering av glykolys och laktyliering kraftigt bromsade HPV‑negativa celler var HPV‑positiva celler mindre beroende av denna väg, sannolikt eftersom virala onkoproteiner ger alternativa tillväxtsignaler. I patientprover korrelerade H3K18‑laktylieringsmärket med onormala mönster av tumörsuppressorn p53, som ofta är muterad i OSCC och normalt håller tillbaka glykolys och DNA‑replikation. Detta tyder på att förlust av p53 och den laktatdrivna slingan kan samspela för att påskynda tidig tumörutveckling.
Vad detta betyder för framtida behandlingar
Sammanfattningsvis visar studien att i tidiga munlesioner ger överdriven sockerförbränning upphov till laktat, som inte bara blir avfall utan dekorerar histoner, aktiverar TK1, ökar DNA‑byggandet och tillväxtsignaler samt initierar en Wnt‑driven cykel som i sin tur genererar ännu mer laktat. Att bryta denna glykolys–laktyliering–TK1–β‑catenin‑återkoppling vid någon av dess nyckelsteg — såsom glykolys, histonlaktyliering, TK1, RhoA eller Wnt‑signalering — kan erbjuda nya sätt att förhindra att leukoplaki blir cancer eller att behandla etablerad OSCC, särskilt hos HPV‑negativa patienter.
Citering: Wang, Y., Geng, Y., Chen, Y. et al. Histone lactylation-driven feedback loop modulates pyrimidine metabolism to promote oral carcinogenesis. Cell Death Dis 17, 316 (2026). https://doi.org/10.1038/s41419-026-08580-w
Nyckelord: muncancer, tumörmetabolism, histonlaktyliering, pyrimidinsyntes, Wnt‑signalering