Clear Sky Science · ru
Обратная связь, управляемая лактиляцией гистонов, модулирует пиримидиновый метаболизм и способствует канцерогенезу полости рта
Почему это важно для здоровья рта
Рак полости рта часто начинается с небольшого белого пятна во рту и может незаметно прогрессировать в опасное для жизни заболевание. В этом исследовании показано, как изменения в том, как предраковые клетки ротовой полости перерабатывают сахар, создают самоподдерживающуюся петлю, подталкивающую их к развитию полноценного рака. Проследив эту петлю шаг за шагом, авторы выявляют новые молекулярные «точки давления», на которые можно воздействовать, чтобы предупредить или замедлить развитие опухолей полости рта.
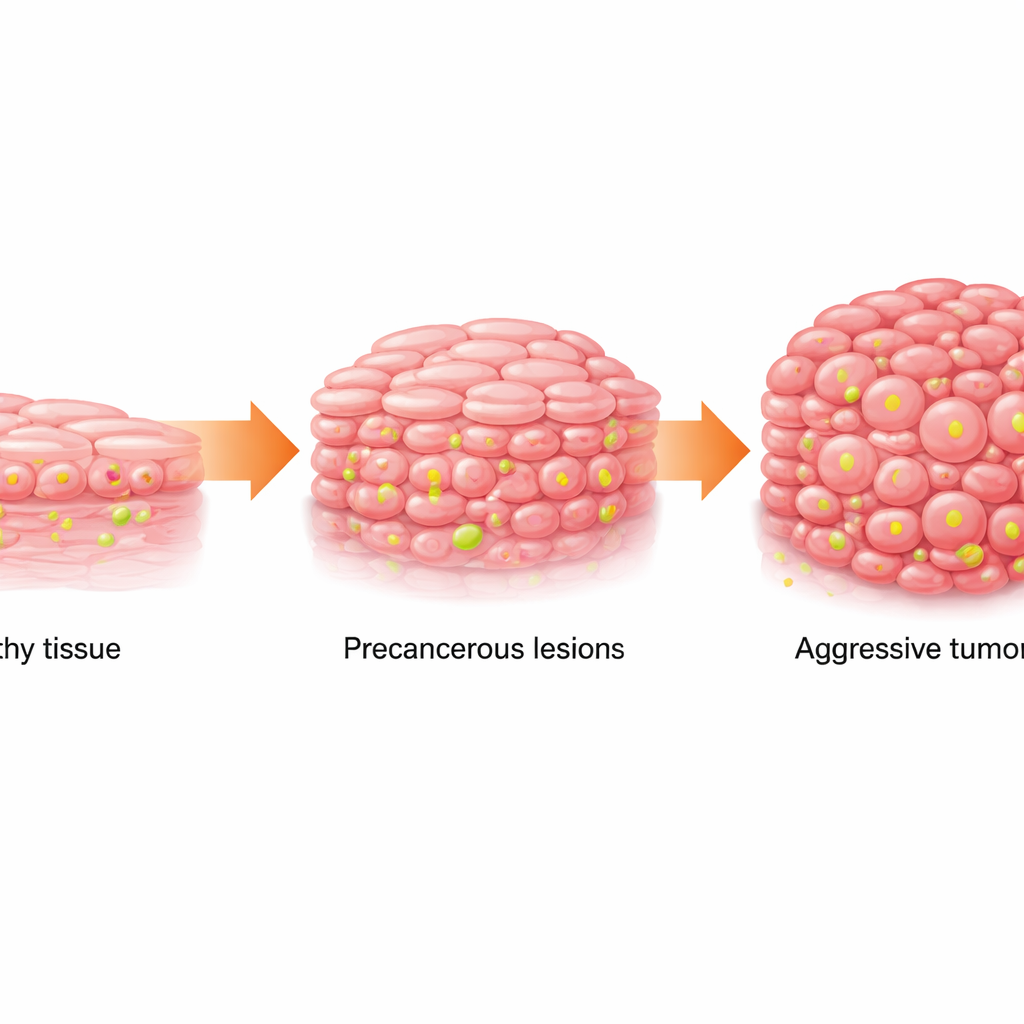
От нормальной ткани до опасных пятен
Плоскоклеточный рак полости рта (OSCC) — распространённый и смертоносный рак ротовой полости. Как правило, он развивается постепенно: клетки здорового эпителия становятся аномальными (состояние, называемое оральным лейкоплакией, проявляющееся в виде белых пятен), а затем прогрессируют в рак. Команда изучала образцы человека из нормальной ткани, лейкоплакии и OSCC, а также данные из общедоступных онкологических баз и одно‑клеточного секвенирования. Они обнаружили, что по мере перехода ткани от нормальной к предраковой и раковой меняется её метаболизм: клетки всё сильнее зависят от быстрого сжигания сахара (гликолиза) и накапливают повышенные уровни лактата — метаболического побочного продукта. Одновременно специфическая химическая метка на упаковывающих ДНК белках — лактиляция гистонов в положении H3K18 — становилась постепенно сильнее.
Когда лактат превращается в генетический переключатель
Лактат обычно считают метаболическим отбросом, но здесь он действует скорее как сигнал. Исследователи показали, что высокие уровни лактата способствуют лактиляции гистонов, что изменяет включение или выключение генов. В культурах клеток и в мышиной модели рака языка блокирование гликолиза или снижение лактата уменьшали общую лактиляцию гистонов и, в частности, метку H3K18. Это ослабляло рост клеток, колониеобразование и способность клеток мигрировать и внедряться — ключевые характеристики рака. У мышей, подвергнутых воздействию химического вещества, индуцирующего опухоли языка, лечение блокаторами гликолиза уменьшало площадь поражений, снижало число канцерозных очагов и не вызывало заметных повреждений печени или почек, что говорит о том, что воздействие на эту ось может быть эффективно и переносимо.
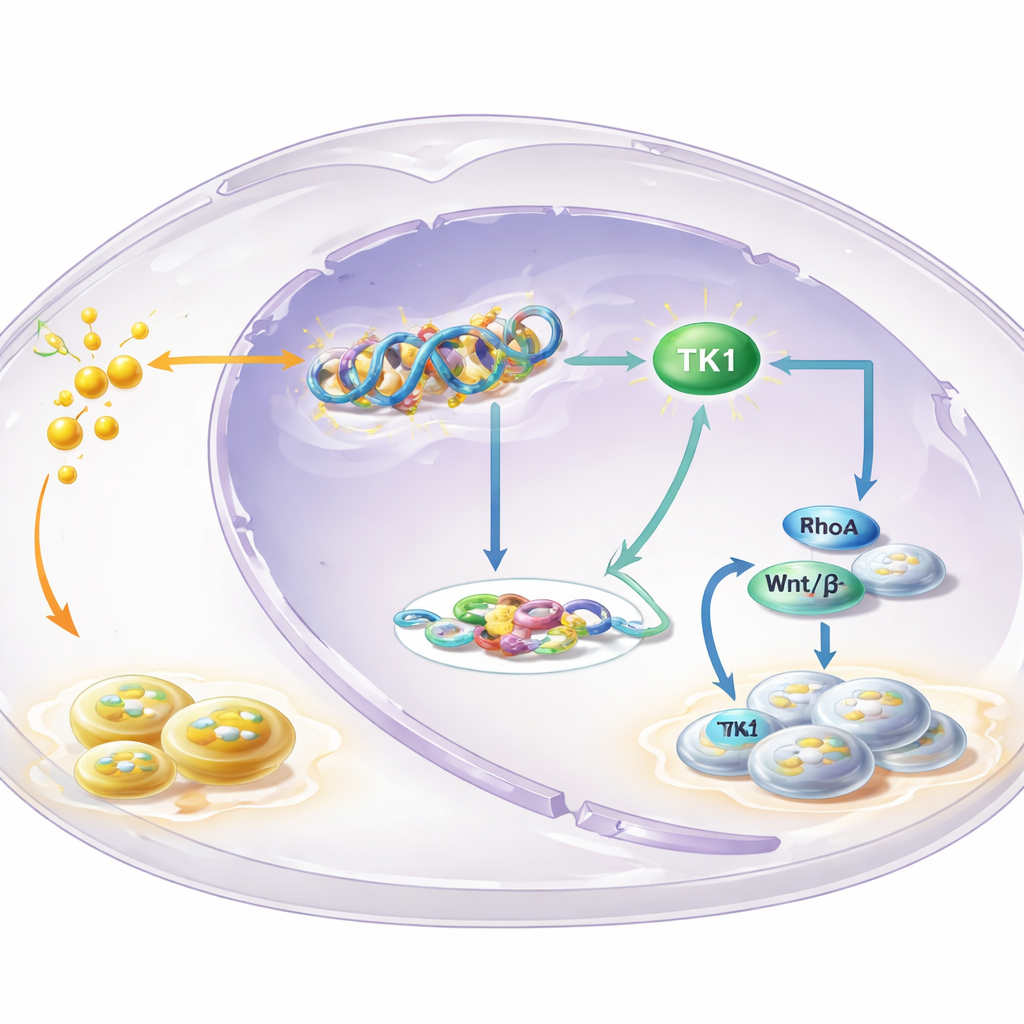
Ключевой фермент в центре петли
Чтобы выяснить, какие гены контролируются лактиляцией H3K18, команда нанесла распределение этой метки на геном и сопоставила его с данными экспрессии генов. Выделился тимидинкиназа 1 (TK1) — фермент, участвующий в синтезе строительных блоков ДНК. Авторы обнаружили, что лактиляция H3K18 обогащена в регуляторной области гена TK1 и что блокирование гликолиза снижает активность TK1 и запасы предшественников ДНК в клетках, особенно dTTP. TK1 был более представлен в лейкоплакии и OSCC по сравнению с нормальной тканью, а пациенты с опухолями, в которых был повышен уровень TK1, как правило, имели худший прогноз. Экспериментальное снижение TK1 замедляло рост клеток, вызывало их остановку на ранней стадии клеточного цикла и уменьшало размер опухолей у мышей, что указывает на роль TK1 как драйвера, а не просто сопутствующего явления.
Как TK1 усиливает сигналы и влияет на метаболизм в обратную сторону
История не ограничивается только строительными блоками ДНК. Продукты активности TK1 меняют соотношение между двумя связанными молекулами — GTP и GDP, которые управляют переключателями, известными как малые GTPазы. Исследование сосредоточилось на одной такой молекуле, RhoA, известной тем, что влияет на форму клетки, её движение и рост. Когда гликолиз блокировали, отношение GTP/GDP падало и активность RhoA снижалась — но оба показателя восстанавливались при принудительном повышении синтеза TK1. Это, в свою очередь, усиливало путь Wnt/β‑catenin, мощную сигнализацию, стимулирующую рост. Активная β‑катенин увеличивала продукцию c‑Myc и гликолитического фермента LDHA, что ещё больше повышало уровень лактата. Больше лактата питало дополнительную лактиляцию гистонов и активацию TK1, замыкая самоподдерживающуюся петлю, которая непрерывно подталкивает клетки к неконтролируемому росту.
Различные пути в разных формах рака полости рта
Авторы также сравнили HPV‑отрицательные и HPV‑положительные клетки рака полости рта. В то время как блокирование гликолиза и лактиляции сильно замедляло HPV‑отрицательные клетки, HPV‑положительные клетки были в меньшей степени зависимы от этого пути, вероятно потому, что вирусные онкогенные белки обеспечивают альтернативные ростовые сигналы. В образцах пациентов метка лактиляции H3K18 коррелировала с аномальными паттернами опухолевого супрессора p53, который часто мутирует при OSCC и который в норме сдерживает гликолиз и репликацию ДНК. Это позволяет предположить, что утрата функции p53 и лактат‑опосредованная петля могут сотрудничать, ускоряя раннее развитие опухоли.
Что это значит для будущих терапий
В целом исследование показывает, что в ранних поражениях полости рта избыточное сжигание сахара производит лактат, который не остаётся просто отходом — он модифицирует гистоны, включает TK1, усиливает синтез ДНК и ростовые сигналы и активирует Wnt‑опосредованную цепь, что возвращается и генерирует ещё больше лактата. Разрыв этой петли «гликолиз–лактиляция–TK1–β‑катенин» на любом из ключевых этапов — например, гликолизе, лактиляции гистонов, TK1, RhoA или Wnt‑сигнализации — может дать новые способы предотвратить превращение лейкоплакии в рак или лечить уже установленный OSCC, особенно у пациентов с HPV‑отрицательными опухолями.
Цитирование: Wang, Y., Geng, Y., Chen, Y. et al. Histone lactylation-driven feedback loop modulates pyrimidine metabolism to promote oral carcinogenesis. Cell Death Dis 17, 316 (2026). https://doi.org/10.1038/s41419-026-08580-w
Ключевые слова: рак полости рта, метаболизм опухоли, лактиляция гистонов, синтез пиримидина, Wnt-сигнализация