Clear Sky Science · es
El bucle de retroalimentación impulsado por lactilación de histonas modula el metabolismo de las pirimidinas para promover la carcinogénesis oral
Por qué importa para la salud bucal
El cáncer oral a menudo comienza como una pequeña mancha blanca en la boca y puede progresar silenciosamente hasta convertirse en una enfermedad potencialmente mortal. Este estudio revela cómo los cambios en la forma en que las células precancerosas bucales metabolizan el azúcar crean un bucle autorreforzante que las impulsa hacia el cáncer franco. Al seguir este bucle paso a paso, los investigadores identifican nuevos puntos moleculares "críticos" que podrían ser diana para prevenir o frenar los tumores orales.
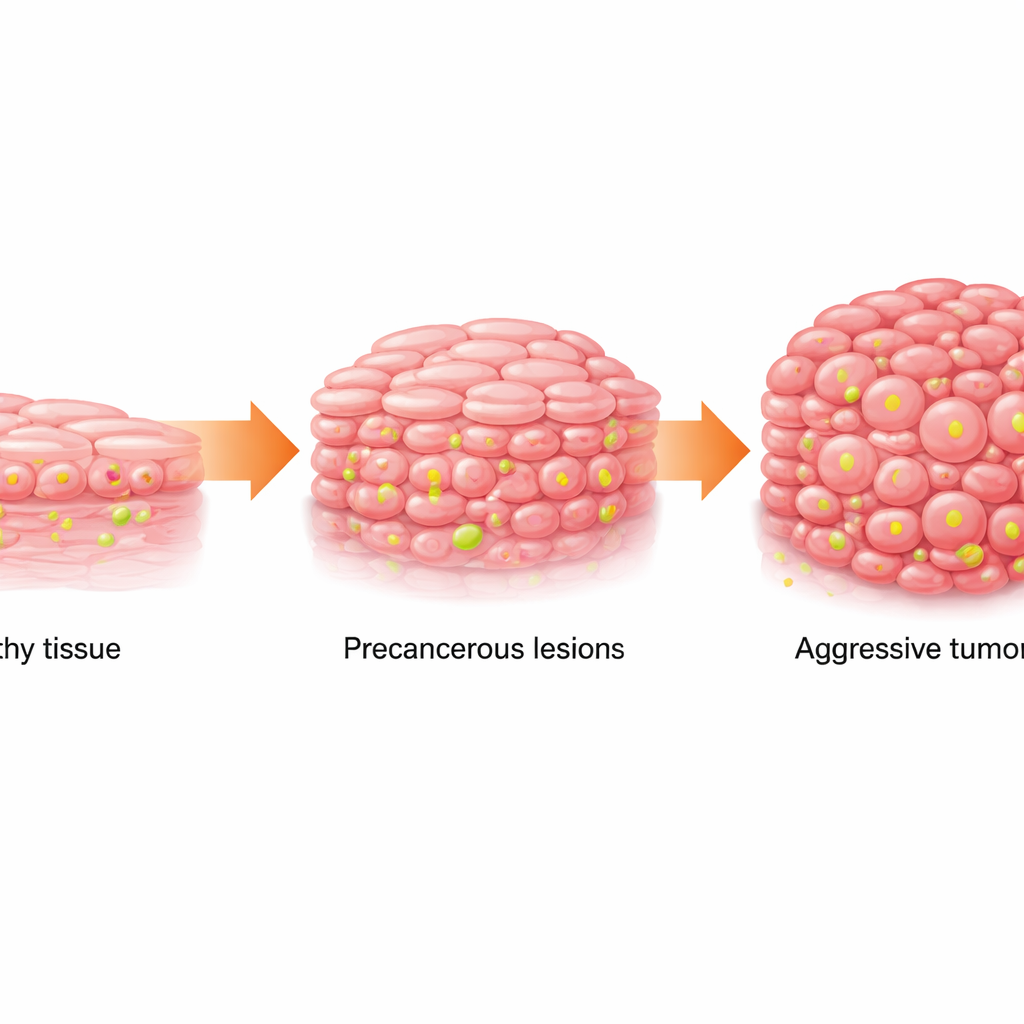
De tejido normal a manchas peligrosas
El carcinoma epidermoide oral (OSCC) es un cáncer de la boca frecuente y letal. Suele desarrollarse de forma gradual: las células del revestimiento sano se vuelven anormales (una condición llamada leucoplasia oral, que aparece como parches blancos) y luego progresan a cáncer. El equipo examinó muestras humanas de tejido normal, leucoplasia y OSCC, así como datos de bases públicas de cáncer y secuenciación unicelular. Encontraron que, a medida que el tejido avanzaba de normal a precanceroso y canceroso, su metabolismo cambiaba: las células dependían más de la combustión rápida de azúcar (glucólisis) y acumulaban niveles más altos de lactato, un subproducto metabólico. Al mismo tiempo, una marca química específica en las proteínas que empaquetan el ADN, llamada lactilación de histonas en el sitio H3K18, se intensificó progresivamente.
Cuando el lactato se convierte en un interruptor genético
El lactato suele considerarse un desecho metabólico, pero aquí actúa más bien como una señal. Los investigadores mostraron que los niveles elevados de lactato alimentan la lactilación de histonas, que cambia cómo se activan o desactivan los genes. Tanto en cultivos celulares como en un modelo de ratón de cáncer de lengua, bloquear la glucólisis o reducir el lactato disminuyó la lactilación histona global y, en particular, la marca H3K18. Esto atenuó el crecimiento celular, la formación de colonias y la capacidad de las células para moverse e invadir, rasgos clave del cáncer. En ratones expuestos a un químico que induce tumores de lengua, el tratamiento con inhibidores de la glucólisis redujo el área de las lesiones, disminuyó el número de focos cancerosos y no causó daños evidentes en hígado o riñón, lo que sugiere que dirigirse a este eje podría ser eficaz y tolerable.
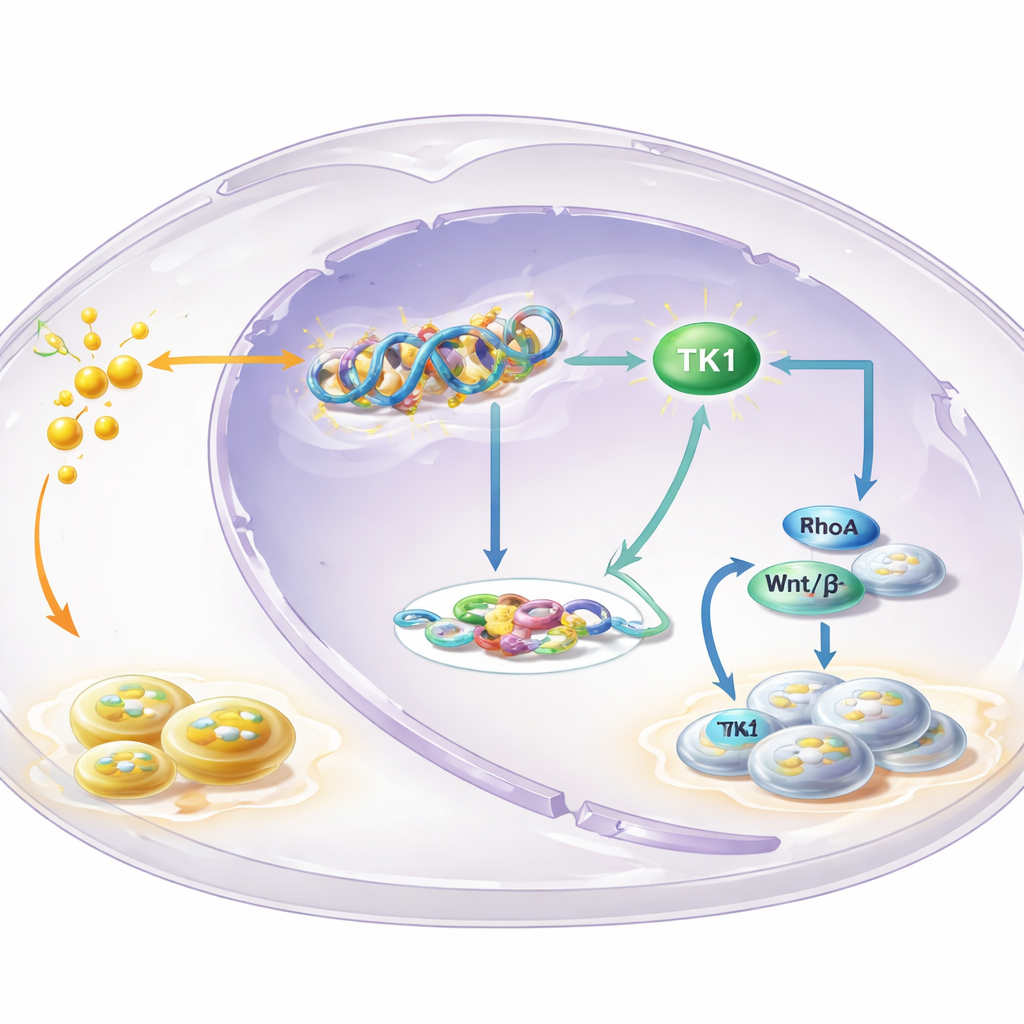
Una enzima clave en el centro del bucle
Para identificar qué genes están controlados por la lactilación en H3K18, el equipo cartografió dónde se localiza esta marca en el genoma y lo combinó con datos de expresión génica. Uno destacado fue la timidina quinasa 1 (TK1), una enzima que ayuda a fabricar los bloques constructores del ADN. Encontraron que la lactilación en H3K18 estaba enriquecida en la región reguladora del gen TK1 y que bloquear la glucólisis reducía la actividad de TK1 y el reservorio de precursores de ADN en las células, especialmente uno llamado dTTP. TK1 era más abundante en leucoplasia y OSCC que en tejido normal, y los pacientes cuyos tumores mostraban niveles más altos de TK1 tendían a tener peor supervivencia. Reducir experimentalmente TK1 ralentizó el crecimiento celular, provocó una detención en una fase temprana del ciclo celular y disminuyó el tamaño de los tumores en ratones, señalando a TK1 como un impulsor y no un mero espectador.
Cómo TK1 impulsa la señalización y retroalimenta el metabolismo
La historia no se detiene en los bloques de ADN. Los productos de la actividad de TK1 alteran el equilibrio entre dos moléculas relacionadas, GTP y GDP, que controlan interruptores conocidos como pequeñas GTPasas. El estudio se centró en uno de estos interruptores, RhoA, conocido por influir en la forma, el movimiento y el crecimiento celular. Cuando se bloqueó la glucólisis, la proporción GTP/GDP disminuyó y la actividad de RhoA cayó, pero ambos se restauraron al forzar a las células a producir más TK1. Esto, a su vez, potenció la vía Wnt/β‑catenina, una potente ruta de señalización promotora del crecimiento. La β‑catenina activa aumentó la producción de c‑Myc y de la enzima glucolítica LDHA, lo que eleva aún más los niveles de lactato. Más lactato alimenta más lactilación de histonas y activación de TK1, cerrando un bucle autorreforzante que empuja continuamente a las células hacia el crecimiento descontrolado.
Diferentes trayectorias en distintos cánceres orales
Los investigadores también compararon células de cáncer oral negativas y positivas para VPH. Mientras que bloquear la glucólisis y la lactilación frenó con fuerza a las células VPH‑negativas, las células VPH‑positivas dependían menos de esta vía, probablemente porque las proteínas virales oncogénicas proporcionan señales de crecimiento alternativas. En muestras de pacientes, la marca de lactilación en H3K18 se correlacionó con patrones anómalos de la proteína supresora tumoral p53, que a menudo está mutada en OSCC y normalmente restringe la glucólisis y la replicación del ADN. Esto sugiere que la pérdida de p53 y el bucle impulsado por el lactato pueden cooperar para acelerar el desarrollo tumoral temprano.
Qué implica esto para tratamientos futuros
En conjunto, el estudio muestra que en las lesiones bucales tempranas, el exceso de combustión de azúcar produce lactato, que no se limita a ser un residuo: modifica histonas, activa TK1, potencia la síntesis de ADN y las señales de crecimiento, y activa un ciclo impulsado por Wnt que retroalimenta para generar aún más lactato. Interrumpir este bucle de retroalimentación glucólisis–lactilación–TK1–β‑catenina en cualquiera de sus pasos clave —como la glucólisis, la lactilación de histonas, TK1, RhoA o la señalización Wnt— podría ofrecer nuevas vías para evitar que la leucoplasia progrese a cáncer o para tratar OSCC establecido, especialmente en pacientes VPH‑negativos.
Cita: Wang, Y., Geng, Y., Chen, Y. et al. Histone lactylation-driven feedback loop modulates pyrimidine metabolism to promote oral carcinogenesis. Cell Death Dis 17, 316 (2026). https://doi.org/10.1038/s41419-026-08580-w
Palabras clave: cáncer oral, metabolismo tumoral, lactilación de histonas, síntesis de pirimidinas, señalización Wnt