Clear Sky Science · de
Histon‑Lactylierung getriebener Rückkopplungsmechanismus moduliert die Pyrimidin‑Verstoffwechselung und fördert die orale Karzinogenese
Warum das für die Mundgesundheit wichtig ist
Oralkrebs beginnt oft als kleiner weißer Fleck im Mund und kann sich unbemerkt zu einer lebensbedrohlichen Krankheit entwickeln. Die vorliegende Studie zeigt, wie Veränderungen in der Art und Weise, wie präkanzeröse Mundzellen Zucker verstoffwechseln, eine sich selbst verstärkende Schleife erzeugen, die sie in Richtung Vollkrebs treibt. Indem die Forschenden diese Schleife Schritt für Schritt nachzeichnen, identifizieren sie neue molekulare „Druckpunkte“, die potenziell angegriffen werden könnten, um orale Tumoren zu verhindern oder zu verlangsamen.
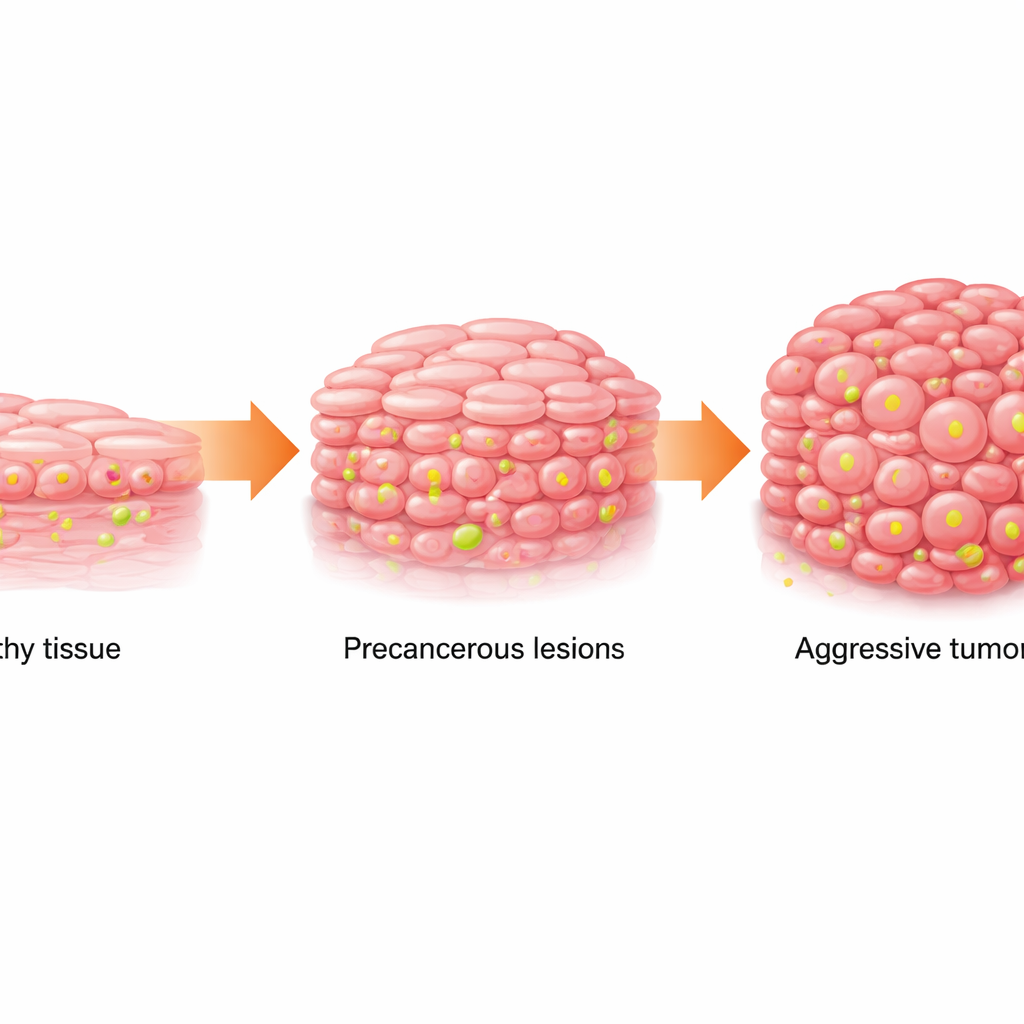
Vom normalen Gewebe zu gefährlichen Flecken
Plattenepithelkarzinom des Mundes (oral squamous cell carcinoma, OSCC) ist ein häufiger und tödlicher Mundkrebs. Es entwickelt sich meist schrittweise: gesunde Schleimhautzellen werden abnormal (ein Zustand, der als orale Leukoplakie bezeichnet wird und sich als weiße Flecken zeigt) und schreiten dann zum Krebs vor. Das Team untersuchte menschliche Proben aus normalem Gewebe, Leukoplakie und OSCC sowie Daten aus öffentlichen Krebsdatenbanken und Einzelzellsequenzierungen. Sie fanden heraus, dass sich der Stoffwechsel mit dem Übergang von normal zu präkanzerös zu krebsartig veränderte: Zellen setzten vermehrt auf schnelle Zuckerverbrennung (Glykolyse) und akkumulierten höhere Laktatwerte, ein Stoffwechselnebenprodukt. Gleichzeitig nahm eine spezifische chemische Markierung der DNA‑verpackenden Proteine, die Histon‑Lactylierung an der Stelle H3K18, progressiv zu.
Wenn Laktat zum genetischen Schalter wird
Laktat wird meist als Stoffwechselabfall angesehen, wirkt hier jedoch eher als Signalstoff. Die Forschenden zeigten, dass hohe Laktatspiegel in die Histon‑Lactylierung einfließen und so die Genaktivierung verändern. Sowohl in Zellkulturen als auch in einem Mausmodell des Zungenkrebses reduzierten das Blockieren der Glykolyse oder das Absenken von Laktat die Gesamthiston‑Lactylierung und speziell die H3K18‑Marke. Das dämpfte Zellwachstum, Koloniebildung sowie die Fähigkeit der Zellen zu wandern und zu invasieren — zentrale Merkmale von Krebs. In Mäusen, die einer chemischen Zungenkarzinogenese ausgesetzt waren, verkleinerte eine Behandlung mit Glykolysehemmern die Läsionsflächen, verringerte die Zahl krebsartiger Herde und verursachte keine offensichtlichen Leber‑ oder Nierenschäden, was darauf hindeutet, dass eine Zielsetzung dieser Achse sowohl wirksam als auch verträglich sein könnte.
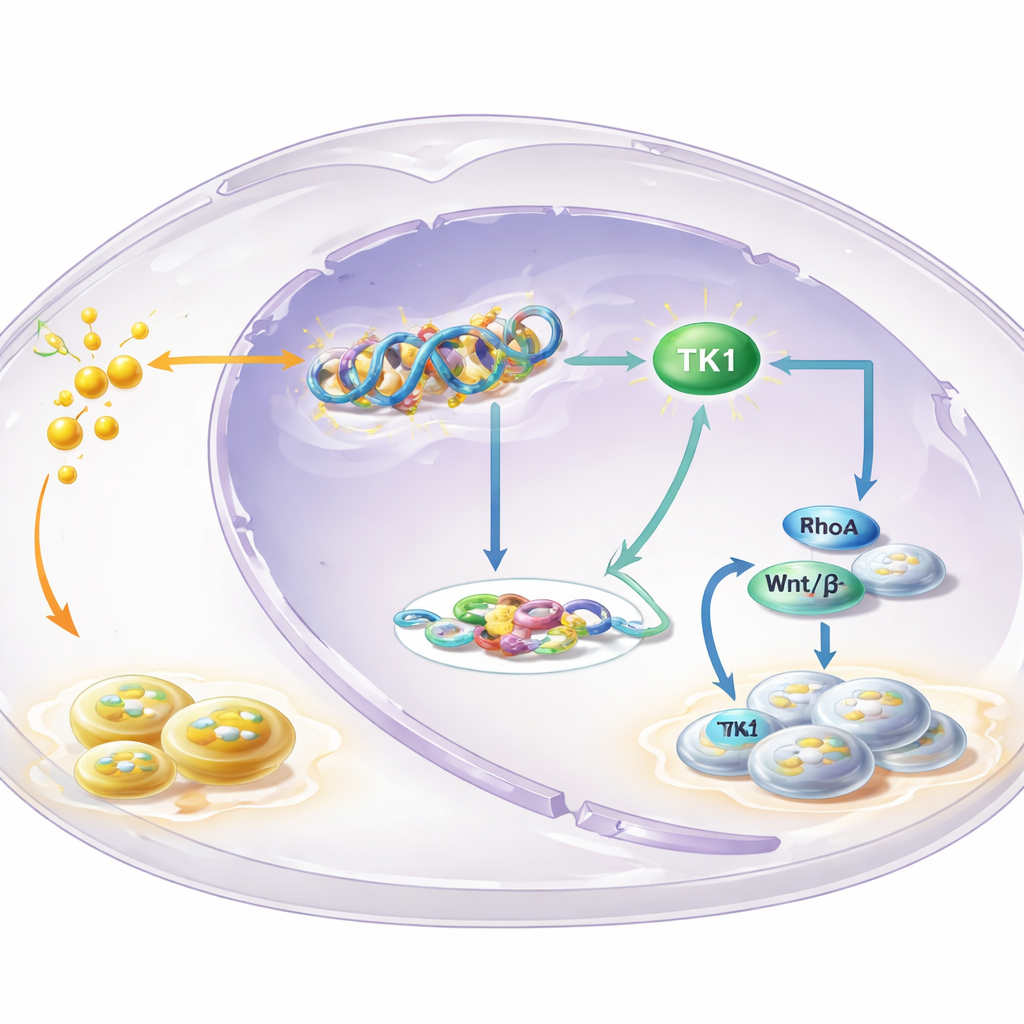
Ein Schlüsselenzym im Zentrum der Schleife
Um zu ermitteln, welche Gene durch H3K18‑Lactylierung gesteuert werden, lokalisierte das Team diese Markierung im Genom und kombinierte die Daten mit Genexpressionsprofilen. Ein hervorstechendes Gen war die Thymidinkinase 1 (TK1), ein Enzym, das beim Aufbau der DNA‑Bausteine hilft. Sie fanden heraus, dass H3K18‑Lactylierung im Kontrollbereich des TK1‑Gens angereichert war und dass das Blockieren der Glykolyse die TK1‑Aktivität und den Vorrat an DNA‑Vorstufen in Zellen verringerte, insbesondere das dTTP. TK1 war in Leukoplakien und OSCC häufiger vorhanden als in normalem Gewebe, und Patientinnen und Patienten, deren Tumoren höhere TK1‑Spiegel aufwiesen, hatten tendenziell eine schlechtere Überlebensprognose. Experimentelles Herunterregulieren von TK1 verlangsamte das Zellwachstum, ließ Zellen in einer frühen Phase des Zellzyklus verharren und verkleinerte Tumoren in Mäusen — ein Hinweis darauf, dass TK1 als Treiber und nicht als Beiwerk wirkt.
Wie TK1 Signalgebung vorantreibt und auf den Stoffwechsel zurückwirkt
Die Geschichte endet nicht bei DNA‑Bausteinen. Die Produkte der TK1‑Aktivität verändern das Gleichgewicht zwischen zwei verwandten Molekülen, GTP und GDP, die Schalter namens kleine GTPasen steuern. Die Studie konzentrierte sich auf einen solchen Schalter, RhoA, der Form, Bewegung und Wachstum von Zellen beeinflusst. Wenn die Glykolyse blockiert wurde, sank das GTP/GDP‑Verhältnis und die RhoA‑Aktivität nahm ab — beides ließ sich jedoch wiederherstellen, indem Zellen gezwungen wurden, mehr TK1 zu produzieren. Das wiederum stärkte den Wnt/β‑Catenin‑Signalweg, eine mächtige wachstumsfördernde Route. Aktives β‑Catenin erhöhte die Produktion von c‑Myc und des glycolytischen Enzyms LDHA, was wiederum die Laktatspiegel ansteigen lässt. Mehr Laktat treibt dann erneut die Histon‑Lactylierung und die TK1‑Aktivierung an und schließt so eine selbstverstärkende Schleife, die Zellen ständig in Richtung unkontrollierten Wachstums drängt.
Unterschiedliche Wege in verschiedenen oralen Krebsen
Die Forschenden verglichen außerdem HPV‑negative und HPV‑positive orale Krebszellen. Während das Blockieren von Glykolyse und Lactylierung HPV‑negative Zellen stark verlangsamte, waren HPV‑positive Zellen weniger abhängig von diesem Weg, vermutlich weil virale onkogene Proteine alternative Wachstumssignale liefern. In Patientenproben korrelierte die H3K18‑Lactylierungsmarke mit abnormalen Mustern des Tumorsuppressors p53, der in OSCC oft mutiert ist und normalerweise Glykolyse und DNA‑Replikation bremst. Das deutet darauf hin, dass der Verlust von p53 und die Laktat‑getriebene Schleife zusammenwirken könnten, um die frühe Tumorentwicklung zu beschleunigen.
Was das für künftige Behandlungen bedeutet
Insgesamt zeigt die Studie, dass in frühen Mundläsionen übermäßige Zuckerverbrennung Laktat produziert, das nicht einfach als Abfall verbleibt — es modifiziert Histone, schaltet TK1 ein, steigert den DNA‑Aufbau und Wachstumssignale und aktiviert einen Wnt‑getriebenen Kreislauf, der noch mehr Laktat erzeugt. Das Zerstören dieser Glykolyse–Lactylierungs–TK1–β‑Catenin‑Rückkopplung an einem ihrer Schlüsselabschnitte — etwa Glykolyse, Histon‑Lactylierung, TK1, RhoA oder Wnt‑Signalgebung — könnte neue Möglichkeiten bieten, eine Leukoplakie am Übergang zum Krebs zu hindern oder etabliertes OSCC zu behandeln, insbesondere bei HPV‑negativen Patientinnen und Patienten.
Zitation: Wang, Y., Geng, Y., Chen, Y. et al. Histone lactylation-driven feedback loop modulates pyrimidine metabolism to promote oral carcinogenesis. Cell Death Dis 17, 316 (2026). https://doi.org/10.1038/s41419-026-08580-w
Schlüsselwörter: oraler Krebs, Tumorstoffwechsel, Histon‑Lactylierung, Pyrimidinsynthese, Wnt‑Signalgebung