Clear Sky Science · nl
Door histonlactylatie aangedreven feedbacklus moduleert pyrimidinestofwisseling en bevordert mondkanker
Waarom dit belangrijk is voor mondgezondheid
Mondkanker begint vaak als een klein wit plekje in de mond en kan ongemerkt doorgroeien tot een levensbedreigende ziekte. Deze studie onthult hoe veranderingen in de manier waarop voorstadia‑cellen in de mond suiker verbranden een zich zelf versterkende lus creëren die hen richting daadwerkelijk kanker maakt. Door deze lus stap voor stap te volgen, laten de onderzoekers nieuwe moleculaire “drukpunten” zien die mogelijk gericht kunnen worden om mondtumoren te voorkomen of te vertragen.
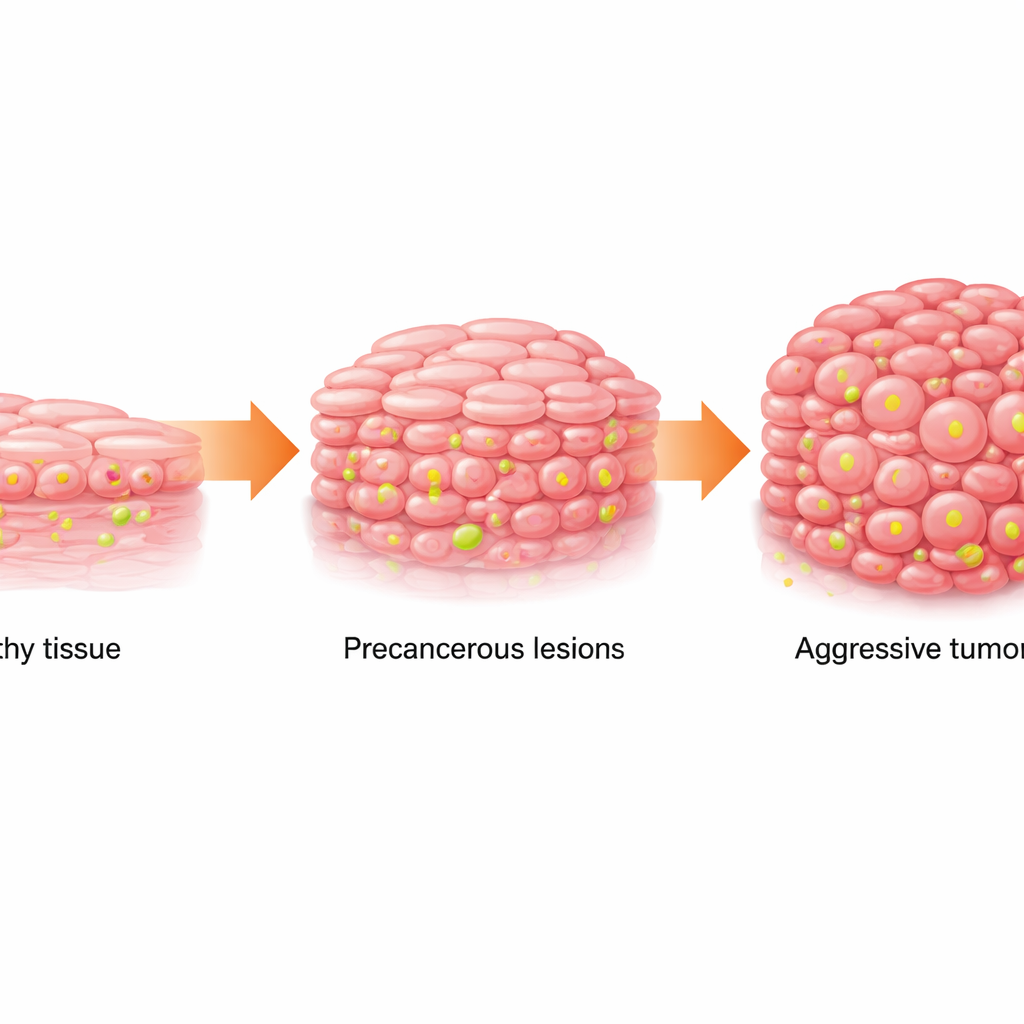
Van normaal weefsel naar gevaarlijke vlekken
Plaveiselcelcarcinoom van de mond (OSCC) is een veelvoorkomende en dodelijke mondkanker. Het ontwikkelt zich meestal geleidelijk: gezonde slijmvliescellen worden abnormaal (een toestand die orale leukoplakie wordt genoemd en zich uit als witte plekken) en zetten daarna om in kanker. Het team onderzocht humane monsters van normaal weefsel, leukoplakie en OSCC, evenals gegevens uit openbare kankerdatabases en single‑cell sequencing. Ze vonden dat naarmate weefsel zich van normaal naar voorstadium naar kankercel ontwikkelde, het metabolisme verschoof: cellen leunden meer op snelle suikerverbranding (glycolyse) en bouwden hogere lactaatniveaus op, een metabolisch bijproduct. Tegelijkertijd werd een specifieke chemische modificatie op de DNA‑verpakkingsproteïnen, histonlactylatie op de plaats H3K18, geleidelijk sterker.
Wanneer lactaat verandert in een genetische schakelaar
Lactaat wordt gewoonlijk gezien als metabool afval, maar hier functioneert het meer als een signaal. De onderzoekers toonden aan dat hoge lactaatniveaus leiden tot histonlactylatie, wat verandert hoe genen aan of uit gezet worden. Zowel in celkweken als in een muismodel van tongkanker verminderde blokkeren van glycolyse of verlagen van lactaat de algehele histonlactylatie en specifiek het H3K18‑kenmerk. Dit dempte celgroei, kolonievorming en het vermogen van cellen om te bewegen en te infiltreren — belangrijke kenmerken van kanker. Bij muizen die waren blootgesteld aan een chemische stof die tongtumoren opwekt, verkleinden behandelingen die glycolyse remmen de laesiegebieden, verminderde het aantal kwaadaardige plekken en veroorzaakten geen duidelijke lever‑ of nierschade, wat suggereert dat het richten op deze as zowel effectief als draaglijk kan zijn.
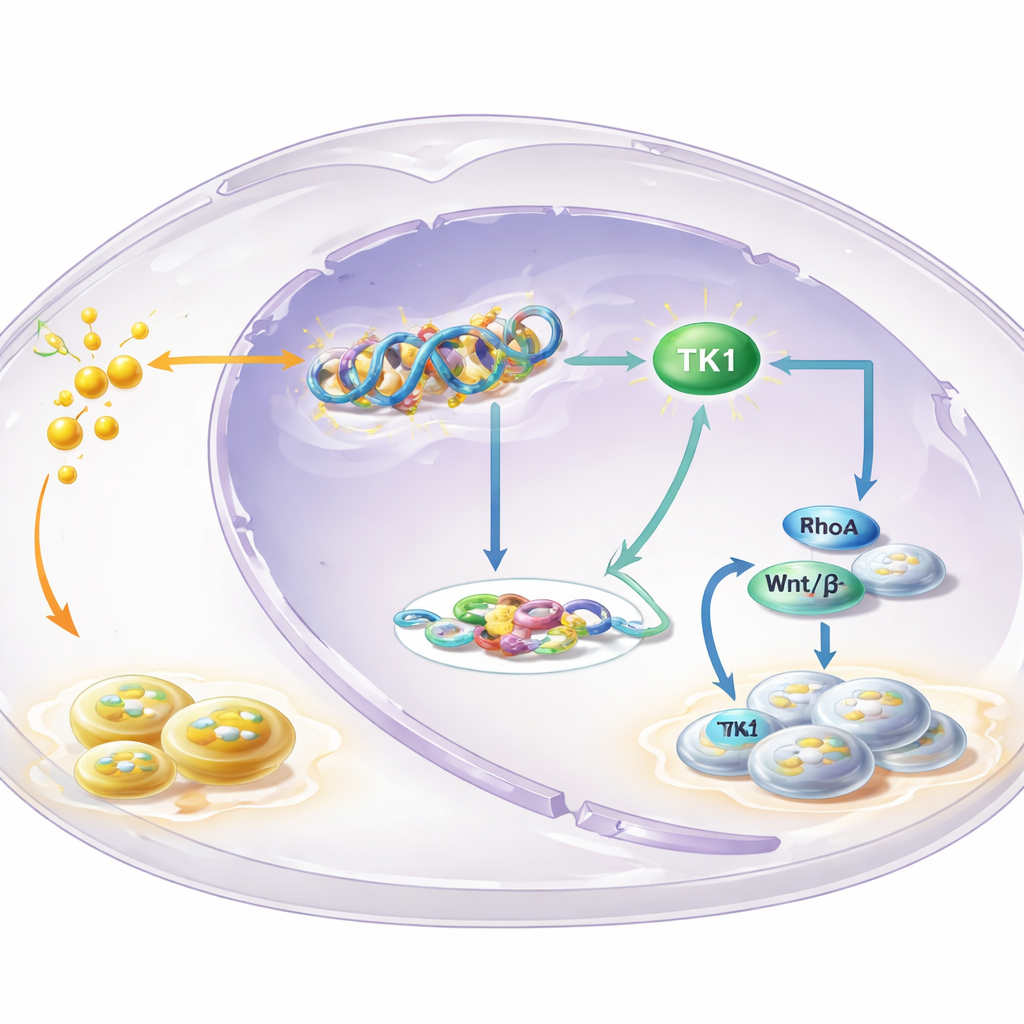
Een sleutelenzym in het hart van de lus
Om te achterhalen welke genen door H3K18‑lactylatie worden beheerd, bracht het team waar dit kenmerk op het genoom zit in kaart en combineerde dat met genexpressiegegevens. Eén uitschieter was thymidinekinase 1 (TK1), een enzym dat helpt bij de opbouw van DNA‑bouwstenen. Ze vonden dat H3K18‑lactylatie verrijkt was in het controlegebied van het TK1‑gen en dat het blokkeren van glycolyse TK1‑activiteit en het reservoir van DNA‑voorlopers in cellen verminderde, met name dTTP. TK1 kwam vaker voor in leukoplakie en OSCC dan in normaal weefsel, en patiënten wiens tumoren hogere TK1‑niveaus hadden, hadden over het algemeen een slechtere overleving. Het experimenteel verlagen van TK1 vertraagde celgroei, zette cellen vast in een vroeg stadium van de celdeling en verkleinde tumoren in muizen, wat TK1 markeert als een drijvende kracht in plaats van een toeschouwer.
Hoe TK1 signalering aandrijft en terugwerkt op het metabolisme
Het verhaal stopt niet bij DNA‑bouwstenen. De producten van TK1‑activiteit veranderen de balans tussen twee verwante moleculen, GTP en GDP, die schakelaars aansturen die bekendstaan als kleine GTPases. De studie richtte zich op één dergelijke schakelaar, RhoA, bekend om zijn invloed op celvorm, beweging en groei. Wanneer glycolyse werd geblokkeerd, daalde de GTP/GDP‑verhouding en nam RhoA‑activiteit af — maar beide werden hersteld door cellen geforceerd meer TK1 te laten maken. Dit versterkte op zijn beurt de Wnt/β‑catenine‑route, een krachtige groeibevorderende signaalweg. Actieve β‑catenine verhoogde de productie van c‑Myc en het glycolytische enzym LDHA, wat het lactaatniveau verder verhoogt. Meer lactaat voedt vervolgens meer histonlactylatie en TK1‑activatie, waarmee een zelfversterkende lus wordt gesloten die cellen voortdurend naar ongecontroleerde groei duwt.
Verschillende paden bij verschillende mondkankers
De onderzoekers vergeleken ook HPV‑negatieve en HPV‑positieve mondkankercellen. Terwijl het blokkeren van glycolyse en lactylatie HPV‑negatieve cellen sterk vertraagde, waren HPV‑positieve cellen minder afhankelijk van deze route, waarschijnlijk omdat virale oncoproteïnen alternatieve groeisignalen leveren. In patiëntmonsters correleerde het H3K18‑lactylatiekenmerk met afwijkende patronen van het tumorneerslagende eiwit p53, dat vaak gemuteerd is in OSCC en normaal gesproken glycolyse en DNA‑replicatie remt. Dit suggereert dat verlies van p53 en de lactaatgedreven lus kunnen samenwerken om vroege tumorontwikkeling te versnellen.
Wat dit betekent voor toekomstige behandelingen
Samengevat toont de studie aan dat in vroege mondlaesies overmatige suikerverbranding lactaat produceert, dat niet simpelweg als afval blijft liggen — het modificeert histonen, zet TK1 aan, vergroot de DNA‑opbouw en groeisignalen, en activeert een Wnt‑gedreven cyclus die terugvoedt om nog meer lactaat te genereren. Het doorbreken van deze glycolyse–lactylatie–TK1–β‑catenine feedbacklus op een van haar sleutelpunten — zoals glycolyse, histonlactylatie, TK1, RhoA of Wnt‑signalering — zou nieuwe mogelijkheden kunnen bieden om te voorkomen dat leukoplakie kanker wordt of om gevestigde OSCC te behandelen, vooral bij HPV‑negatieve patiënten.
Bronvermelding: Wang, Y., Geng, Y., Chen, Y. et al. Histone lactylation-driven feedback loop modulates pyrimidine metabolism to promote oral carcinogenesis. Cell Death Dis 17, 316 (2026). https://doi.org/10.1038/s41419-026-08580-w
Trefwoorden: mondkanker, tumormetabolisme, histonlactylatie, pyrimidinesynthese, Wnt-signaleringsroute