Clear Sky Science · it
Un anello di retroazione guidato dalla lattilazione degli istoni modula il metabolismo delle pirimidine per promuovere la carcinogenesi orale
Perché questo conta per la salute della bocca
Il cancro orale spesso inizia come una piccola chiazza bianca nella bocca e può progredire silenziosamente fino a diventare una malattia potenzialmente letale. Questo studio svela come i cambiamenti nel modo in cui le cellule precancerose della bocca metabolizzano lo zucchero generino un circuito auto‑rinforzante che le spinge verso il cancro conclamato. Tracciando questo circuito passo dopo passo, i ricercatori mettono in luce nuovi punti molecolari che potrebbero essere bersagliati per prevenire o rallentare i tumori orali.
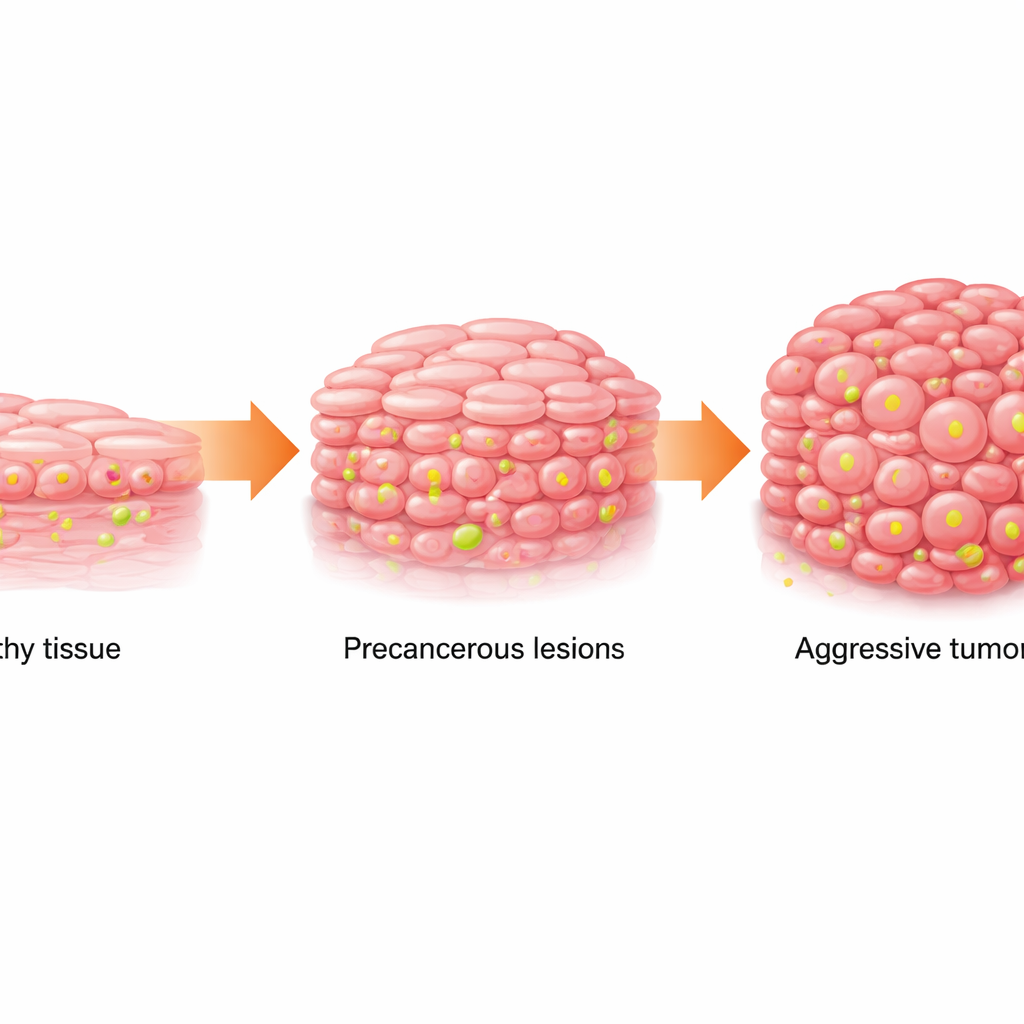
Dal tessuto normale alle chiazze pericolose
Il carcinoma squamoso orale (OSCC) è un tumore della bocca comune e letale. Di solito si sviluppa gradualmente: le cellule della mucosa sane diventano anomale (una condizione chiamata leucoplachia orale, che si presenta come macchie bianche) e poi progrediscono verso il cancro. Il team ha esaminato campioni umani di tessuto normale, leucoplachia e OSCC, oltre a dati da banche dati pubbliche sul cancro e da sequenziamento a singola cellula. Hanno scoperto che, man mano che il tessuto passa da normale a precanceroso e poi a canceroso, il suo metabolismo cambia: le cellule fanno maggior affidamento sulla rapida combustione dello zucchero (glicolisi) e accumulano livelli più elevati di lattato, un sottoprodotto metabolico. Allo stesso tempo, un particolare marcatore chimico sulle proteine che impacchettano il DNA, chiamato lattilazione degli istoni sul sito H3K18, si intensifica progressivamente.
Quando il lattato diventa un interruttore genetico
Il lattato è solitamente considerato un rifiuto metabolico, ma qui agisce più come un segnale. I ricercatori hanno dimostrato che alti livelli di lattato alimentano la lattilazione degli istoni, che modifica come i geni vengono accesi o spenti. In colture cellulari e in un modello murino di tumore della lingua, bloccare la glicolisi o ridurre il lattato ha diminuito la lattilazione complessiva degli istoni e in particolare il marcatore H3K18. Questo ha attenuato la proliferazione cellulare, la formazione di colonie e la capacità delle cellule di muoversi e invadere—caratteristiche chiave del cancro. Nei topi esposti a una sostanza chimica che induce tumori alla lingua, il trattamento con inibitori della glicolisi ha ridotto l’area delle lesioni, il numero di focolai cancerosi e non ha causato danni evidenti a fegato o reni, suggerendo che mirare a questo asse potrebbe essere efficace e tollerabile.
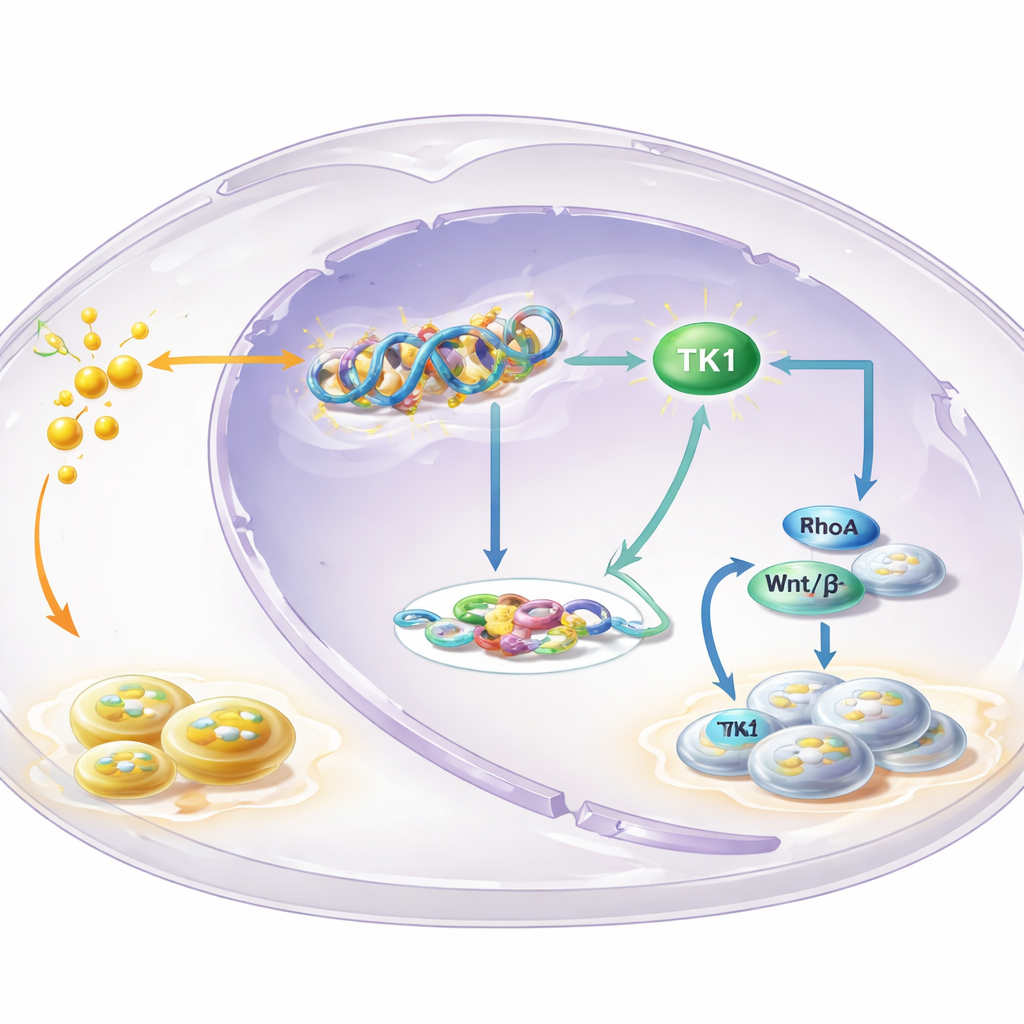
Un enzima chiave al centro dell’anello
Per identificare quali geni sono regolati dalla lattilazione su H3K18, il team ha mappato dove questo marcatore si trova sul genoma e ha combinato questi dati con l’espressione genica. Uno dei più rilevanti è stato la timidina chinasi 1 (TK1), un enzima che contribuisce a costruire i mattoni del DNA. Hanno trovato che la lattilazione di H3K18 era arricchita nella regione di controllo del gene TK1 e che bloccare la glicolisi riduceva l’attività di TK1 e la riserva di precursori del DNA nelle cellule, in particolare il dTTP. TK1 era più abbondante in leucoplachia e OSCC rispetto al tessuto normale, e i pazienti i cui tumori presentavano livelli più alti di TK1 tendevano ad avere una sopravvivenza peggiore. Ridurre sperimentalmente TK1 rallentava la crescita cellulare, bloccava le cellule in una fase precoce del ciclo cellulare e riduceva le dimensioni dei tumori nei topi, indicando che TK1 è un driver e non un semplice spettatore.
Come TK1 spinge la segnalazione e ricade sul metabolismo
La storia non si ferma ai mattoni del DNA. I prodotti dell’attività di TK1 alterano l’equilibrio tra due molecole correlate, GTP e GDP, che regolano interruttori noti come piccole GTPasi. Lo studio si è concentrato su uno di questi interruttori, RhoA, noto per influenzare la forma, il movimento e la crescita cellulare. Quando la glicolisi veniva bloccata, il rapporto GTP/GDP diminuiva e l’attività di RhoA calava—ma entrambi venivano ripristinati forzando le cellule a esprimere più TK1. Questo, a sua volta, potenziava la via Wnt/β‑catenina, un potente percorso di segnalazione pro‑crescita. La β‑catenina attiva aumentava la produzione di c‑Myc e dell’enzima glicolitico LDHA, che innalzano ulteriormente i livelli di lattato. Più lattato alimenta quindi più lattilazione degli istoni e attivazione di TK1, chiudendo un circuito auto‑rinforzante che spinge continuamente le cellule verso una crescita incontrollata.
Percorsi diversi in diversi tumori orali
I ricercatori hanno anche confrontato cellule di cancro orale HPV‑negative e HPV‑positive. Mentre bloccare la glicolisi e la lattilazione rallentava fortemente le cellule HPV‑negative, le cellule HPV‑positive erano meno dipendenti da questa via, probabilmente perché le proteine virali oncogene forniscono segnali di crescita alternativi. Nei campioni dei pazienti, il marcatore di lattilazione H3K18 correla con pattern anomali della proteina oncosoppressore p53, spesso mutata nell’OSCC e che normalmente limita la glicolisi e la replicazione del DNA. Questo suggerisce che la perdita di p53 e l’anello guidato dal lattato possano cooperare per accelerare lo sviluppo tumorale precoce.
Cosa significa per i trattamenti futuri
Nel complesso, lo studio mostra che nelle lesioni orali precoci l’eccessiva combustione dello zucchero produce lattato, che non rimane semplicemente un rifiuto: modifica gli istoni, attiva TK1, potenzia la sintesi dei mattoni del DNA e i segnali di crescita, e innesca un ciclo guidato dalla Wnt che ricade aumentando ancora il lattato. Interrompere questo circuito glicolisi–lattilazione–TK1–β‑catenina in uno qualsiasi dei suoi passaggi chiave—come la glicolisi, la lattilazione degli istoni, TK1, RhoA o la segnalazione Wnt—potrebbe offrire nuovi modi per impedire che una leucoplachia si trasformi in cancro o per trattare un OSCC già stabilito, in particolare nei pazienti HPV‑negativi.
Citazione: Wang, Y., Geng, Y., Chen, Y. et al. Histone lactylation-driven feedback loop modulates pyrimidine metabolism to promote oral carcinogenesis. Cell Death Dis 17, 316 (2026). https://doi.org/10.1038/s41419-026-08580-w
Parole chiave: cancro orale, metabolismo tumorale, lattilazione degli istoni, sintesi delle pirimidine, segnalazione Wnt