Clear Sky Science · he
לולאת משוב מונעת-לקטילציה של היסטונים משנה את חילוף החומרים של פירימידין ומקדמת קרצינוגנזה של הפה
מדוע זה חשוב לבריאות הפה
סרטן הפה מתחיל לעתים קרובות ככתם לבן קטן ברירית הפה ויכול להתפתח בשקט למחלה מסכנת חיים. מחקר זה מגלה כיצד שינויים באופן שבו תאים טרום-סרטניים שורפים סוכר יוצרים לולאת משוב מחזקת שמניעה אותם לקראת סרטן מתקדם. במיפוי צעד אחר צעד של הלולאה חשפו החוקרים "נקודות לחץ" מולקולריות חדשות שעשויות להוות מטרה למניעה או להאטת גידולי הפה.
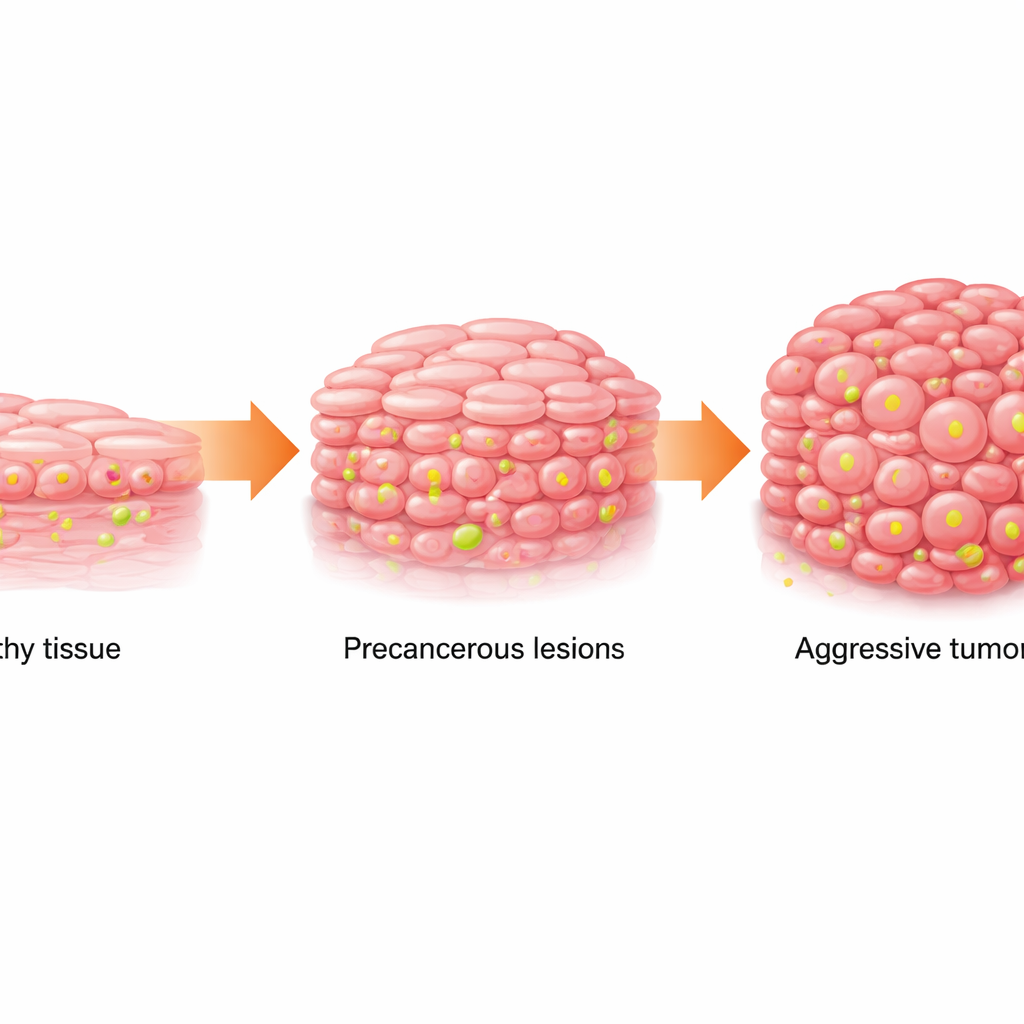
מרקמה תקינה לכתמים מסוכנים
קרצינומת תאי קשקש של הפה (OSCC) היא סרטן נפוץ וקטלני של הפה. הוא מתפתח בדרך כלל בהדרגה: תאי הרירית הבריאים הופכים לבלתי תקינים (מצב הנקרא ליהוקופלקיה אוראלית, המופיעה ככתמים לבנים) ואז מתקדמים לסרטן. הצוות בדק דגימות אנושיות ממרקמות תקינות, ליהוקופלקיה ו-OSCC, וכן נתונים מבסיסי נתוני סרטן ציבוריים וריצוף חד-תאי. הם מצאו שכאשר הרקמה עוברת ממצב תקין לטרום-סרטני ולסרטני, המטבוליזם שלה משתקף: התאים מסתמכים יותר על שריפת סוכר מהירה (גליקוליזה) וצוברים רמות גבוהות יותר של לקטאט, תוצר לוואי מטבולי. במקביל, סימן כימי ספציפי על חלבוני אריזת ה-DNA, שנקרא לקטילציה של היסטון באתר H3K18, התחזק בהדרגה.
כשלקטאט הופך למתג גנטי
לקטאט נתפס בדרך כלל כסימן לבזבוז מטבולי, אך כאן הוא פועל יותר כאות. החוקרים הראו שרמות לקטאט גבוהות מכניסות לקטילציה של היסטונים, שמשנה את אופן הפתיחה או הסגירה של גנים. בתרביות תאים ובמודל חולדה של סרטן הלשון, חסימת גליקוליזה או הפחתת לקטאט הפחיתה את רמות הלקטילציה הכלליות ובעיקר את סימן H3K18. זה הגביל גדילת תאים, היווצרות קבוצות תאים (קולוניות) ואת יכולת התנועה והפלישה של התאים — מאפיינים מרכזיים של סרטן. בעכברים שנחשפו לחומר כימי שמשרה גידולי לשון, טיפול בחוסמי גליקוליזה הקטין את שטח הנגעים, הפחית את מספר הנקודות הסרטניות ולא גרם לנזק ברור לכבד או לכליות, מה שמרמז כי מיקוד על ציר זה עשוי להיות גם יעיל וגם נסבל.
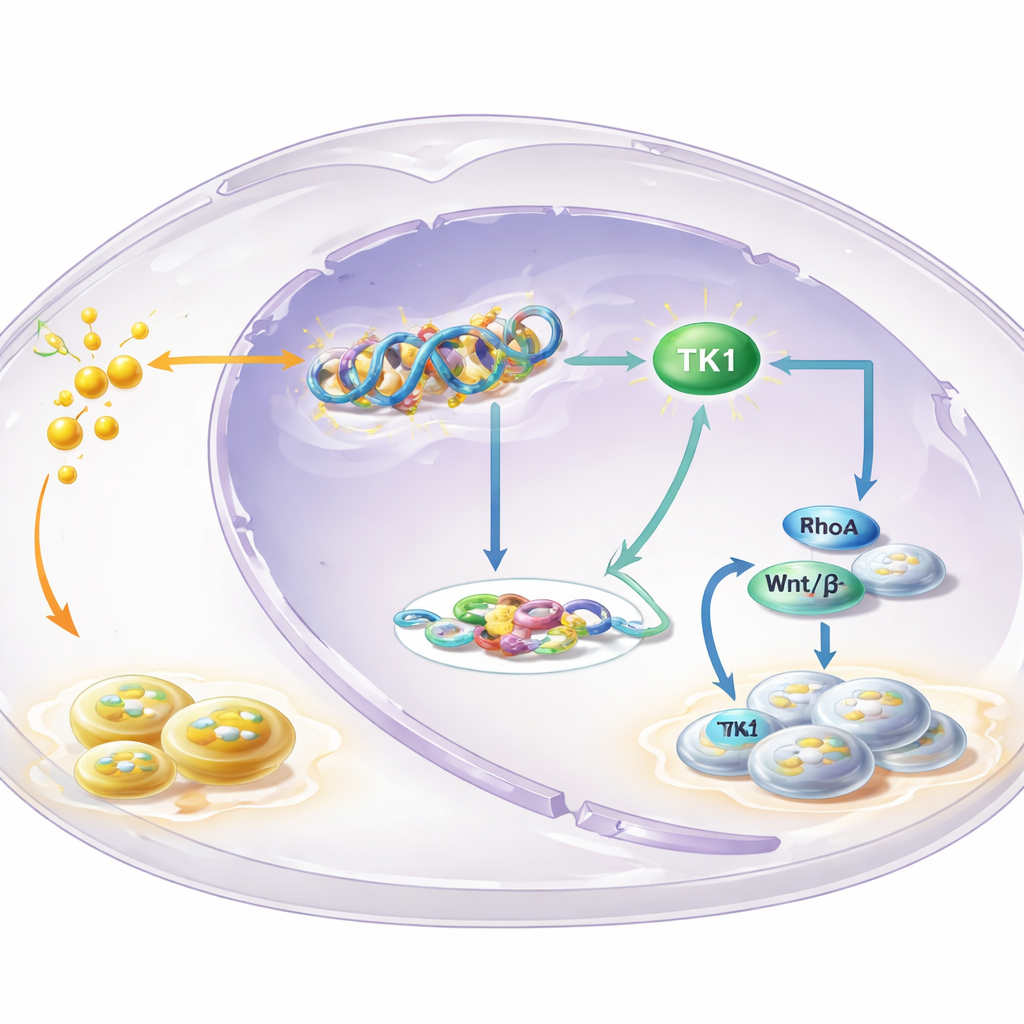
אנזים מרכזי בלב הלולאה
כדי לזהות אילו גנים נשלטים על ידי לקטילציה ב-H3K18, הצוות מיפה היכן הסימן נמצא בגנום ושילב זאת עם נתוני ביטוי גנים. אחד הבולטים היה תימידין קינאז 1 (TK1), אנזים המסייע לבניית אבני הבניין של ה-DNA. הם מצאו שלקטילציה ב-H3K18 רוכזת באזור הבקרה של גן TK1 וכי חסימת גליקוליזה הפחיתה את פעילות TK1 ואת מאגר מקדמי ה-DNA בתאים, במיוחד את dTTP. רמות TK1 היו גבוהות יותר בליהוקופלקיה וב-OSCC מאשר ברקמה תקינה, ומטופלים שלגידוליהם היו רמות גבוהות של TK1 נטו להישרדות גרועה יותר. הורדה ניסויית של TK1 האטה גדילת תאים, דחפה את התאים להשהייה בשלב מוקדם במחזור התא והקטינה גידולים בעכברים, מה שמציין ש-TK1 הוא ביצועי ולא רק על-ידי-מקרה.
כיצד TK1 דוחף איתות ומוחזר על המטבוליזם
הסיפור אינו מסתיים באבני בניין ל-DNA. תוצרי פעילות TK1 משנים את האיזון בין שתי מולקולות קרובות, GTP ו-GDP, השולטות במתגים הנקראים GTPases קטנים. המחקר התמקד במתג אחד כזה, RhoA, המוכר בהשפעתו על צורת התא, תזוזתו וצמיחתו. כשחסמו גליקוליזה, יחס GTP/GDP ירד ופעילות RhoA פחתה — אך שניהם שוחזרו על-ידי אילוץ התאים לייצר יותר TK1. זה, בתורו, חיזק את מסלול Wnt/β-catenin, נתיב איתות רב עוצמה שמעודד צמיחה. β-catenin פעיל הגביר את ייצור c-Myc ואת האנזים הגליקוליטי LDHA, שהגביר עוד יותר את רמות הלקטאט. לקטאט רב יותר הדלק עוד לקטילציה של היסטונים ופעילות TK1, וסגר לולאת משוב עצמית שמניעה את התאים בהתמדה לכיוון גדילה בלתי נשלטת.
מסלולים שונים בסוגי סרטן פה שונים
החוקרים גם השוו תאי סרטן פה שליליים ל-HPV מול חיוביים ל-HPV. בעוד שחסימת גליקוליזה ולקטילציה האטה בחוזקה תאים שליליים ל-HPV, התאים החיוביים ל-HPV היו פחות תלויים בציר זה, ככל הנראה מפני שחלבוני וירוס ממאירים מספקים אותות צמיחה חלופיים. בדגימות מטופלים, סימן לקטילציה ב-H3K18 היה מתואם עם דפוסים בלתי רגילים של חלבון המדכא גידול p53, שלעיתים קרובות מוטנטי ב-OSCC ובמצב תקין מעכב גליקוליזה ושכפול DNA. זה מרמז שאבדן p53 ולולאת הלקטאט המונעת עשויים לשתף פעולה להאצת התפתחות הגידול המוקדמת.
מה זה אומר לטיפולים עתידיים
בסך הכול, המחקר מראה שבנגעים מוקדמים בפה, שריפת סוכר מוגברת מייצרת לקטאט, שהוא לא רק פסולת — הוא מקשט היסטונים, מדליק TK1, מגדיל בניית DNA ואותות צמיחה ומפעיל מעגל מונע-וונתי שמזין ייצור לקטאט נוסף. שבירת לולאת המשוב גליקוליזה–לקטילציה–TK1–β-catenin בכל אחד מצעדי המפתח שלה — כגון גליקוליזה, לקטילציה של היסטונים, TK1, RhoA או איתות Wnt — עשויה להציע דרכים חדשות למנוע ליהוקופלקיה מלהפוך לסרטן או לטפל ב-OSCC מבוסס, במיוחד בחולים שליליים ל-HPV.
ציטוט: Wang, Y., Geng, Y., Chen, Y. et al. Histone lactylation-driven feedback loop modulates pyrimidine metabolism to promote oral carcinogenesis. Cell Death Dis 17, 316 (2026). https://doi.org/10.1038/s41419-026-08580-w
מילות מפתח: סרטן הפה, מטבוליזם של גידול, לקטילציה של היסטונים, סינתזת פירימידין, אותות וונט (Wnt)