Clear Sky Science · pt
Loop de retroalimentação impulsionado por lactilação de histonas modula o metabolismo de pirimidina para promover a carcinogênese oral
Por que isso importa para a saúde bucal
O câncer oral frequentemente começa como uma pequena mancha branca na boca e pode progredir silenciosamente para uma doença potencialmente fatal. Este estudo revela como mudanças na forma como células pré‑cancerosas da boca metabolizam açúcar criam um ciclo autorreforçador que as empurra rumo ao câncer pleno. Ao rastrear esse circuito passo a passo, os pesquisadores identificam novos "pontos de pressão" moleculares que podem ser alvos para prevenir ou retardar tumores orais.
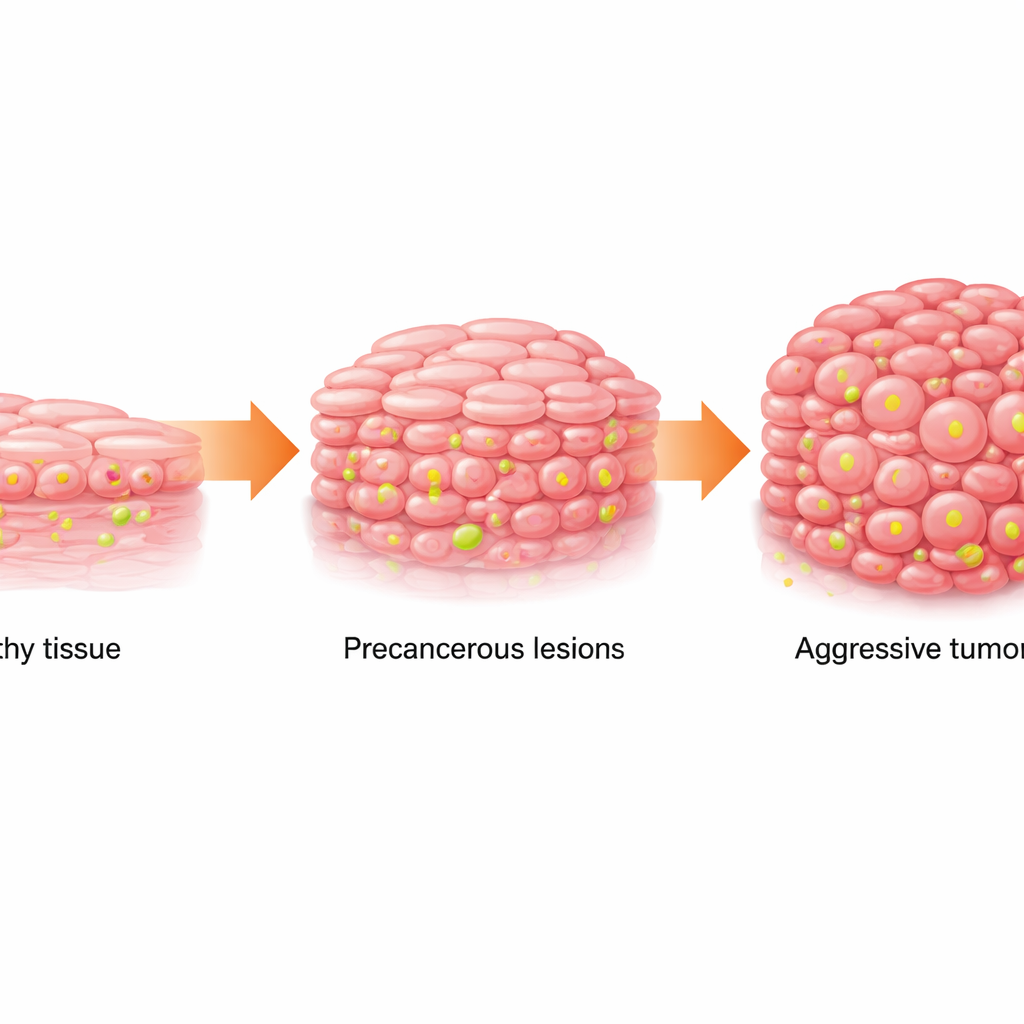
Do tecido normal a manchas perigosas
O carcinoma de células escamosas oral (OSCC) é um câncer comum e letal da boca. Ele geralmente se desenvolve gradualmente: células da mucosa saudáveis tornam‑se anormais (uma condição chamada leucoplasia oral, que aparece como manchas brancas) e depois progridem para câncer. A equipe analisou amostras humanas de tecido normal, leucoplasia e OSCC, além de dados de bancos públicos de câncer e sequenciamento de célula única. Eles descobriram que, à medida que o tecido evoluía de normal para pré‑canceroso e depois para canceroso, seu metabolismo mudava: as células passaram a depender mais da queima rápida de açúcar (glicólise) e acumularam níveis mais altos de lactato, um subproduto metabólico. Ao mesmo tempo, uma marca química específica nas proteínas que compactam o DNA, chamada lactilação de histonas no sítio H3K18, tornava‑se progressivamente mais intensa.
Quando o lactato vira um interruptor genético
Lactato costuma ser visto como resíduo metabólico, mas aqui atua mais como um sinal. Os pesquisadores demonstraram que níveis elevados de lactato alimentam a lactilação de histonas, que altera como genes são ativados ou silenciados. Em culturas celulares e em um modelo murino de câncer de língua, bloquear a glicólise ou reduzir o lactato diminuiu a lactilação global de histonas e, especificamente, a marca H3K18. Isso atenuou o crescimento celular, a formação de colônias e a capacidade de migração e invasão — características-chave do câncer. Em camundongos expostos a um químico que induz tumores de língua, o tratamento com bloqueadores da glicólise reduziu a área das lesões, diminuiu o número de focos cancerosos e não causou dano hepático ou renal óbvio, sugerindo que mirar nesse eixo pode ser eficaz e tolerável.
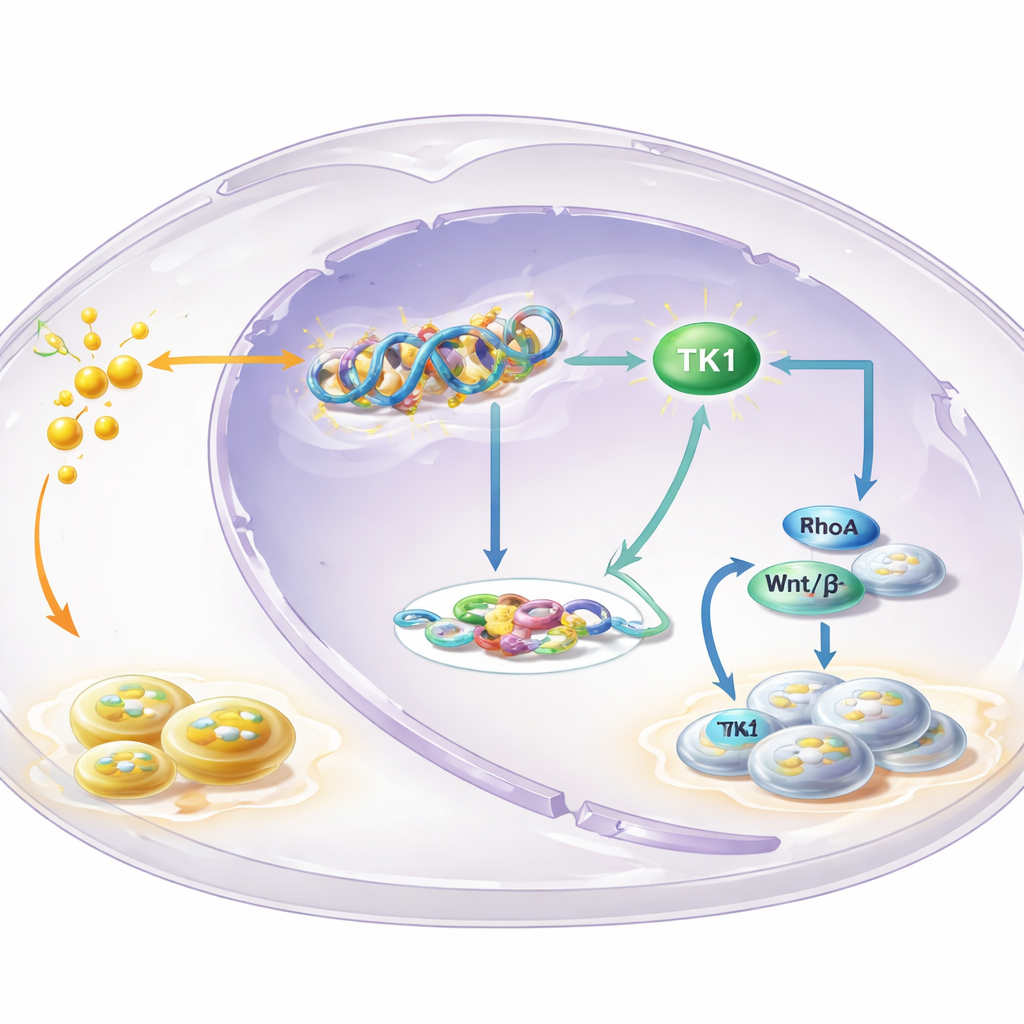
Uma enzima-chave no centro do circuito
Para identificar quais genes são controlados pela lactilação em H3K18, a equipe mapeou onde essa marca se localiza no genoma e combinou esses dados com perfis de expressão gênica. Um destaque foi a timidina quinase 1 (TK1), uma enzima que ajuda a construir os blocos de construção do DNA. Eles descobriram que a lactilação em H3K18 estava enriquecida na região reguladora do gene TK1 e que bloquear a glicólise reduzia a atividade de TK1 e o reservatório de precursores do DNA nas células, especialmente um chamado dTTP. TK1 era mais abundante em leucoplasia e OSCC do que em tecido normal, e pacientes cujos tumores apresentavam níveis mais altos de TK1 tendiam a ter pior sobrevida. Reduzir experimentalmente a TK1 retardou o crescimento celular, fez as células pausarem em uma fase inicial do ciclo celular e encolheu tumores em camundongos, caracterizando TK1 como um motor do processo, e não um mero espectador.
Como a TK1 impulsiona sinalização e retroalimenta o metabolismo
A história não termina nos blocos de DNA. Os produtos da atividade da TK1 alteram o equilíbrio entre duas moléculas relacionadas, GTP e GDP, que controlam chaves conhecidas como pequenas GTPases. O estudo concentrou‑se em um desses interruptores, RhoA, conhecido por influenciar forma, movimento e crescimento celular. Quando a glicólise foi bloqueada, a razão GTP/GDP caiu e a atividade de RhoA diminuiu — mas ambos foram restaurados ao forçar as células a produzir mais TK1. Isso, por sua vez, reforçou a via Wnt/β‑catenina, uma rota de sinalização poderosa que promove crescimento. A β‑catenina ativa aumentou a produção de c‑Myc e da enzima glicolítica LDHA, o que eleva ainda mais os níveis de lactato. Mais lactato então alimenta mais lactilação de histonas e ativação de TK1, fechando um ciclo autorreforçador que empurra continuamente as células para o crescimento descontrolado.
Caminhos diferentes em diferentes cânceres orais
Os pesquisadores também compararam células de câncer oral negativas para HPV e positivas para HPV. Enquanto bloquear a glicólise e a lactilação retardou fortemente as células HPV‑negativas, as células HPV‑positivas foram menos dependentes dessa via, provavelmente porque proteínas virais oncogênicas fornecem sinais de crescimento alternativos. Em amostras de pacientes, a marca de lactilação em H3K18 correlacionou com padrões anormais da proteína supressora de tumor p53, frequentemente mutada no OSCC e que normalmente restringe glicólise e replicação do DNA. Isso sugere que a perda de p53 e o circuito impulsionado por lactato podem cooperar para acelerar o desenvolvimento tumoral precoce.
O que isso significa para tratamentos futuros
No conjunto, o estudo mostra que em lesões bucais iniciais o excesso de queima de açúcar produz lactato, que não fica apenas como resíduo — ele modifica histonas, ativa TK1, impulsiona a produção de blocos de DNA e sinais de crescimento, e ativa um ciclo dirigido por Wnt que retroalimenta para gerar ainda mais lactato. Romper esse loop glicólise–lactilação–TK1–β‑catenina em qualquer de seus elos chave — como glicólise, lactilação de histonas, TK1, RhoA ou sinalização Wnt — pode oferecer novas maneiras de impedir que leucoplasias se tornem câncer ou de tratar OSCC estabelecido, especialmente em pacientes HPV‑negativos.
Citação: Wang, Y., Geng, Y., Chen, Y. et al. Histone lactylation-driven feedback loop modulates pyrimidine metabolism to promote oral carcinogenesis. Cell Death Dis 17, 316 (2026). https://doi.org/10.1038/s41419-026-08580-w
Palavras-chave: câncer oral, metabolismo tumoral, lactilação de histonas, síntese de pirimidina, sinalização Wnt