Clear Sky Science · ar
حلقة تغذية راجعة مدفوعة بإلاكتيلات الهيستون تعدل أيض البيريميدين لتعزيز التسرطن الفموي
لماذا هذا مهم لصحة الفم
غالبًا ما يبدأ سرطان الفم كبقعة بيضاء صغيرة في الفم ويمكن أن يتقدّم بهدوء إلى مرض يهدد الحياة. تكشف هذه الدراسة كيف أن التغييرات في طريقة احتراق السكر داخل الخلايا قبل السرطانية في الفم تخلق حلقة تغذية راجعة تعزز تحولها إلى سرطان كامل. من خلال تتبع هذه الحلقة خطوة بخطوة، يبرز الباحثون نقاط ضعف جزيئية جديدة قد يُستهدَف لمعالجة أو إبطاء الأورام الفموية.
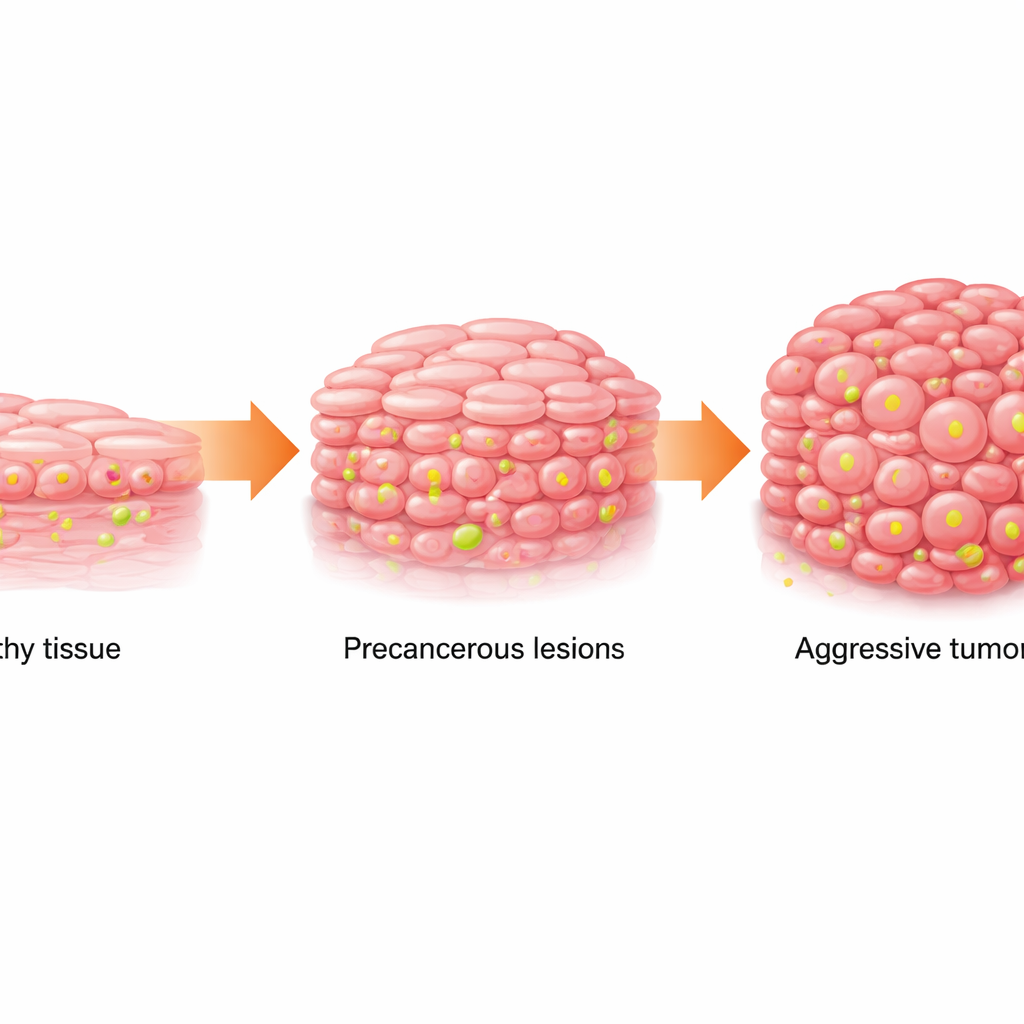
من النسيج الطبيعي إلى البقع الخطرة
سرطان الخلايا الحرشفية الفموي (OSCC) هو سرطان شائع قاتل في الفم. يتطور عادة تدريجيًا: تتحول خلايا البطانة السليمة إلى خلايا غير طبيعية (حالة تُسمى بقع بيضاء فموية أو لوكيوبلاكيا) ثم تتقدم إلى السرطان. فحص الفريق عينات بشرية من نسيج سليم، ولوكيوبلاكيا، وOSCC، بالإضافة إلى بيانات من قواعد بيانات سرطانية عامة وتسلسل خلية مفردة. وجدوا أنه مع انتقال النسيج من طبيعي إلى ما قبل سرطاني ثم إلى سرطاني، يتغير أيضه: تعتمد الخلايا أكثر على احتراق السكر السريع (التحلل السكري) وتتراكم مستويات أعلى من اللاكتات، المنتج الثانوي الأيضي. وفي الوقت نفسه، أصبح علامة كيميائية محددة على بروتينات تغليف الحمض النووي—تسمى لاكتيلية الهيستون عند الموقع H3K18—أقوى تدريجيًا.
عندما يتحول اللاكتات إلى مفتاح جيني
عادة ما يُنظر إلى اللاكتات على أنها نفاية أيضية، لكنه هنا يعمل كإشارة. أظهرت التجارب أن مستويات اللاكتات العالية تغذي لاكتيلية الهيستون، مما يغير كيفية تشغيل أو إيقاف الجينات. في مستنبتات خلوية ونموذج فأري لسرطان اللسان، أدى حجب التحلل السكري أو خفض اللاكتات إلى تقليل لاكتيلية الهيستون عمومًا وبشكل خاص علامة H3K18. خفّض هذا من نمو الخلايا وتشكيل المستعمرات وقدرة الخلايا على الحركة والغزو—خصائص أساسية للسرطان. في فئران تعرضت لمادة كيميائية تحفز أورام اللسان، أدى العلاج بحاصرات التحلل السكري إلى تقلص مساحة الآفات وتقليل عدد البقع السرطانية، ولم يسبب ضررًا واضحًا للكبد أو الكلى، مما يشير إلى أن استهداف هذا المحور قد يكون فعالًا ومتحملاً.
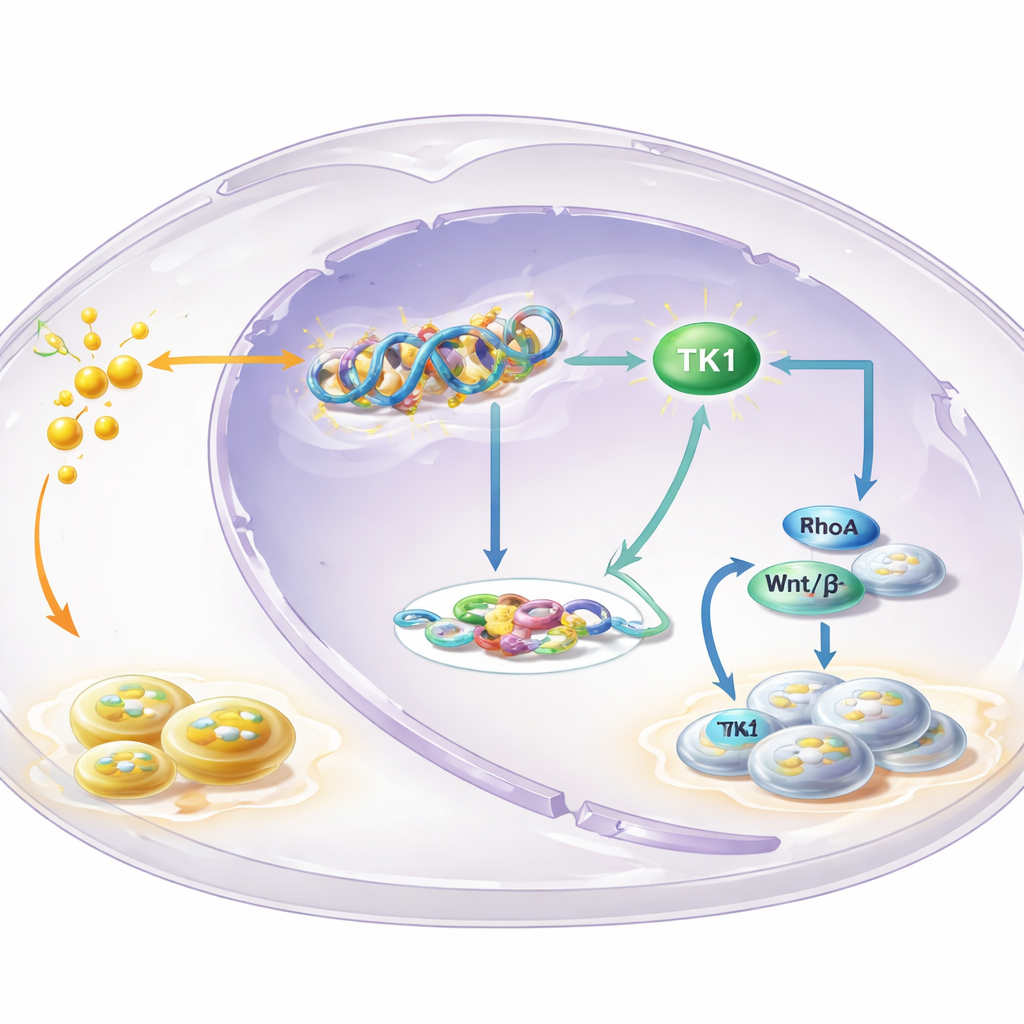
إنزيم رئيسي في قلب الحلقة
لتحديد الجينات التي تتحكم بها لاكتيلية H3K18، رسم الفريق مواقع هذه العلامة على الجينوم ودمجها مع بيانات التعبير الجيني. برز إنزيم واحد هو ثايميدين كيناز 1 (TK1)، وهو إنزيم يساعد في بناء لبنات الحمض النووي. وجدوا أن لاكتيلية H3K18 كانت متجمعة في منطقة التحكم بجين TK1 وأن حجب التحلل السكري قلّل من نشاط TK1 ومخزون سواغ الحمض النووي داخل الخلايا، وخصوصًا dTTP. كان TK1 أكثر وفرة في اللوكيوبلاكيا وOSCC مقارنة بالنسيج الطبيعي، والمرضى الذين كانت أورامهم تحتوي على مستويات أعلى من TK1 مالوا إلى بقاء أسوأ. أدى خفض TK1 تجريبيًا إلى إبطاء نمو الخلايا، ودفع الخلايا إلى التوقف في مرحلة مبكرة من دورة الخلية، وتقليص الأورام في الفئران، مما يدل على أن TK1 عامل دفع وليس مجرد مارة.
كيف يدفع TK1 الإشارة ويؤثر مرة أخرى على الأيض
القصة لا تتوقف عند لبنات الحمض النووي. تغير منتجات نشاط TK1 التوازن بين جزيئتين مرتبطتين، GTP وGDP، اللتين تتحكمان بمفاتيح تُعرف باسم الجي بيكازات الصغيرة. ركزت الدراسة على مفتاح واحد، RhoA، المعروف بتأثيره على شكل الخلية وحركتها ونموها. عند حجب التحلل السكري، انخفضت نسبة GTP/GDP ونشاط RhoA—لكنهما استُرجعا عندما أُجبرت الخلايا على إنتاج المزيد من TK1. هذا بدوره عزّز طريق إشارة Wnt/β‑catenin، وهو مسار قوي يعزز النمو. زاد β‑catenin النشط إنتاج c‑Myc وإنزيم التحلل السكري LDHA، مما يرفع مستويات اللاكتات أكثر. ثم يغذي المزيد من اللاكتات المزيد من لاكتيلية الهيستون وتفعيل TK1، مغلقًا حلقة تغذية راجعة تدفع الخلايا باستمرار نحو النمو غير المنضبط.
مسارات مختلفة في سرطانات فموية مختلفة
قارن الباحثون أيضًا خلايا سرطان الفم السلبية لـ HPV مع الإيجابية للفيروس. بينما أدى حجب التحلل السكري واللاكتيلية إلى إبطاء قوي في الخلايا السالبة لـ HPV، كانت الخلايا الموجبة للـ HPV أقل اعتمادًا على هذا المسار، ربما لأن بروتينات الفيروس المسرطنة توفر إشارات نمو بديلة. في عينات المرضى، ارتبطت علامة لاكتيلية H3K18 بأنماط شاذة لبروتين كابح الورم p53، الذي غالبًا ما يتحور في OSCC ويمنع عادة التحلل السكري وتكرار الحمض النووي. يشير هذا إلى أن فقدان p53 وحلقة اللاكتات المدفوعة قد يتعاونان لتسريع تطور الورم المبكر.
ماذا يعني هذا للعلاجات المستقبلية
تُظهر الدراسة في المجمل أن في الآفات الفموية المبكرة، يؤدي احتراق السكر الزائد إلى إنتاج اللاكتات، التي لا تبقى مجرد نفاية—بل تزيّن الهيستونات، وتشغّل TK1، وتعزز بناء الحمض النووي وإشارات النمو، وتنشّط حلقة مدفوعة بـ Wnt تعيد تغذية إنتاج اللاكتات. إن كسر حلقة التغذية هذه بين التحلل السكري–اللاكتيلية–TK1–β‑catenin عند أي من خطواتها الأساسية—مثل التحلل السكري، لاكتيلية الهيستون، TK1، RhoA، أو إشارات Wnt—قد يقدّم طرقًا جديدة لمنع تحول اللوكيوبلاكيا إلى سرطان أو لعلاج OSCC القائم، خصوصًا لدى المرضى سلبيي HPV.
الاستشهاد: Wang, Y., Geng, Y., Chen, Y. et al. Histone lactylation-driven feedback loop modulates pyrimidine metabolism to promote oral carcinogenesis. Cell Death Dis 17, 316 (2026). https://doi.org/10.1038/s41419-026-08580-w
الكلمات المفتاحية: سرطان الفم, أيض الورم, لاكتيلية الهيستون, تخليق البيريميدين, إشارة Wnt