Clear Sky Science · pl
Sprzężenie zwrotne napędzane laktylacją histonów modyfikuje metabolizm pirymidyn, promując karcinogenezę jamy ustnej
Dlaczego to ma znaczenie dla zdrowia jamy ustnej
Rak jamy ustnej często zaczyna się jako niewielka biała plamka i może cicho postępować do choroby zagrażającej życiu. W tym badaniu odkryto, w jaki sposób zmiany w sposobie, w jaki przedrakowe komórki jamy ustnej przetwarzają cukier, tworzą samonapędzające się sprzężenie, które popycha je w stronę pełnoobjawowego nowotworu. Śledząc to sprzężenie krok po kroku, badacze ujawniają nowe molekularne „punkty nacisku”, które mogą być celem zapobiegania lub spowalniania rozwoju nowotworów jamy ustnej.
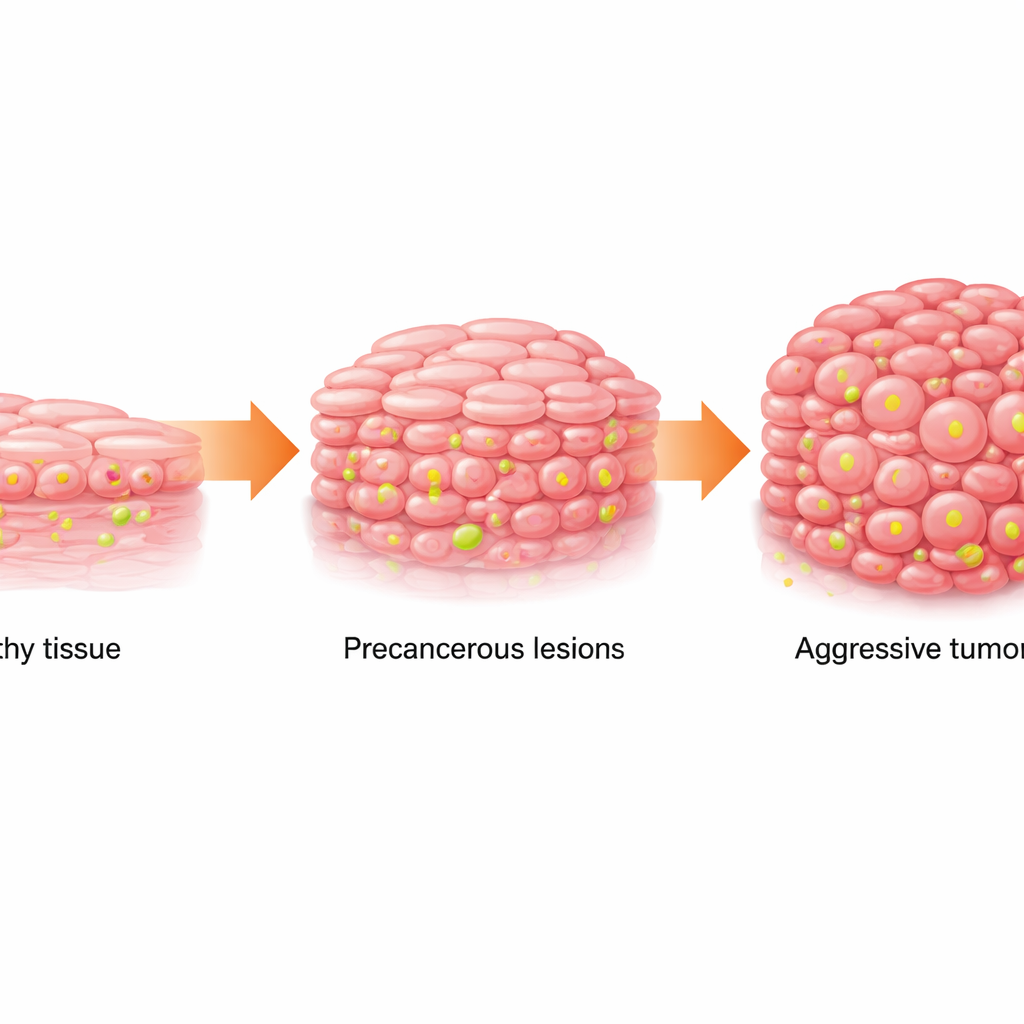
Od tkanki prawidłowej do niebezpiecznych plam
Rogowiak płaskonabłonkowy jamy ustnej (OSCC) to powszechny i śmiertelny nowotwór jamy ustnej. Zazwyczaj rozwija się stopniowo: komórki wyściełające przełyk stają się nieprawidłowe (stan zwany leukoplakią, objawiający się białymi plamami), a następnie przechodzą w raka. Zespół przebadał próbki ludzkie pochodzące z tkanki prawidłowej, leukoplakii i OSCC oraz dane z publicznych baz nowotworowych i sekwencjonowania pojedynczych komórek. Stwierdzili, że wraz z przejściem tkanki od stanu prawidłowego przez przedrakowy do rakowego zmienia się metabolizm: komórki coraz bardziej polegają na szybkim spalaniu cukru (glikolizie) i gromadzą wyższe poziomy mleczanu, produktu metabolicznego. Jednocześnie specyficzny chemiczny znacznik na białkach pakujących DNA, zwany laktylacją histonów w miejscu H3K18, stopniowo się nasilał.
Gdy mleczan staje się przełącznikiem genetycznym
Mleczan jest zwykle uważany za odpad metaboliczny, ale tutaj działa raczej jak sygnał. Badacze wykazali, że wysokie poziomy mleczanu zasilają laktylację histonów, która zmienia sposób, w jaki geny są włączane lub wyłączane. Zarówno w hodowlach komórek, jak i w modelu mysim raka języka, blokowanie glikolizy lub obniżanie poziomu mleczanu zmniejszało ogólną laktylację histonów, a w szczególności znacznik H3K18. Tłumiło to wzrost komórek, tworzenie kolonii oraz zdolność komórek do poruszania się i inwazji — kluczowe cechy nowotworu. U myszy wystawionych na chemiczny induktor guzów języka leczenie inhibitorami glikolizy zmniejszało obszar zmian, redukowało liczbę ognisk nowotworowych i nie powodowało oczywistych uszkodzeń wątroby ani nerek, co sugeruje, że celowanie w tę oś może być zarówno skuteczne, jak i tolerowane.
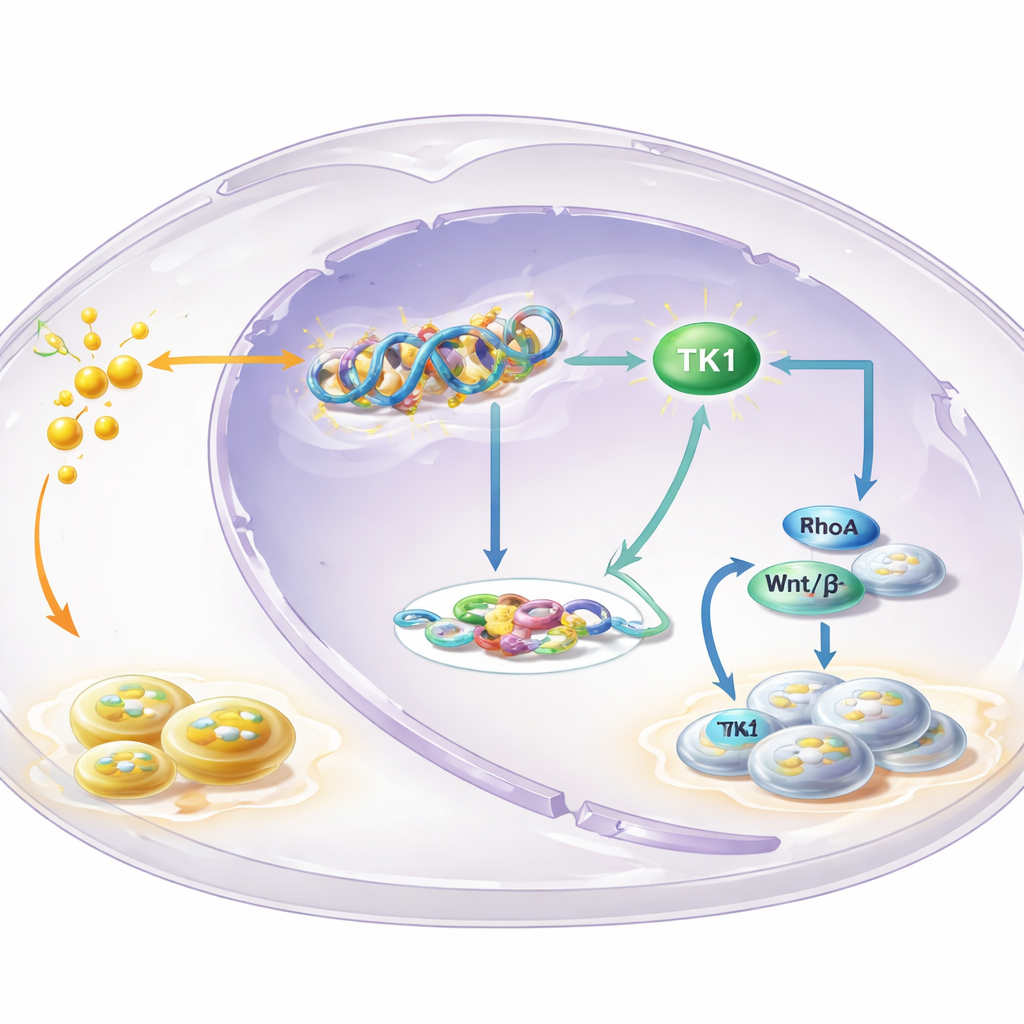
Kluczowy enzym w centrum pętli
Aby ustalić, które geny są kontrolowane przez laktylację H3K18, zespół zmapował położenie tego markera w genomie i powiązał to z danymi o ekspresji genów. Jednym z wyróżniających się był kinaza tymidynowa 1 (TK1), enzym uczestniczący w budowie składników DNA. Odkryto, że laktylacja H3K18 była wzbogacona w regionie regulatorowym genu TK1, a blokowanie glikolizy obniżało aktywność TK1 i pulę prekursorów DNA w komórkach, szczególnie dTTP. TK1 występował w większej ilości w leukoplakii i OSCC niż w tkance prawidłowej, a pacjenci, których guzy miały wyższe poziomy TK1, mieli skłonność do gorszego przeżycia. Eksperymentalne obniżenie TK1 spowalniało wzrost komórek, zatrzymywało je w wczesnej fazie cyklu komórkowego i zmniejszało guzy u myszy, co oznacza, że TK1 działa jako czynnik napędowy, a nie tylko bierny towarzysz.
Jak TK1 pobudza sygnalizację i oddziałuje na metabolizm
Opowieść nie kończy się na prekursorach DNA. Produkty aktywności TK1 zmieniają równowagę między dwoma powiązanymi cząsteczkami, GTP i GDP, które kontrolują przełączniki znane jako małe GTPazy. Badanie skupiło się na jednym z tych przełączników, RhoA, znanym z wpływu na kształt, ruch i wzrost komórek. Gdy glikoliza została zablokowana, stosunek GTP/GDP spadł, a aktywność RhoA zmalała — jednak oba parametry zostały przywrócone przez wymuszenie zwiększonej produkcji TK1. To z kolei wzmocniło szlak Wnt/β-katenina, potężną drogę promującą wzrost. Aktywna β-katenina zwiększała produkcję c-Myc i enzymu glikolitycznego LDHA, co dalej podnosiło poziomy mleczanu. Więcej mleczanu potem zasilało kolejną laktylację histonów i aktywację TK1, zamykając samonapędzającą się pętlę, która nieustannie popycha komórki ku niekontrolowanemu wzrostowi.
Różne ścieżki w różnych nowotworach jamy ustnej
Badacze porównali także komórki raka jamy ustnej ujemne i dodatnie pod kątem HPV. Podczas gdy blokowanie glikolizy i laktylacji silnie spowalniało komórki HPV-ujemne, komórki HPV-dodatnie były mniej zależne od tej ścieżki, prawdopodobnie dlatego, że wirusowe onkoproteiny dostarczają alternatywne sygnały wzrostu. W próbkach pacjentów znak laktylacji H3K18 korelował z nieprawidłowymi wzorcami białka supresorowego p53, które często jest zmutowane w OSCC i normalnie hamuje glikolizę oraz replikację DNA. Sugeruje to, że utrata p53 i pętla napędzana mleczanem mogą współdziałać, przyspieszając wczesny rozwój guza.
Co to oznacza dla przyszłych terapii
Podsumowując, badanie pokazuje, że we wczesnych zmianach w jamie ustnej nadmierne spalanie cukru wytwarza mleczan, który nie pozostaje jedynie odpadem — dekoruje histony, włącza TK1, zwiększa budowę DNA i sygnały wzrostu oraz aktywuje cykl napędzany przez Wnt, który z kolei generuje jeszcze więcej mleczanu. Przerwanie tej pętli glikoliza–laktylacja–TK1–β-katenina w dowolnym z jej kluczowych punktów — takich jak glikoliza, laktylacja histonów, TK1, RhoA czy sygnalizacja Wnt — mogłoby dać nowe możliwości zapobiegania przemianie leukoplakii w raka lub leczenia ustalonego OSCC, szczególnie u pacjentów HPV-ujemnych.
Cytowanie: Wang, Y., Geng, Y., Chen, Y. et al. Histone lactylation-driven feedback loop modulates pyrimidine metabolism to promote oral carcinogenesis. Cell Death Dis 17, 316 (2026). https://doi.org/10.1038/s41419-026-08580-w
Słowa kluczowe: rak jamy ustnej, metabolizm guza, laktylacja histonów, synteza pirymidyn, szlak Wnt