Clear Sky Science · zh
异常的钙信号和神经元活动:L271H CACNA1D (Cav1.3) iPSC 神经发育疾病模型
单个基因改变如何在脑发育中引起涟漪效应
基因中的罕见变异可以微妙地改变脑细胞处理电和化学信号的方式。本研究追踪了钙通道基因中的一种变异,该基因与发育迟缓、癫痫和类自闭症表型相关。研究人员将患者的血细胞重编程为干细胞,再分化为培养皿中的微型脑组织和神经元,从而描绘出一个分子微调如何扭曲早期脑发育和神经元活动的路径。
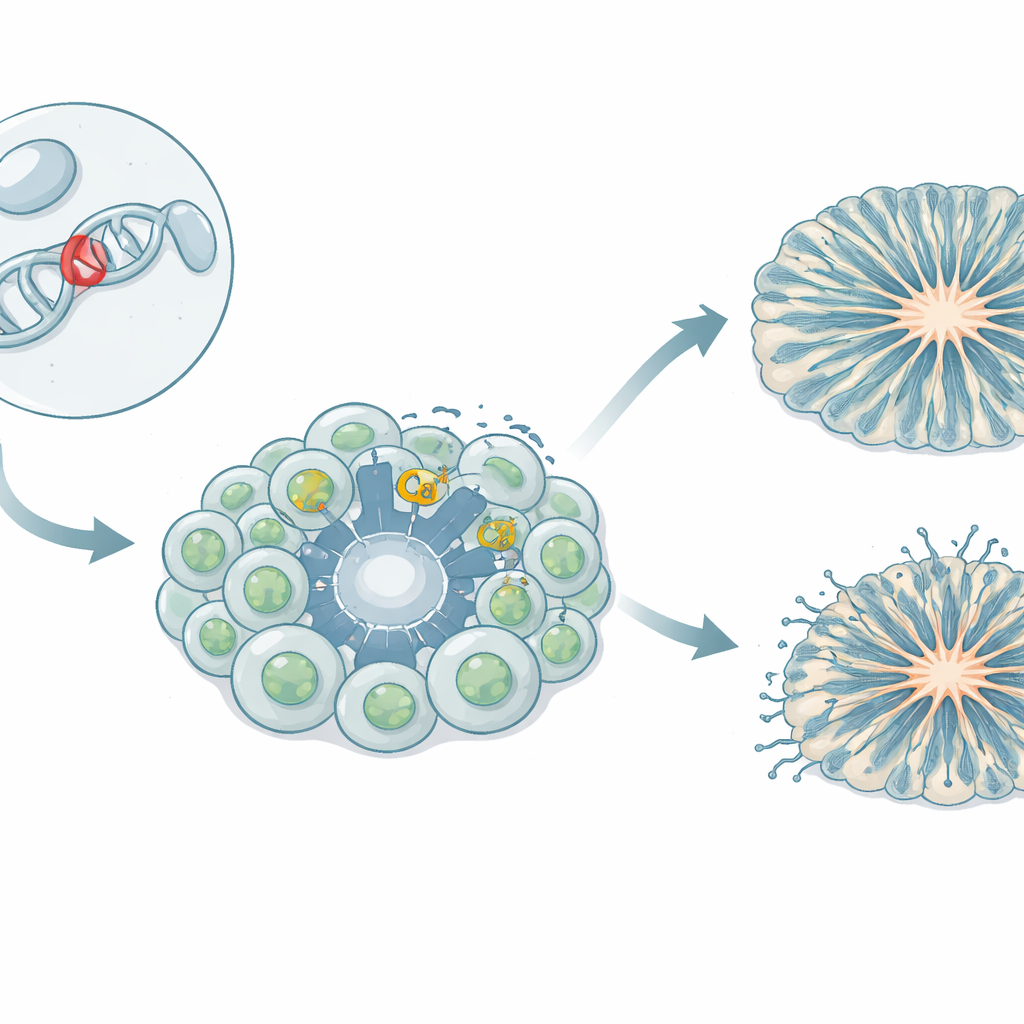
允许钙进入脑细胞的“门卫”
脑细胞依赖受控制的钙离子流入来生长、相互通信并开关基因。位于细胞膜上的专门“门”——电压门控钙通道,在电活动时打开允许钙流入。其中一种称为 Cav1.3 的通道,在大脑和激素分泌组织中都很重要。在若干患者中,Cav1.3 基因的罕见遗传变异与一系列症状相关:激素失衡、肌无力、癫痫、发育迟缓以及自闭谱系特征。本研究中检验的变体 L271H 在非神经细胞中已被证明使通道更易开通,但其对人类脑细胞的影响尚不清楚。
在实验室构建患者特异性的脑细胞
研究团队建立了一个 iPSC 模型:来自携带 L271H 变体女孩的血细胞被重编程为能够形成任何组织的干细胞。这些诱导多能干细胞随后被引导分化为神经祖细胞——产生神经元的早期构建单元——以及与多巴胺信号相关的中脑神经元。研究者还培养了三维皮层类器官,这些“迷你大脑”结构模拟了人类皮层形成的早期阶段。通过将患者来源的细胞与几条来自健康供体的对照系比较,他们能够将变体效应与自然遗传变异区分开来。
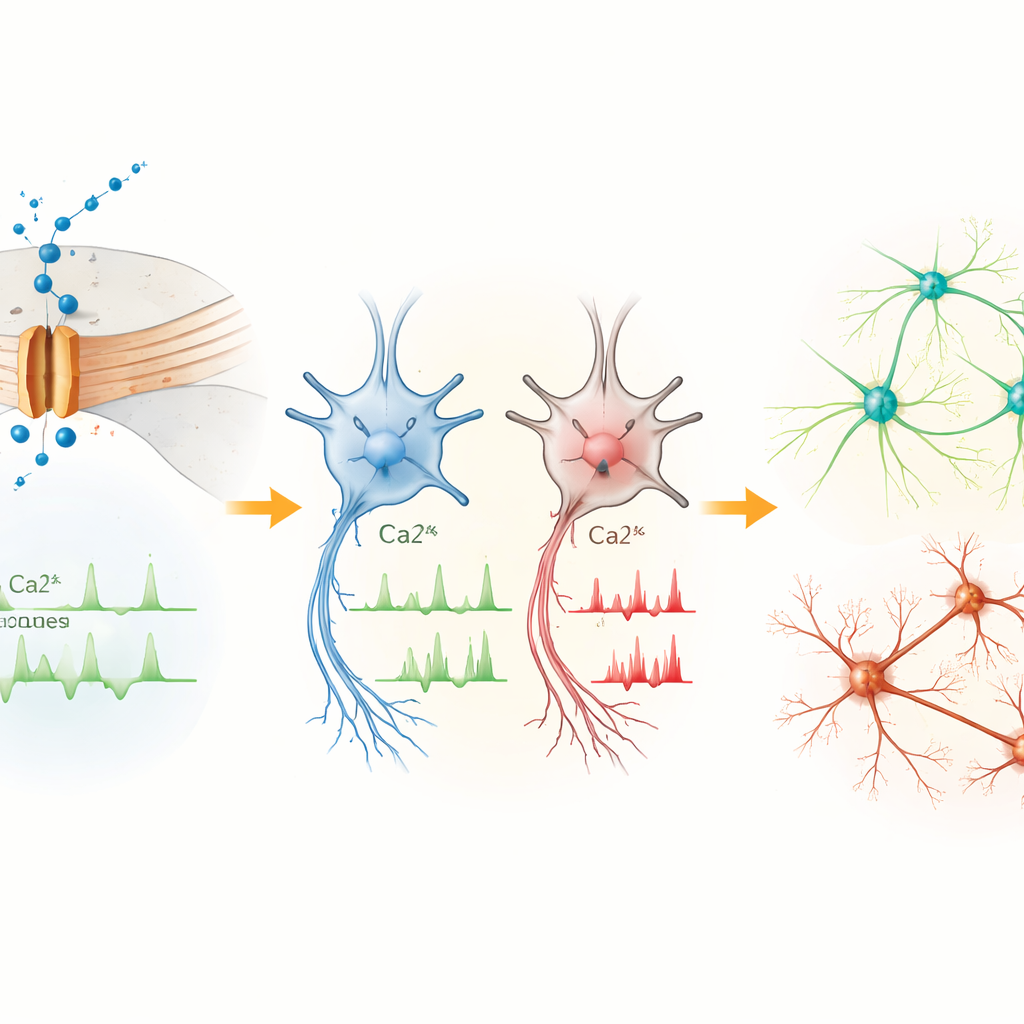
早期细胞信号过强,成熟神经元放电不足
在最早的神经祖细胞中,Cav1.3 是该类钙通道的主要形式。携带 L271H 变体的细胞比对照更频繁地出现自发钙激增,尽管其基本电特性相似。这表明在这一阶段,变体主要干扰细胞内钙平衡,而不是明显改变电冲动的放电。随着细胞分化为中脑神经元,情况发生逆转。尽管另一类钙通道总体上变得更丰富,携带 L271H 的神经元显示更少的钙峰、更去极化的静息电位,并且更难被驱动为重复放电。它们的动作电位幅度更小、上升和下降更慢,表明该变体最终削弱了神经元发送强有力电信号的能力。
生长更快但组织化较差的迷你大脑
在皮层类器官中,L271H 变体对结构产生了显著影响。与对照相比,患者来源的类器官具有更少且更小的类脑室腔——这些环状区域中祖细胞通常按序排列。作为支架并引导新生神经元的放射状胶质细胞分散在组织中,而不是形成整齐的极化层。中间祖细胞和神经元出现得更早但随后下降,这表明祖细胞被促使过早分化。到第 60 天时,总神经元数量赶上了对照,但早期的时序紊乱和组织松散表明这是构建皮层回路蓝图被扰乱,而非完全无法生成神经元。
基因表达向神经发育风险程序倾斜
为了解改变的钙处理如何影响基因调控,团队对不同发育阶段的患者与对照细胞进行了 RNA 测序。干细胞阶段的差异较小,但随着 Cav1.3 表达增加,在祖细胞和神经元中差异扩大。患者细胞中上调或下调的许多基因参与转录调控、脑发育和神经发生。其中若干基因(包括 PTN、MEIS2、POU3F2、CNTN4、CNTNAP2 和 AUTS2)已知与自闭症及相关神经发育状况有关。这些变化表明,通过 Cav1.3 的异常钙流入重塑了那些依赖活动的基因程序,而这些程序指导着脑细胞如何增殖、迁移并建立连接。
对患者和未来疗法的意义
简而言之,这项工作展示了单一钙通道变体如何先过度刺激早期脑细胞、随后使成熟神经元功能不足,同时将与神经发育障碍相关的基因网络推离正常轨道。结果可能是外观上大体正常的大脑,但其电路在发育过程中进程过快且组织不完善。通过在人体细胞和类器官中重现这位患者的突变,该研究提供了一张从分子缺陷到细胞信号、组织结构和基因调控改变的详细路线图。该模型现在为测试针对性药物和基因策略,旨在恢复 Cav1.3 相关通道病的更正常钙信号,提供了平台。
引用: Tisch, M., Geisler, S.M., Gabassi, E. et al. Aberrant calcium signaling and neuronal activity in the L271H CACNA1D (Cav1.3) iPSC model of neurodevelopmental disease. Mol Psychiatry 31, 2927–2940 (2026). https://doi.org/10.1038/s41380-025-03429-8
关键词: 钙通道, 神经发育障碍, 诱导多能干细胞, 脑类器官, 自闭症风险基因