Clear Sky Science · he
תאי איתות סידן וסירי פעילות עצבית חריגים בדגם iPSC של CACNA1D (Cav1.3) L271H במחלות התפתחות עצבית
כאשר שינוי גנטי יחיד מתפשט דרך התפתחות המוח
שינויים נדירים בגנים יכולים לשנות בעדינות את האופן שבו תאי המוח מעבדים אותות חשמליים וכימיים. המחקר הזה עוקב אחרי שינוי כזה בגן לתעלת סידן המקושרת לעיכוב התפתחותי, לפרכוסים ולתסמינים הדומים לאוטיזם. על ידי הפיכת תאי דם של מטופלת לתאים פלוריפוטנטיים ובהמשך לרקמות מוח ומוחיות נוירונים במבחנה, החוקרים מציירים מפת כיצד תיקון מולקולרי קטן עלול לעוות את התפתחות המוח המוקדמת ואת פעילות הנוירונים.
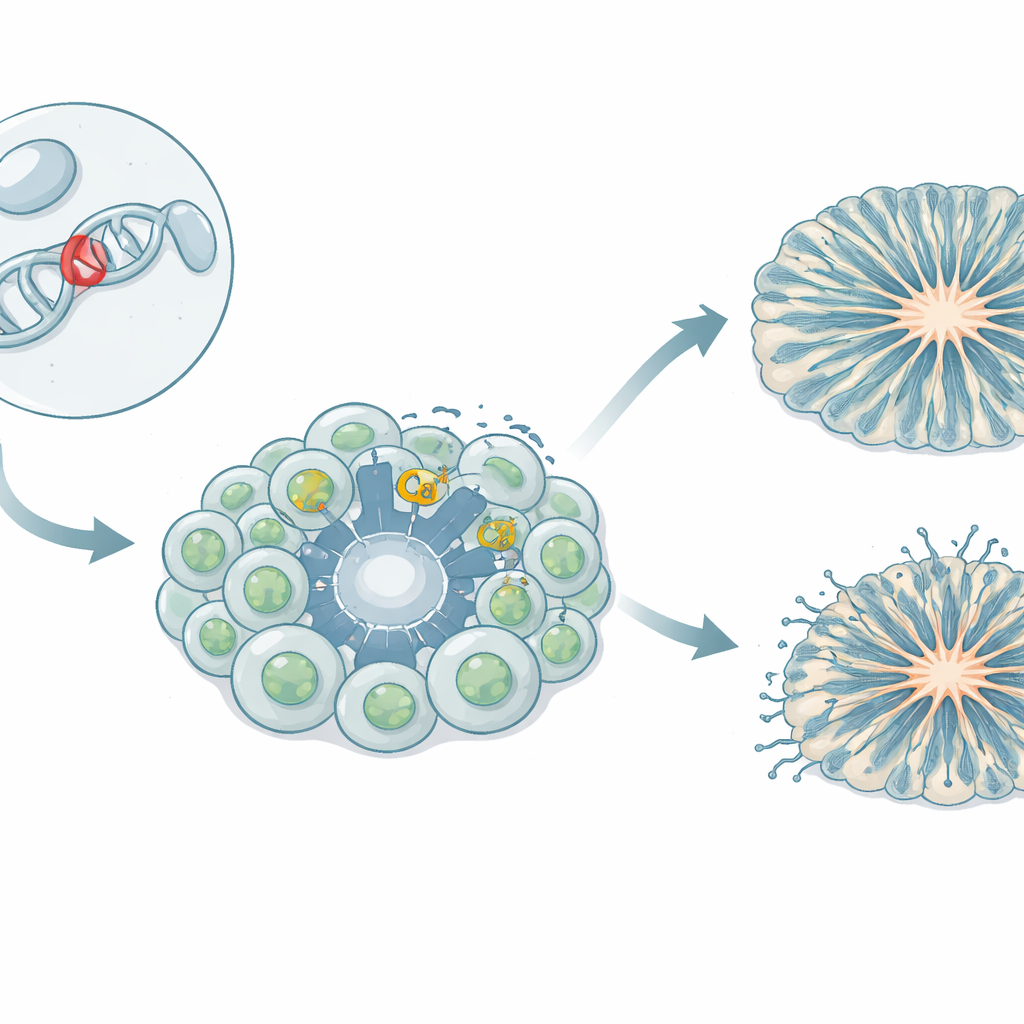
שומרי הסף שמאפשרים לסידן להיכנס לתאי המוח
תאי המוח נשענים על זרם מבוקר של יוני סידן לצורך גדילה, תקשורת הדדית והפעלת גנים. "שייחים" מיוחדים בממברנת התא, הנקראים תעלות סידן תלויות מתח, נפתחים במהלך פעילות חשמלית ומאפשרים לסידן לזרום פנימה. אחת שתיקות אלו, המכונה Cav1.3, חשובה באיברים רבים, כולל המוח ורקמות המייצרות הורמונים. במספר מטופלים זוהו שינויים תורשתיים נדירים בגן Cav1.3 שקושרו למגוון סימפטומים: חוסר איזון הורמונלי, חולשת שרירים, פרכוסים, עיכוב בהתפתחות ותכונות על הספקטרום האוטיסטי. הווריאנט שנחקר כאן, הקרוי L271H, הראה בתאים שאינם נוירונליים כי הוא מקל על פתיחת התעלה, אך השפעתו על תאי מוח אנושיים הייתה לא ידועה.
בניית תאי מוח ספציפיים למטופל במעבדה
הצוות יצר מודל iPSC, שבו תאי דם של ילדה הנושאת את הווריאנט L271H תוכנתו מחדש לתאי גזע שיכולים ליצור כל רקמה. תאי גזע פלוריפוטנטיים אלו הונחו להפוך לתאי אב נוירליים—אבני הבניין המוקדמות שממנו יווצרו הנוירונים—ולנוירונים של המוח האמצעי הקשורים לסיגנלי הדופאמין. החוקרים גם גידלו אורגנואידים קורטיקליים תלת־ממדיים, "מיני־מוחות" שמחקים שלבי התהוות מוקדמים של הקורטקס האנושי. בהשוואה לתאי ביקורת ממספר תורמים בריאים, הם יכלו להפריד את השפעות הווריאנט מהשונות הגנטית הטבעית.
תאים מוקדמים משדרים יותר מדי, נוירונים בוגרים יורים מעט מדי
בתאי האב הנוירליים המוקדמים ביותר, תעלת Cav1.3 הייתה הצורה הדומיננטית של שער סידן זה. תאים הנושאים את הווריאנט L271H הראו גליצות סידן ספונטניות תכופות יותר מאשר הביקורות, אף על פי שתכונותיהם החשמליות הבסיסיות היו דומות. זה מרמז שבשלב זה הווריאנט משבש בעיקר את מאזן הסידן בתוך התא במקום לגרום לירי חשמלי ברור. כשהתאים בגרו לנוירונים של המוח האמצעי התמונה התהפכה. אף כי סוג אחר של תעלת סידן הפך לשכיח יותר, נוירונים עם הווריאנט L271H הראו פחות התפרצויות סידן, מצב מנוחה יותר דפולריזלי והיו קשים יותר להניע לירי חוזר. פוטנציאלי הפעולה שלהם היו קטנים יותר ואיטי עלייה וירידה, מה שמצביע שהווריאנט מדכא בסופו של דבר את יכולת הנוירונים לשדר אותות חשמליים חזקים.
מיני־מוחות שגדלים מהר יותר אך מסתדרים רע
באורגנואידים קורטיקליים, לווריאנט L271H היה חותם מבני בולט. בהשוואה לביקורות, אורגנואידים ממקור המטופלת הכילו פחות חללים דמויי חדרונים והם היו קטנים יותר—אזורים טבעתיים שבהם תאי אב נוטים ליישר את עצמם בצורה מסודרת. תאי גליה רדיאליים, המשמשים כשלד ומנחים לנוירונים חדשים, היו מפוזרים ברקמה במקום להיווצר בשכבות מקוטבות וסדורות. תאי אב בינוניים ונוירונים הופיעו מוקדם יותר ואז ירדו מהר יותר, מה שמרמז שתאי האב הופרזו להתמיין מהר מדי. עד יום 60 מספר הנוירונים הכולל התאזן, אבל התזמון המוקדם והשיבוש בארגון מצביעים על תבנית בנייה של מעגלי הקורטקס שהופרעה יותר מאשר כישלון מוחלט בייצור נוירונים.
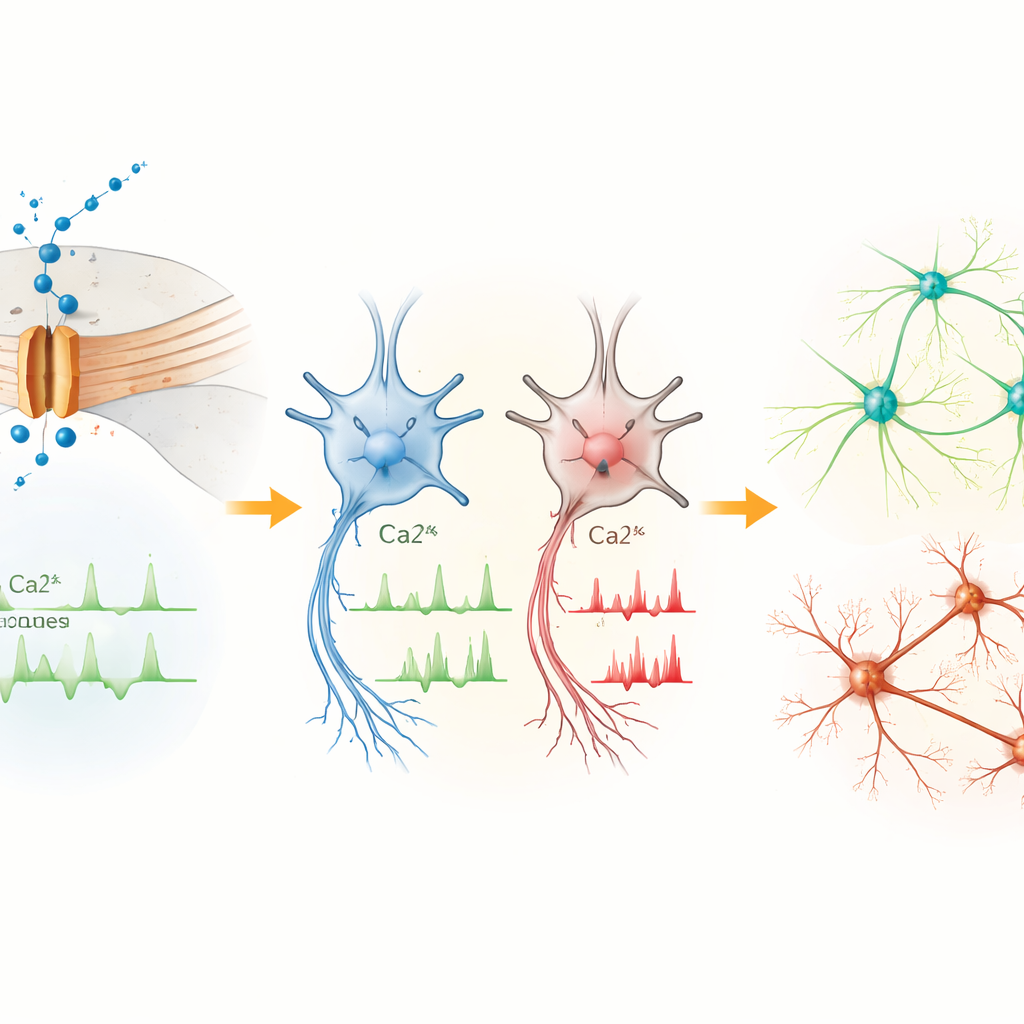
פעילות גנטית נעה לכיוון תוכניות סיכון להתפתחות עצבית
כדי להבין כיצד שינוי בטיפול בסידן משפיע על בקרה גנטית, הצוות רצף RNA מתאים ומשורי ביקורת בשלביה שונים. ההבדלים היו מתונים בתאי הגזע אך גדלו בתאי האב ובנוירונים ככל שביטוי Cav1.3 עלה. רבים מהגנים שהופעלו או הועמסו בתאי המטופלת מעורבים בבקרת שעתוק, בהתפתחות המוח ובהניאוגנזה. כמה מהם, כולל PTN, MEIS2, POU3F2, CNTN4, CNTNAP2 ו‑AUTS2, מוכרים כגני סיכון לאוטיזם ומצבים נוירו‑התפתחותיים קשורים. השינויים הללו מעידים שכניסה חריגה של סידן דרך Cav1.3 מעצבת מחדש תוכניות גנטיות התלויות פעילות שמנחות כיצד תאי המוח מתחלקים, נודדים ומתחברים זה לזה.
מה משמעות הדבר עבור מטופלים וטיפולים עתידיים
בקצרה, עבודה זו מראה כיצד וריאנט יחיד בתעלת סידן יכול תחילה להגביר פעילות בתאי מוח מוקדמים, ואז להותיר נוירונים בוגרים מוחלשים, בעוד בו‑זמנית מגלגל רשתות גנטיות המקושרות להפרעות התפתחותיות מהטרף. התוצאה היא מוח שעשוי להיראות תקין בחזית החיצונית אך נבנה ממעגלים שהתפתחו מהר מדי ואורגנו באופן בלתי מושלם. על ידי שיחזור המוטציה של המטופלת בתאים אנושיים ובאורגנואידים, המחקר מספק מפת דרכים מפורטת שמקשרת פגם מולקולרי לשינוי בסיגנל תא, בארכיטקטורת רקמה ובבקרת גנים. המודל הזה מציע עכשיו פלטפורמה לבדוק תרופות ממוקדות ואסטרטגיות גנטיות שמטרתן לשחזר איתות סידן תקין בהפרעות תעלתיות הקשורות ל‑Cav1.3.
ציטוט: Tisch, M., Geisler, S.M., Gabassi, E. et al. Aberrant calcium signaling and neuronal activity in the L271H CACNA1D (Cav1.3) iPSC model of neurodevelopmental disease. Mol Psychiatry 31, 2927–2940 (2026). https://doi.org/10.1038/s41380-025-03429-8
מילות מפתח: תעלות סידן, הפרעות בהתפתחות המוח, תאי גזע פלוריפונטיים מוצאים (iPSC), אורגנואידים מוחיים, גנים בסיכון לאוטיזם