Clear Sky Science · tr
L271H CACNA1D (Cav1.3) iPSC modelinde anormal kalsiyum sinyallemesi ve nöronal aktivite — nörogelişimsel hastalık modeli
Tek Bir Gen Değişikliğinin Beyin Gelişiminde Yarattığı Dalga
Nadir gen değişiklikleri, beyin hücrelerinin elektriksel ve kimyasal sinyalleri işlemesini ince şekilde değiştirebilir. Bu çalışma, gelişim geriliği, nöbetler ve otizm benzeri semptomlarla ilişkilendirilmiş bir kalsiyum kanalı genindeki böyle bir değişikliği izliyor. Hastanın kan hücrelerini kök hücrelere, ardından kültürde küçük beyin dokuları ve nöronlara dönüştürerek araştırmacılar, moleküler düzeydeki küçük bir değişikliğin erken beyin gelişimini ve nöronal aktiviteyi nasıl bozabildiğini haritalıyor.
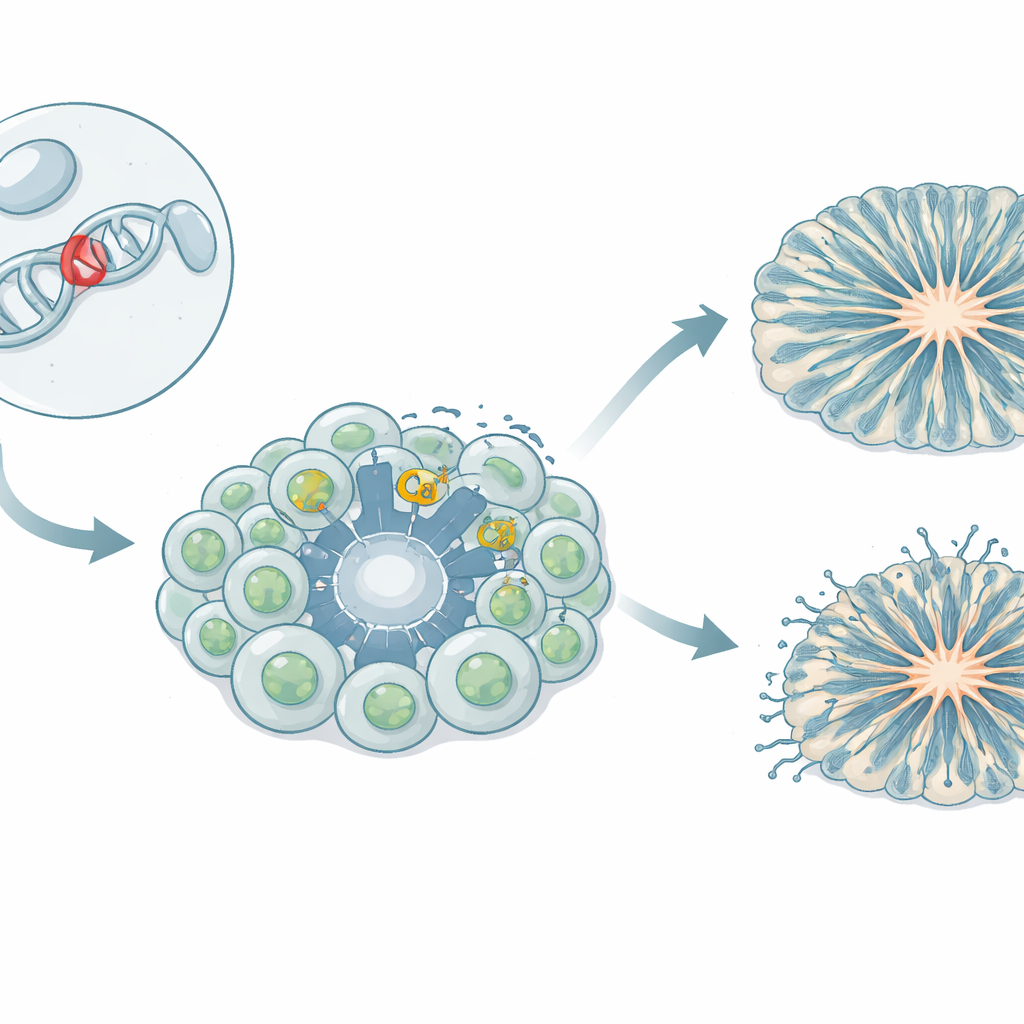
Beyin Hücrelerine Kalsiyum Aldıran Kapı Bekçileri
Beyin hücreleri, büyümek, birbirleriyle iletişim kurmak ve genleri açıp kapamak için kontrollü bir kalsiyum iyonu akışına güvenir. Hücre zarındaki özelleşmiş “kapılar”, yani voltaja duyarlı kalsiyum kanalları, elektriksel aktivite sırasında açılarak kalsiyum girişine izin verir. Cav1.3 olarak bilinen bu kapılardan biri beyin ve hormon üreten dokular da dahil olmak üzere birçok organda önem taşır. Birkaç hastada Cav1.3 genindeki nadir kalıtsal değişiklikler hormon dengesizlikleri, kas zayıflığı, nöbetler, gelişim gecikmesi ve otizm spektrumuna ait özelliklerin karışımıyla ilişkilendirilmiştir. Burada incelenen L271H varyantı, nöronal olmayan hücrelerde kanalın daha kolay açılmasına neden olduğu gösterilmişti, ancak insan beyin hücrelerindeki etkisi bilinmiyordu.
Hastaya Özgü Beyin Hücrelerini Laboratuvarda İnşa Etmek
Araştırma ekibi, L271H varyantını taşıyan bir kızın kan hücrelerini her türlü doku oluşturabilen kök hücrelere yeniden programlayarak bir iPSC modeli oluşturdu. Bu indüklenmiş pluripotent kök hücreler daha sonra nöral progenitör hücrelere—ileride nöronları üretecek erken yapı taşlarına—ve dopamin sinyalizasyonuyla ilişkili orta beyin nöronlarına yönlendirildi. Araştırmacılar ayrıca insan korteksinin erken aşamalarını taklit eden üç boyutlu kortikal organoidler, yani küçük “mini-beyin” yapıları da yetiştirdiler. Hasta kaynaklı hücreleri sağlıklı donörlerden alınan birkaç kontrol hattıyla karşılaştırarak, varyantın etkilerini doğal genetik farklılıktan ayırabildiler.
Erken Hücreler Fazla Sinyal Veriyor, Olgun Nöronlar Yetersiz Ateşleniyor
En erken nöral progenitörlerde Cav1.3 kanalı bu kalsiyum kapısının baskın formuydu. L271H varyantını taşıyan hücreler, temel elektriksel özellikleri benzer olmasına rağmen kontrollere göre daha sık spontan kalsiyum dalgalanmaları gösterdi. Bu, bu aşamada varyantın esas olarak hücre içi kalsiyum dengesini bozduğunu, bariz elektriksel atım ateşlenmesi yerine içsel kalsiyum dinamiklerini etkilediğini düşündürür. Hücreler orta beyin nöronlarına olgunlaştıkça tablo tersine döndü. Başka bir kalsiyum kanal türü genel olarak daha bol hale gelmiş olsa da, L271H varyantlı nöronlar daha az kalsiyum tepe gösterdi, daha depolarize bir dinlenme durumuna sahipti ve tekrarlı ateşlemeye zorlamak daha zordu. Aksiyon potansiyelleri daha küçük, yükseliş ve düşüşleri daha yavaştı; bu da varyantın nihayetinde nöronların güçlü elektrik sinyalleri gönderme kapasitesini azaltığını gösteriyor.
Daha Hızlı Büyüyen ama Kötü Örgütlenen Mini Beyinler
Kortikal organoidlerde L271H varyantı yapı üzerinde belirgin bir iz bıraktı. Kontrollere kıyasla hasta kaynaklı organoidlerde daha az ve daha küçük ventrikül benzeri boşluklar vardı—progenitör hücrelerin normalde düzenli şekilde sıralandığı halka biçimli bölgeler. Yeni doğan nöronlara iskeletlik hizmeti veren ve onları yönlendiren radyal glia hücreleri doku boyunca dağınık haldeydi; düzgün, kutuplaşmış katmanlar oluşturmadılar. Ara ara progenitör hücreleri ve nöronlar daha erken ortaya çıkıp sonra daha çabuk azaldı; bu da progenitörlerin çok hızlı farklılaşmaya itildiğini gösteriyor. 60. günde toplam nöron sayısı yakalasa da, erken zamanlamadaki ve örgütlenmedeki bozulma kortikal devrelerin nasıl kurulduğuna dair bozulmuş bir planı işaret ediyor; yani nöron yapımında mutlak bir başarısızlıktan ziyade yanlış zamanlanma ve düzensizlik söz konusu.
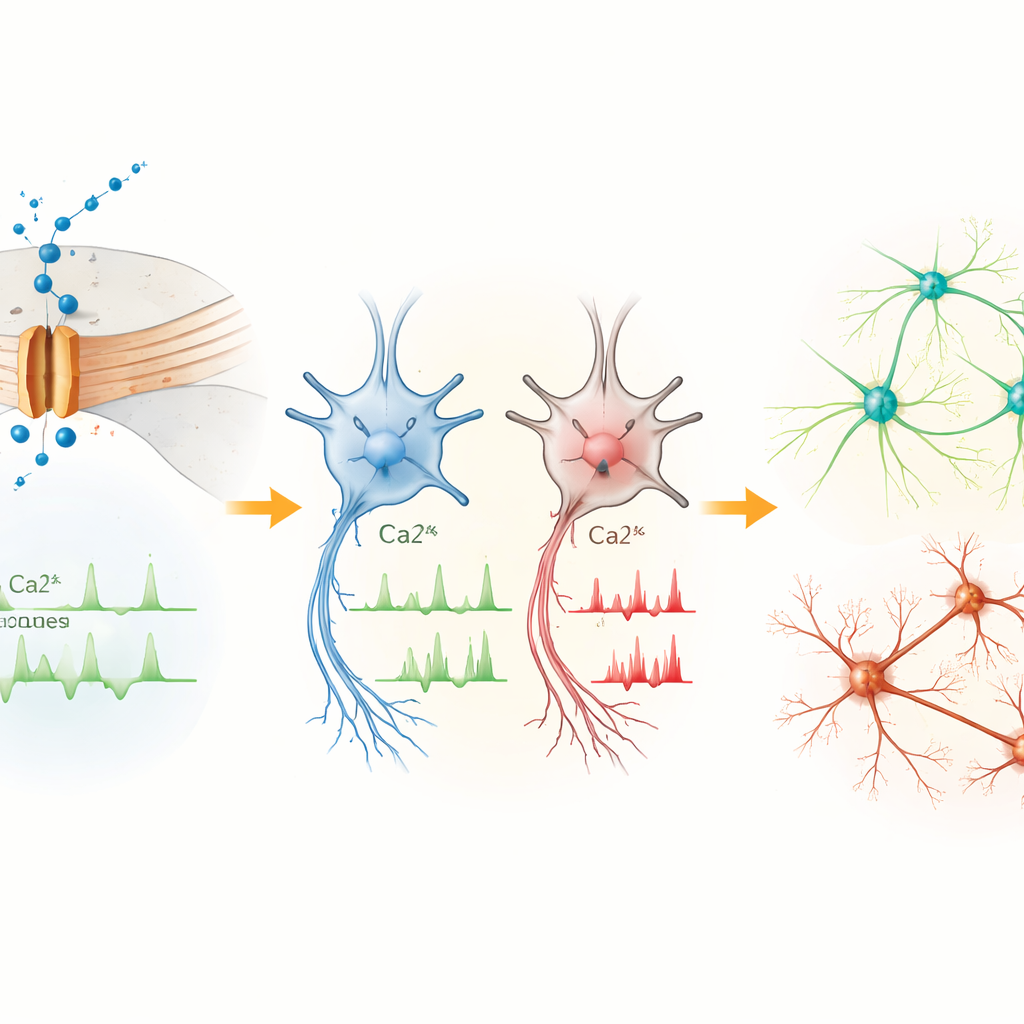
Gen Aktivitesi Nörogelişimsel Risk Programlarına Kayıyor
Değişmiş kalsiyum yönetiminin gen kontrolüne nasıl etki ettiğini anlamak için ekip, hasta ve kontrol hücrelerinden farklı aşamalarda RNA dizilimi yaptı. KöK hücrelerdeki farklılıklar ılımlıydı ancak Cav1.3 ekspresyonu arttıkça progenitörlerde ve nöronlarda daha da belirginleşti. Hasta hücrelerinde yukarı veya aşağı yönlü değişen birçok gen transkripsiyon kontrolü, beyin gelişimi ve nörogenez ile ilgiliydi. PTN, MEIS2, POU3F2, CNTN4, CNTNAP2 ve AUTS2 dahil birkaç gen, otizm ve ilişkili nörogelişimsel durumlar için bilinen risk genleri arasında yer alıyor. Bu değişiklikler, Cav1.3 aracılığıyla anormal kalsiyum girişinin, beyin hücrelerinin çoğalma, göç ve bağlantı kurma biçimlerini yönlendiren aktivite-bağımlı gen programlarını yeniden şekillendirdiğini öne sürüyor.
Bu Hastalar ve Gelecekteki Tedaviler İçin Ne Anlama Geliyor
Basitçe söylemek gerekirse, bu çalışma tek bir kalsiyum kanal varyantının önce erken beyin hücrelerini aşırı uyarmasına, sonra olgun nöronları güçsüz bırakmasına ve aynı zamanda nörogelişimsel bozukluklarla ilişkili gen ağlarını yolundan çıkarma eğilimine nasıl sahip olduğunu gösteriyor. Sonuç, dışarıdan büyük ölçüde normal görünen ancak çok hızlı gelişmiş ve kusurlu şekilde örgütlenmiş devrelerden oluşan bir beyin olabilir. Bu hastanın mutasyonunu insan hücreleri ve organoidlerde yeniden yaratarak çalışma, moleküler bir kusuru hücre sinyallemesi, doku mimarisi ve gen regülasyonundaki değişikliklere bağlayan ayrıntılı bir yol haritası sunuyor. Bu model artık Cav1.3 ilişkili kanalopatilerde daha normal kalsiyum sinyallemesini geri kazanmaya yönelik hedefe yönelik ilaçları ve genetik stratejileri test etmek için bir platform sağlıyor.
Atıf: Tisch, M., Geisler, S.M., Gabassi, E. et al. Aberrant calcium signaling and neuronal activity in the L271H CACNA1D (Cav1.3) iPSC model of neurodevelopmental disease. Mol Psychiatry 31, 2927–2940 (2026). https://doi.org/10.1038/s41380-025-03429-8
Anahtar kelimeler: kalsiyum kanalları, nörogelişimsel bozukluklar, indüklenmiş pluripotent kök hücreler, beyin organoidleri, otizm risk genleri