Clear Sky Science · nl
Abnormale calciumsignalering en neuronale activiteit in het L271H CACNA1D (Cav1.3) iPSC-model van neuroontwikkelingsziekten
Wanneer één genverandering golven slaat door de hersenontwikkeling
Zeldzame wijzigingen in genen kunnen subtiel veranderen hoe hersencellen elektrische en chemische signalen verwerken. Deze studie volgt zo’n wijziging in een calciumedraalingsgen dat wordt gekoppeld aan ontwikkelingsachterstand, aanvallen en autismeachtige symptomen. Door bloedcellen van een patiënt om te zetten in stamcellen en vervolgens in miniatuurhersentjes en neuronen in een schaal, brengen de onderzoekers in kaart hoe een kleine moleculaire aanpassing de vroege hersenontwikkeling en neuronale activiteit kan vervormen.
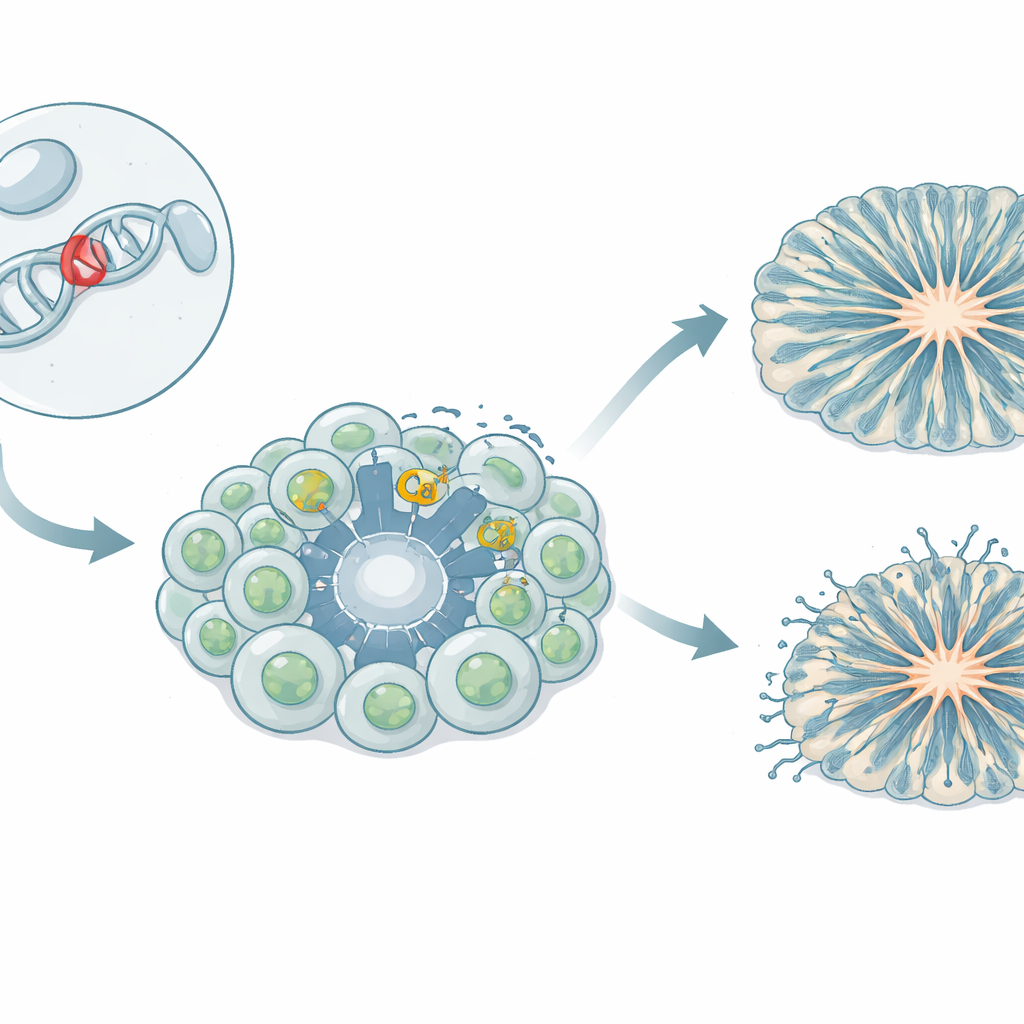
Poortwachters die calcium in hersencellen laten
Hersencellen vertrouwen op een gecontroleerde instroom van calciumionen om te groeien, met elkaar te communiceren en genen aan of uit te zetten. Gespecialiseerde “poorten” in het celmembraan, zogenaamde spanningsafhankelijke calciumkanalen, openen tijdens elektrische activiteit en laten calcium naar binnen stromen. Eén van deze poorten, bekend als Cav1.3, is belangrijk in veel organen, waaronder de hersenen en hormoonproducerende weefsels. Bij meerdere patiënten zijn zeldzame erfelijke veranderingen in het Cav1.3-gen gekoppeld aan een scala aan symptomen: hormonale disbalans, spierzwakte, aanvallen, vertraagde ontwikkeling en kenmerken op het autismespectrum. De hier bestudeerde variant, L271H, bleek in niet‑neuronaal cellen de kanaalopening te vergemakkelijken, maar het effect op menselijke hersencellen was onduidelijk.
Het maken van patiëntspecifieke hersencellen in het laboratorium
Het team maakte een iPSC-model waarin bloedcellen van een meisje met de L271H-variant werden herprogrammeerd tot stamcellen die elk weefsel kunnen vormen. Deze geïnduceerde pluripotente stamcellen werden vervolgens gestuurd naar neurale voorlopercellen—de vroege bouwstenen die later neuronen voortbrengen—en naar middenhersenneuronen die betrokken zijn bij dopaminesignalering. De onderzoekers kweekten ook driedimensionale corticale organoïden, kleine “mini‑hersenen” die vroege stadia van menselijke cortexvorming nabootsen. Door patiëntafgeleide cellen te vergelijken met meerdere controles van gezonde donoren, konden ze de effecten van de variant scheiden van natuurlijke genetische variatie.
Vroege cellen signaleren te veel, volwassen neuronen vuren te weinig
In de vroegste neurale voorlopercellen was het Cav1.3-kanaal de dominante vorm van deze calciumpoort. Cellen met de L271H-variant vertoonden vaker spontane calciuminvloeden dan controles, hoewel hun basale elektrische eigenschappen vergelijkbaar waren. Dit suggereert dat de variant in dit stadium vooral de calciumbalans binnenin de cel verstoort in plaats van duidelijk verhoogde elektrische ontladingen. Naarmate cellen uitrijpten tot middenhersenneuronen, keerde het beeld om. Hoewel een ander type calciumkanaal in het algemeen meer aanwezig werd, lieten neuronen met de L271H-variant minder calciumpieken zien, een meer gedepolariseerde rusttoestand en waren ze moeilijker in herhaald vuren te brengen. Hun actiepotentialen waren kleiner en langzamer in opkomst en verval, wat aangeeft dat de variant uiteindelijk de capaciteit van neuronen om robuuste elektrische signalen te sturen dempt.
Mini‑hersenen die sneller groeien maar slecht organiseren
In corticale organoïden liet de L271H-variant een sterke invloed op de structuur zien. Vergeleken met controles hadden patiëntafgeleide organoïden minder en kleinere ventrikelachtige holtes—ringvormige zones waar voorlopercellen normaal netjes op een rij liggen. Radiale gliacellen, die fungeren als steigers en pasgeboren neuronen geleiden, lagen verspreid door het weefsel in plaats van in nette, gepolariseerde lagen. Intermediaire voorlopercellen en neuronen verschenen eerder en namen vervolgens sneller af, wat suggereert dat voorlopercellen te snel tot differentiatie werden aangespoord. Na 60 dagen haalden de totale aantallen neuronen weer bij, maar de vroege verkeerde timing en desorganisatie wijzen op een verstoord bouwplan voor corticale circuits in plaats van een absolute fout in het maken van neuronen.
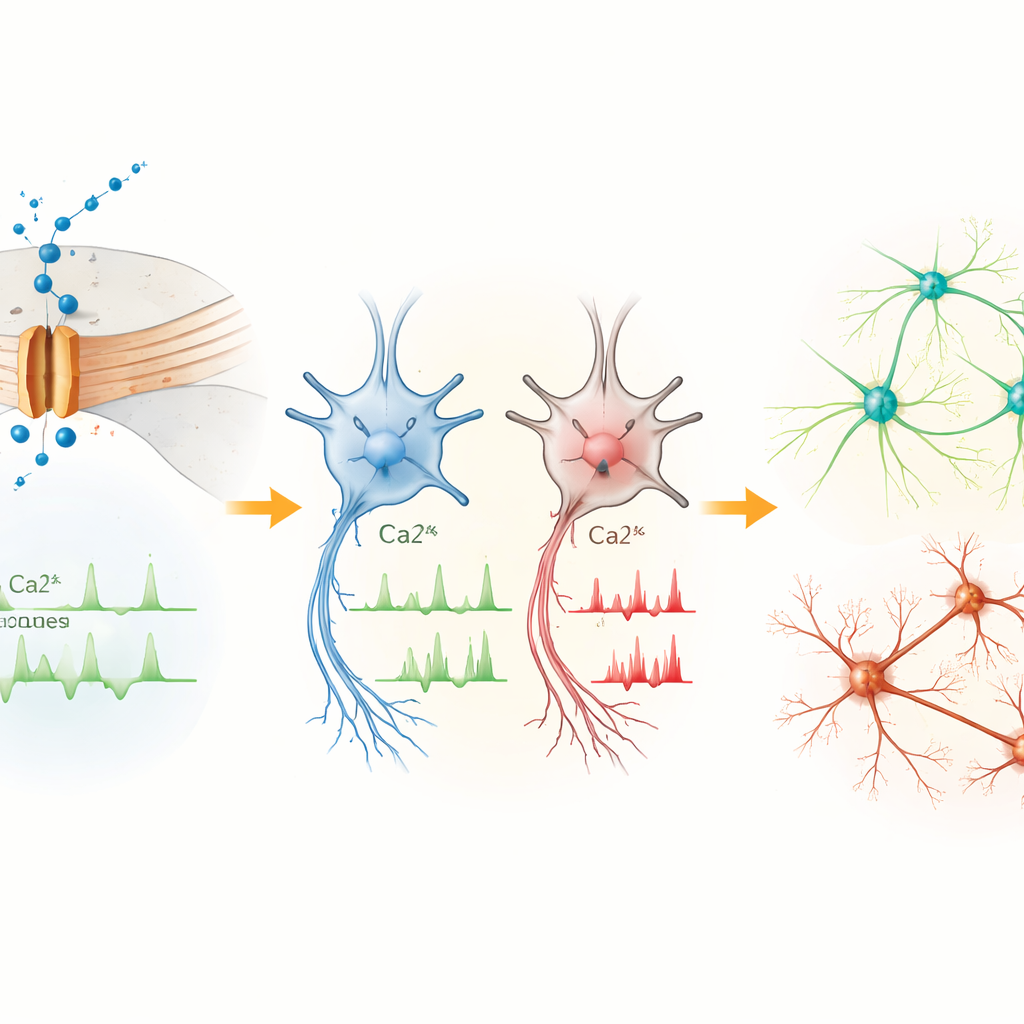
Genactiviteit verschuift richting programma’s met neuro‑ontwikkelingsrisico
Om te begrijpen hoe veranderde calciuminstroming de genregulatie beïnvloedt, sequentieerden de onderzoekers RNA van patiënt- en controlecellen in verschillende stadia. De verschillen waren bescheiden in stamcellen maar werden groter in voorlopers en neuronen naarmate de Cav1.3-expressie toenam. Veel genen die in patiëntcellen omhoog- of omlaagreguleerden zijn betrokken bij transcriptieregulatie, hersenontwikkeling en neurogenese. Verschillende daarvan, waaronder PTN, MEIS2, POU3F2, CNTN4, CNTNAP2 en AUTS2, zijn bekende risicogenen voor autisme en verwante neuro‑ontwikkelingsaandoeningen. Deze veranderingen suggereren dat abnormale calciuminstroming via Cav1.3 activiteit-afhankelijke genprogramma’s herschikt die sturen hoe hersencellen prolifereren, migreren en met elkaar verbinden.
Wat dit betekent voor patiënten en toekomstige therapieën
Kort gezegd laat dit werk zien hoe een enkele variant in een calciumkanaal vroege hersencellen eerst kan overstimuleren en later volwassen neuronen kan verzwakken, terwijl het tegelijkertijd gennetwerken die met neuroontwikkelingsstoornissen geassocieerd zijn, uit koers duwt. Het resultaat is een brein dat er van buiten grotendeels normaal uit kan zien, maar is opgebouwd uit circuits die te snel ontwikkelden en onvolmaakt georganiseerd zijn. Door de mutatie van deze patiënt na te bootsen in menselijke cellen en organoïden, biedt de studie een gedetailleerde routekaart die een moleculair defect verbindt met veranderde celsignaleringspatronen, weefselarchitectuur en genregulatie. Dit model biedt nu een platform om gerichte geneesmiddelen en genetische strategieën te testen die erop zijn gericht een meer normale calciumsignalering in Cav1.3‑gerelateerde channelopathieën te herstellen.
Bronvermelding: Tisch, M., Geisler, S.M., Gabassi, E. et al. Aberrant calcium signaling and neuronal activity in the L271H CACNA1D (Cav1.3) iPSC model of neurodevelopmental disease. Mol Psychiatry 31, 2927–2940 (2026). https://doi.org/10.1038/s41380-025-03429-8
Trefwoorden: calciumkanalen, neuroontwikkelingsstoornissen, geïnduceerde pluripotente stamcellen, hersenorganoïden, autisme-risicogenen