Clear Sky Science · de
Abnorme Kalziumsignalgebung und neuronale Aktivität im L271H CACNA1D (Cav1.3) iPSC-Modell neuroentwicklungsbedingter Erkrankungen
Wenn eine einzige Genveränderung die Gehirnentwicklung durchdringt
Seltener Varianten in Genen können subtil verändern, wie Gehirnzellen elektrische und chemische Signale verarbeiten. Diese Studie verfolgt eine solche Veränderung in einem Kalziumkanalgen, das mit Entwicklungsverzögerung, Anfällen und autismusähnlichen Symptomen in Verbindung gebracht wird. Indem sie die Blutzellen einer Patientin in Stammzellen und daraus in miniaturisierte Gehirngewebe und Neuronen im Reagenzglas zurückverwandelten, kartieren die Forschenden, wie eine winzige molekulare Verschiebung die frühe Hirnentwicklung und neuronale Aktivität verzerren kann.
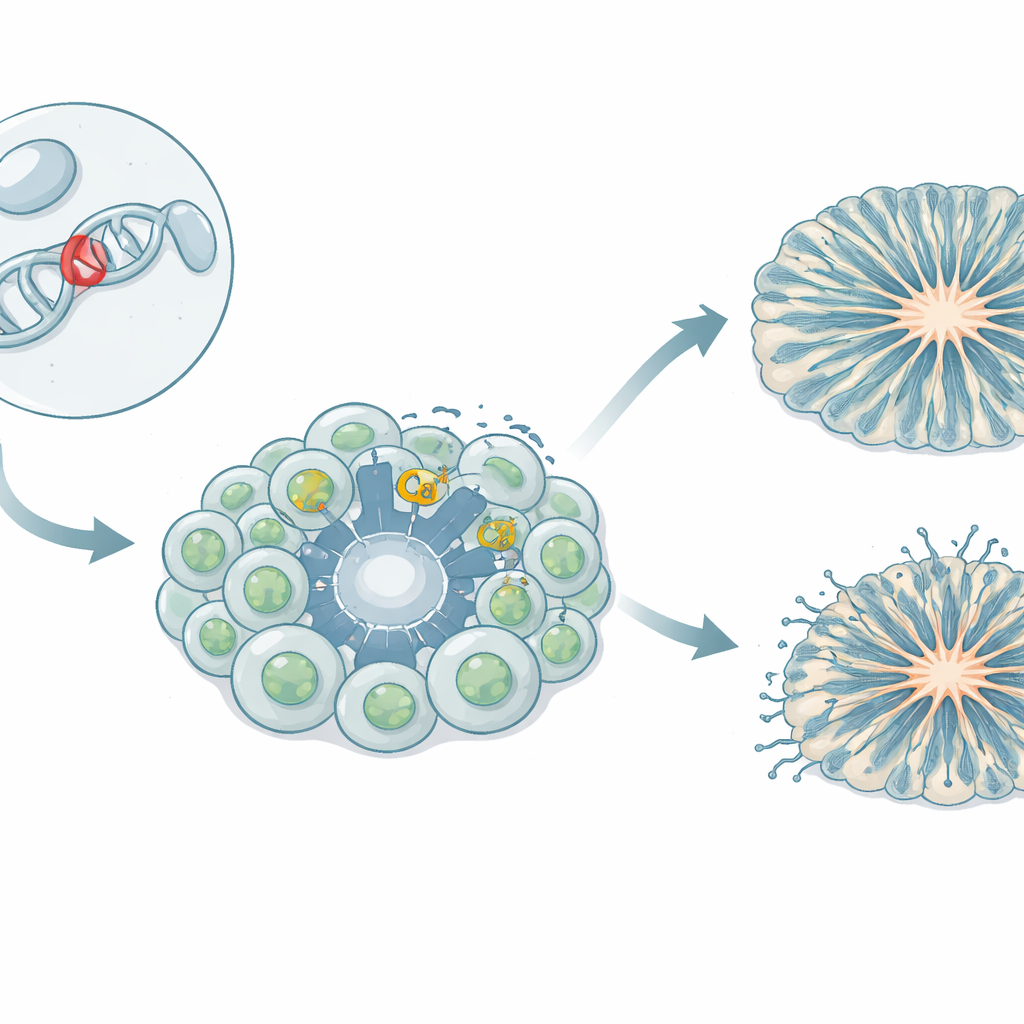
Wächter, die Kalzium in Gehirnzellen lassen
Gehirnzellen sind auf einen kontrollierten Einstrom von Kalziumionen angewiesen, um zu wachsen, miteinander zu kommunizieren und Gene an- und auszuschalten. Spezialisierte „Tore“ in der Zellmembran, die spannungsabhängigen Kalziumkanäle, öffnen sich bei elektrischer Aktivität und lassen Kalzium einströmen. Ein solcher Kanal, bekannt als Cav1.3, ist in vielen Organen wichtig, darunter im Gehirn und in hormonproduzierenden Geweben. Bei mehreren Patienten wurden seltene vererbte Varianten im Cav1.3-Gen mit einer Mischung aus Symptomen in Verbindung gebracht: Hormonstörungen, Muskelschwäche, Anfälle, Entwicklungsverzögerung und Merkmale des Autismus-Spektrums. Die hier untersuchte Variante, L271H, hatte in nicht-neuronalen Zellen gezeigt, dass der Kanal leichter öffnet, doch ihre Auswirkungen auf menschliche Gehirnzellen waren bislang unbekannt.
Patientenspezifische Gehirnzellen im Labor erzeugen
Das Team entwickelte ein iPSC-Modell, bei dem Blutzellen eines Mädchens mit der L271H-Variante zu Stammzellen umprogrammiert wurden, die jede Gewebeart bilden können. Diese induzierten pluripotenten Stammzellen wurden dann in neuronale Vorläuferzellen gelenkt – die frühen Bausteine, die später Neurone erzeugen – sowie in Mittelhirnneurone, die mit Dopamin-Signalen in Verbindung stehen. Die Forschenden züchteten außerdem dreidimensionale kortikale Organoide, winzige „Mini-Gehirn“-Strukturen, die frühe Stadien der menschlichen Kortexbildung nachahmen. Durch den Vergleich patientenabgeleiteter Zellen mit mehreren Kontrolllinien gesunder Spender konnten sie die Effekte der Variante von natürlicher genetischer Variabilität unterscheiden.
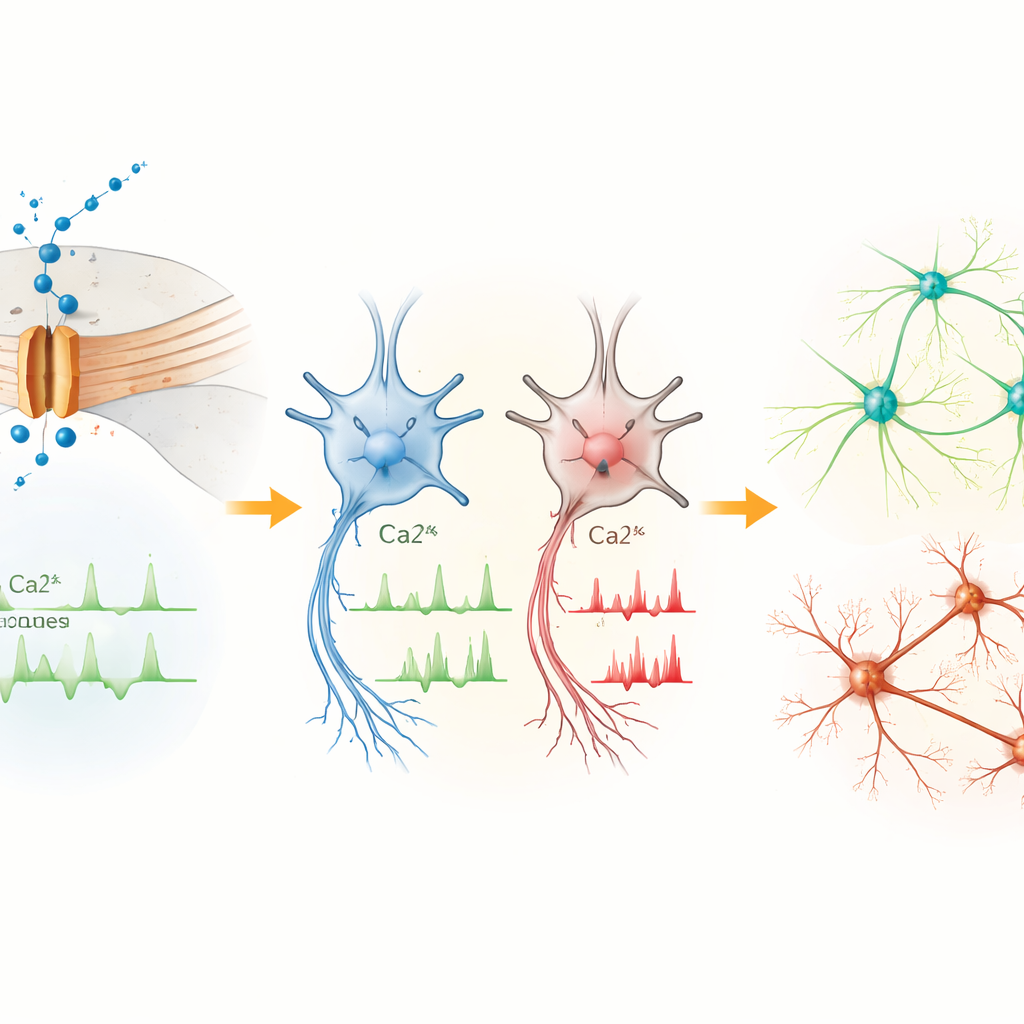
Frühe Zellen signalisieren zu viel, reife Neurone feuern zu wenig
In den frühesten neuronalen Vorläufern war der Cav1.3-Kanal die dominante Form dieses Kalziumtores. Zellen mit der L271H-Variante zeigten häufigere spontane Kalziumanstiege als Kontrollen, obwohl ihre grundlegenden elektrischen Eigenschaften ähnlich waren. Das deutet darauf hin, dass die Variante in diesem Stadium vor allem das Kalziumgleichgewicht innerhalb der Zelle stört, statt offensichtliche elektrische Entladungen auszulösen. Mit der Reifung zu Mittelhirnneuronen kehrte sich das Bild um. Obwohl ein anderer Kalziumkanaltyp insgesamt häufiger wurde, zeigten Neurone mit der L271H-Variante weniger Kalziumspitzen, einen stärker depolarisierten Ruhemodus und ließen sich schwerer zu wiederholtem Feuern anregen. Ihre Aktionspotenziale waren kleiner und langsamer im Anstieg und Abfall, was darauf hindeutet, dass die Variante letztlich die Fähigkeit der Neurone dämpft, robuste elektrische Signale zu senden.
Mini-Gehirne, die schneller wachsen, sich aber schlecht organisieren
In kortikalen Organoiden hinterließ die L271H-Variante deutliche strukturelle Spuren. Im Vergleich zu Kontrollen hatten patientenabgeleitete Organoide weniger und kleinere ventrikelähnliche Hohlräume – ringförmige Zonen, in denen sich Vorläuferzellen normalerweise geordnet aneinanderreihen. Radiale Gliazellen, die als Gerüst dienen und neugeborene Neurone leiten, waren über das Gewebe verstreut, statt ordentliche, polarisierte Schichten zu bilden. Intermediäre Vorläuferzellen und Neurone traten früher auf und gingen dann schneller zurück, was darauf hindeutet, dass Vorläufer zu früh zur Differenzierung gedrängt wurden. Nach 60 Tagen holte die Gesamtzahl der Neurone auf, doch das frühe Fehlzeitmuster und die Desorganisation deuten eher auf einen gestörten Bauplan für kortikale Schaltkreise als auf ein absolutes Versagen bei der Neuronenbildung hin.
Verschiebung der Genaktivität hin zu Programmen mit neuroentwicklungsbedingtem Risiko
Um zu verstehen, wie veränderte Kalziumverarbeitung in die Genkontrolle einfließt, sequenzierten die Forschenden RNA aus Patienten- und Kontrollzellen in verschiedenen Stadien. Die Unterschiede waren in Stammzellen gering, wuchsen aber in Vorläufern und Neuronen, als die Cav1.3-Expression zunahm. Viele Gene, die in den Patientenzellen hoch- oder herunterreguliert waren, sind an Transkriptionskontrolle, Hirnentwicklung und Neurogenese beteiligt. Mehrere davon, darunter PTN, MEIS2, POU3F2, CNTN4, CNTNAP2 und AUTS2, sind bekannte Risikogene für Autismus und verwandte neuroentwicklungsbedingte Erkrankungen. Diese Veränderungen sprechen dafür, dass abnormer Kalziumeinstrom durch Cav1.3 die aktivitätsabhängigen Genprogramme umformt, die steuern, wie Gehirnzellen proliferieren, migrieren und sich verschalten.
Was das für Patientinnen, Patienten und künftige Therapien bedeutet
Kurz gesagt zeigt diese Arbeit, wie eine einzelne Kalziumkanalvariante frühe Gehirnzellen zunächst überstimulieren kann, dann reife Neurone unterversorgt zurücklässt und gleichzeitig Gennetzwerke, die mit neuroentwicklungsbedingten Störungen assoziiert sind, aus dem Gleichgewicht bringt. Das Ergebnis kann ein äußerlich weitgehend normales wirkendes Gehirn sein, das jedoch aus zu schnell entstandenen und unvollständig organisierten Schaltkreisen aufgebaut ist. Indem die Studie die Mutation dieser Patientin in menschlichen Zellen und Organoiden nachbildet, liefert sie einen detaillierten Fahrplan, der einen molekularen Defekt mit veränderter Zellsignalgebung, Gewebearchitektur und Genregulation verknüpft. Dieses Modell bietet nun eine Plattform, um gezielte Medikamente und genetische Strategien zu testen, die darauf abzielen, das Kalziumsignal in Cav1.3-assoziierten Kanalopathien wieder normaler zu gestalten.
Zitation: Tisch, M., Geisler, S.M., Gabassi, E. et al. Aberrant calcium signaling and neuronal activity in the L271H CACNA1D (Cav1.3) iPSC model of neurodevelopmental disease. Mol Psychiatry 31, 2927–2940 (2026). https://doi.org/10.1038/s41380-025-03429-8
Schlüsselwörter: Kalziumkanäle, neuroentwicklungsstörungen, induzierte pluripotente Stammzellen, Gehirnorganoide, Autismus-Risikogene