Clear Sky Science · es
Señalización de calcio aberrante y actividad neuronal en el modelo iPSC L271H CACNA1D (Cav1.3) de enfermedad del neurodesarrollo
Cuando un cambio en un solo gen se propaga por el desarrollo cerebral
Alteraciones raras en genes pueden modificar sutilmente cómo las células cerebrales manejan señales eléctricas y químicas. Este estudio sigue uno de esos cambios en un gen de un canal de calcio vinculado con retraso del desarrollo, convulsiones y síntomas similares al autismo. Al convertir las células sanguíneas de una paciente en células madre y luego en tejidos cerebrales diminutos y neuronas en cultivo, los investigadores trazan cómo una pequeña modificación molecular puede distorsionar el desarrollo temprano del cerebro y la actividad neuronal.
Guardianes que dejan entrar calcio a las células cerebrales
Las células cerebrales dependen de un flujo controlado de iones de calcio para crecer, comunicarse y activar o desactivar genes. «Portones» especializados en la membrana celular, llamados canales de calcio dependientes de voltaje, se abren durante la actividad eléctrica y permiten la entrada de calcio. Uno de estos, conocido como Cav1.3, es importante en muchos órganos, incluido el cerebro y tejidos productores de hormonas. En varios pacientes, cambios hereditarios raros en el gen de Cav1.3 se han relacionado con una combinación de síntomas: desequilibrios hormonales, debilidad muscular, convulsiones, retraso del desarrollo y rasgos del espectro autista. La variante estudiada aquí, denominada L271H, se había demostrado en células no neuronales que hace que el canal se abra más fácilmente, pero se desconocía su impacto en células cerebrales humanas.
Construir células cerebrales específicas del paciente en el laboratorio
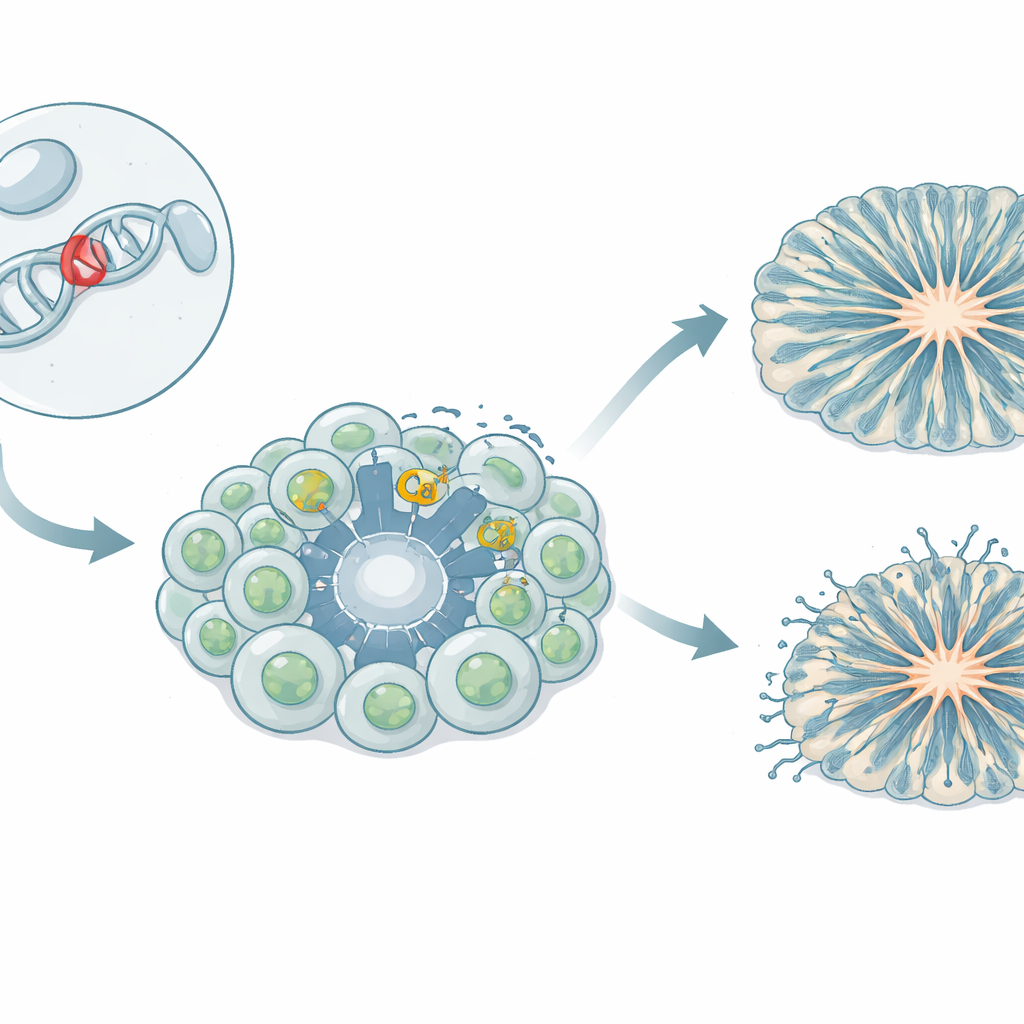
El equipo creó un modelo iPSC, en el que células sanguíneas de una niña portadora de la variante L271H fueron reprogramadas a células madre capaces de formar cualquier tejido. Estas células madre pluripotentes inducidas se dirigieron luego a convertirse en células progenitoras neurales—los bloques constructores tempranos que generan posteriormente neuronas—y en neuronas del mesencéfalo relacionadas con la señalización dopaminérgica. Los investigadores también cultivaron organoides corticales tridimensionales, pequeñas estructuras «mini‑cerebrales» que imitan las primeras etapas de la formación de la corteza humana. Al comparar células derivadas del paciente con varias líneas de control de donantes sanos, pudieron separar los efectos de la variante de la variación genética natural.
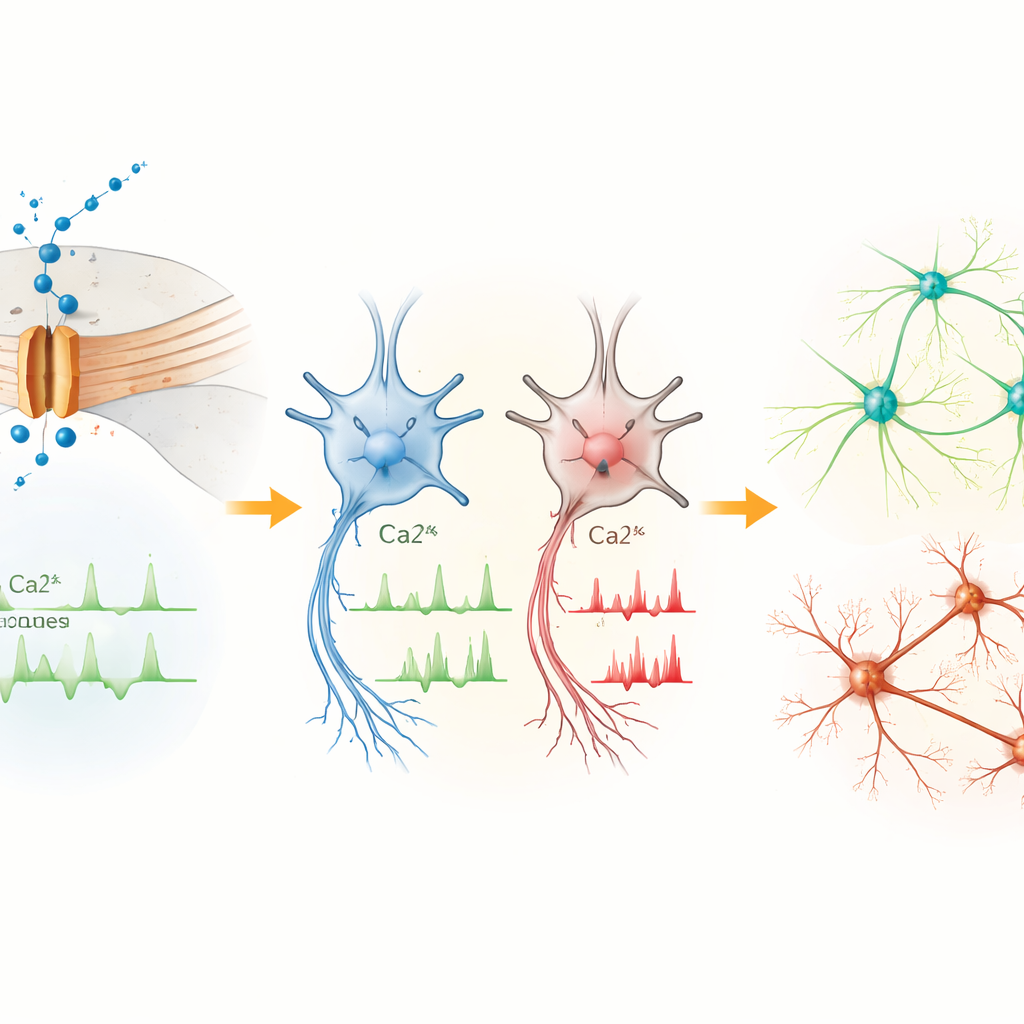
Las células tempranas señalan en exceso, las neuronas maduras disparan de menos
En los progenitores neurales más tempranos, el canal Cav1.3 era la forma dominante de este portón de calcio. Las células portadoras de la variante L271H mostraron oleadas espontáneas de calcio con mayor frecuencia que los controles, aunque sus propiedades eléctricas básicas eran similares. Esto sugiere que, en esta etapa, la variante perturba principalmente el equilibrio de calcio dentro de la célula más que el disparo evidente de impulsos eléctricos. A medida que las células maduraron en neuronas del mesencéfalo, la situación se invirtió. Aunque otro tipo de canal de calcio se volvió más abundante en general, las neuronas con la variante L271H mostraron menos picos de calcio, un estado de reposo más despolarizado y resultaron más difíciles de inducir a descargas repetidas. Sus potenciales de acción eran más pequeños y más lentos en subir y bajar, lo que indica que la variante acaba atenuando la capacidad de las neuronas para enviar señales eléctricas robustas.
Mini‑cerebros que crecen más rápido pero se organizan mal
En los organoides corticales, la variante L271H dejó una huella marcada en la estructura. En comparación con los controles, los organoides derivados del paciente tenían menos y más pequeñas cavidades tipo ventrículo—zonas en forma de anillo donde las células progenitoras normalmente se alinean ordenadamente. Las células gliales radiales, que actúan como andamiaje y guían a las neuronas recién nacidas, estaban dispersas por el tejido en lugar de formar capas polarizadas y ordenadas. Las células progenitoras intermedias y las neuronas aparecieron antes y luego disminuyeron antes, lo que sugiere que los progenitores fueron impulsados a diferenciarse demasiado rápido. A los 60 días, el número total de neuronas se igualó, pero la descoordinación y el desajuste temporal temprano apuntan a un plano alterado para construir circuitos corticales más que a un fracaso absoluto en producir neuronas.
La actividad génica se desplaza hacia programas de riesgo neurodesarrollista
Para entender cómo el manejo alterado del calcio incide en el control génico, el equipo secuenció ARN de células del paciente y controles en diferentes etapas. Las diferencias fueron modestas en las células madre pero crecieron en progenitores y neuronas a medida que aumentaba la expresión de Cav1.3. Muchos genes que subieron o bajaron en las células del paciente están implicados en el control de la transcripción, el desarrollo cerebral y la neurogénesis. Varios, incluidos PTN, MEIS2, POU3F2, CNTN4, CNTNAP2 y AUTS2, son genes de riesgo conocidos para el autismo y condiciones neurodesarrollistas relacionadas. Estos cambios sugieren que la entrada anómala de calcio a través de Cav1.3 remodela programas génicos dependientes de la actividad que guían cómo las células cerebrales proliferan, migran y se conectan entre sí.
Qué significa esto para los pacientes y las terapias futuras
En pocas palabras, este trabajo muestra cómo una sola variante en un canal de calcio puede, primero, sobreestimular las células cerebrales tempranas y, luego, dejar a las neuronas maduras con menor potencia, mientras al mismo tiempo desvía redes génicas asociadas con trastornos del neurodesarrollo. El resultado es un cerebro que puede parecer en gran medida normal desde el exterior pero que está construido a partir de circuitos que se desarrollaron demasiado rápido y se organizaron de forma imperfecta. Al recrear la mutación de esta paciente en células humanas y organoides, el estudio ofrece una hoja de ruta detallada que vincula un defecto molecular con señalización celular alterada, arquitectura tisular y regulación génica. Este modelo ahora proporciona una plataforma para probar fármacos dirigidos y estrategias genéticas destinadas a restaurar una señalización de calcio más normal en las canalopatías relacionadas con Cav1.3.
Cita: Tisch, M., Geisler, S.M., Gabassi, E. et al. Aberrant calcium signaling and neuronal activity in the L271H CACNA1D (Cav1.3) iPSC model of neurodevelopmental disease. Mol Psychiatry 31, 2927–2940 (2026). https://doi.org/10.1038/s41380-025-03429-8
Palabras clave: canales de calcio, trastornos del neurodesarrollo, células madre pluripotentes inducidas, organoides cerebrales, genes de riesgo para el autismo