Clear Sky Science · ru
Отклонённая кальциевая сигнализация и активность нейронов в модели нейроразвитийных заболеваний на iPSC с вариантом L271H гена CACNA1D (Cav1.3)
Когда одиночное изменение гена вызывает волну в развитии мозга
Редкие изменения в генах могут тонко менять то, как клетки мозга обрабатывают электрические и химические сигналы. В этом исследовании прослеживается одно такое изменение в гене кальциевого канала, связанное с задержкой развития, судорогами и симптомами, похожими на аутизм. Превратив кровь пациентки в стволовые клетки, а затем в миниатюрные ткани мозга и нейроны в чашке Петри, исследователи проследили, как незначительная молекулярная модификация может исказить раннее развитие мозга и активность нейронов.
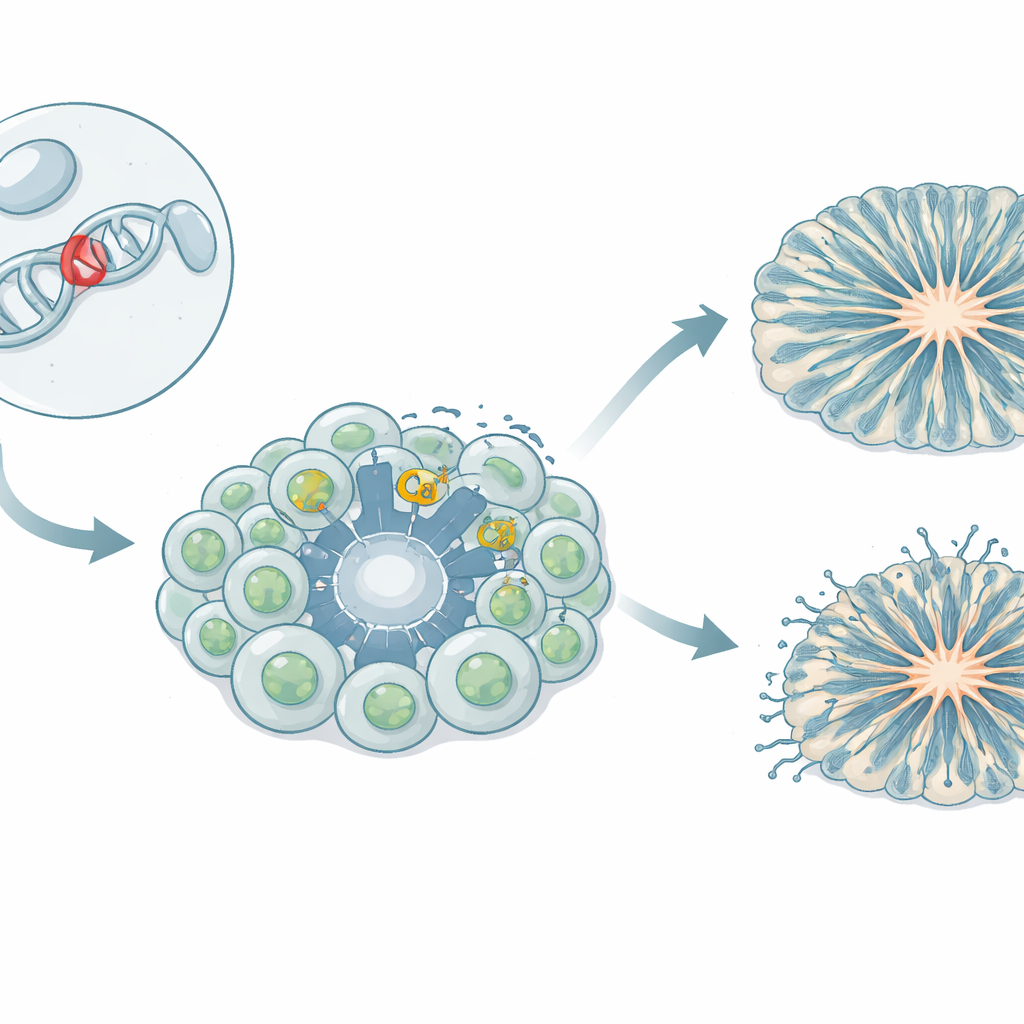
«Привратники», впускающие кальций в клетки мозга
Клетки мозга зависят от контролируемого притока ионов кальция, который помогает им расти, общаться друг с другом и включать или выключать гены. Специальные «ворота» в мембране клетки, называемые потенциалзависимыми кальциевыми каналами, открываются при электрической активности и пропускают кальций. Один из таких каналов, известный как Cav1.3, важен во многих органах, включая мозг и гормонопродуцирующие ткани. У нескольких пациентов редкие наследуемые изменения в гене Cav1.3 связывали со смесью симптомов: гормональными нарушениями, мышечной слабостью, судорогами, задержкой развития и чертами аутистического спектра. Вариант, изученный здесь, названный L271H, в ненейрональных клетках показал, что канал открывается легче, но его влияние на клетки человеческого мозга оставалось неизвестным.
Создание специфичных для пациента клеток мозга в лаборатории
Команда создала модель на основе iPSC: клетки крови девочки с вариантом L271H перепрограммировали в стволовые клетки, способные образовывать любые ткани. Эти индуцированные плюрипотентные стволовые клетки затем направляли к превращению в нейральные прогениторы — ранние строительные блоки, которые позднее дают нейроны — и в нейроны среднего мозга, связанные с допаминергическим сигналингом. Исследователи также выращивали трёхмерные кортикальные органоиды — крошечные «мини‑мозги», имитирующие ранние стадии формирования человеческой коры. Сравнивая клетки, полученные от пациента, с несколькими контрольными линиями здоровых доноров, они могли отделить эффекты варианта от естественной генетической изменчивости.
Ранние клетки сигнализируют слишком активно, зрелые нейроны — слишком слабо
В самых ранних нейральных прогениторах канал Cav1.3 был доминирующим типом этого кальциевого «ворот». Клетки с вариантом L271H демонстрировали более частые спонтанные всплески кальция по сравнению с контролем, хотя их базовые электрические свойства были схожи. Это указывает на то, что на этой стадии вариант прежде всего нарушает внутриклеточный баланс кальция, а не явно усиливает генерацию электрических импульсов. По мере созревания в нейроны среднего мозга картина менялась. Несмотря на то, что другой тип кальциевого канала становился более распространённым в целом, нейроны с вариантом L271H показывали меньше кальциевых всплесков, более деполяризованный покой и были менее склонны к повторной активации. Их потенциалы действия были меньшими по амплитуде и медленнее по подъёму и спаду, что указывает на то, что в итоге вариант ослабляет способность нейронов генерировать сильные электрические сигналы.
Мини‑мозги растут быстрее, но организуются плохо
В кортикальных органоидах вариант L271H сильно повлиял на структуру. По сравнению с контролями, органоиды пациента имели меньше и меньшие по размеру желудочкообразные полости — кольцевые зоны, где прогениторные клетки обычно выстраиваются упорядоченно. Радиальные глиальные клетки, которые служат каркасом и направляют новообразованные нейроны, были разбросаны по ткани вместо того, чтобы формировать аккуратные поляризованные слои. Промежуточные прогениторы и нейроны появлялись раньше и затем их число снижалось, что свидетельствует о том, что прогениторы вынужденно дифференцировались слишком быстро. К 60 дню общее число нейронов сравнялось с контролем, но раннее смещение по времени и дезорганизация указывают на нарушение чертежа построения кортикальных цепей, а не на полную неспособность образовывать нейроны.
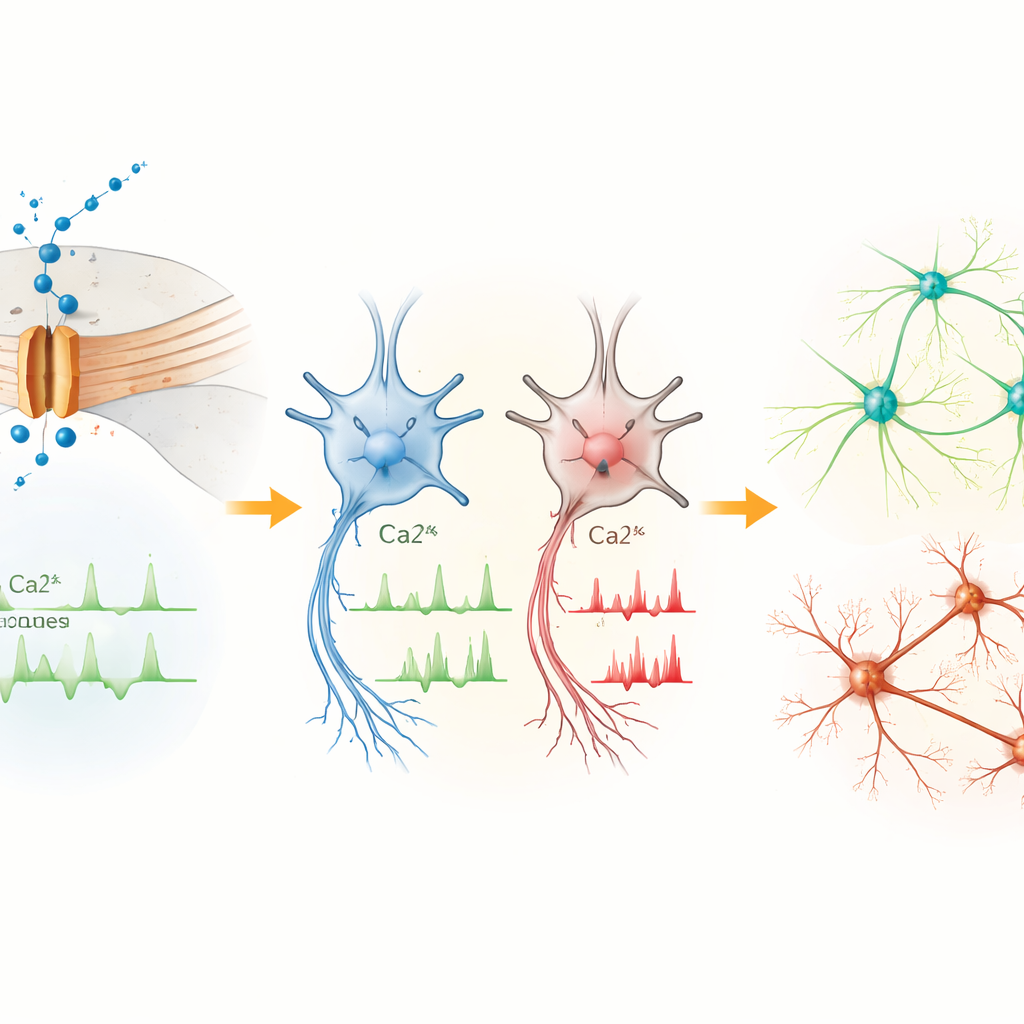
Сдвиг активности генов в сторону программ риска нейроразвития
Чтобы понять, как изменённое обращение с кальцием влияет на регуляцию генов, команда секвенировала РНК из клеток пациента и контролей на разных стадиях. Различия были скромными в стволовых клетках, но усиливались в прогениторах и нейронах по мере увеличения экспрессии Cav1.3. Многие генетические изменения в клетках пациента затрагивали гены, участвующие в контроле транскрипции, развитии мозга и нейрогенезе. Несколько из них, включая PTN, MEIS2, POU3F2, CNTN4, CNTNAP2 и AUTS2, известны как гены риска аутизма и связанных нейроразвитийных состояний. Эти изменения предполагают, что аномальный вход кальция через Cav1.3 перестраивает программы активности‑зависимой регуляции генов, которые направляют пролиферацию, миграцию и формирование связей клеток мозга.
Что это значит для пациентов и будущих терапий
Проще говоря, эта работа показывает, как один вариант кальциевого канала может сначала гиперстимулировать ранние клетки мозга, а затем ослабить зрелые нейроны, одновременно сдвигая генетические сети, связанные с нейроразвитийными расстройствами. В результате может сформироваться мозг, который внешне выглядит в целом нормально, но построен из цепей, развившихся слишком быстро и организованных с погрешностями. Воспроизведя мутацию этого пациента в человеческих клетках и органоидах, исследование предоставляет подробную маршрутную карту, связывающую молекулярный дефект с изменённой клеточной сигнализацией, архитектурой тканей и регуляцией генов. Эта модель теперь представляет собой платформу для тестирования целевых лекарств и генетических стратегий, направленных на восстановление более нормальной кальциевой сигнализации при связанных с Cav1.3 каналопатиях.
Цитирование: Tisch, M., Geisler, S.M., Gabassi, E. et al. Aberrant calcium signaling and neuronal activity in the L271H CACNA1D (Cav1.3) iPSC model of neurodevelopmental disease. Mol Psychiatry 31, 2927–2940 (2026). https://doi.org/10.1038/s41380-025-03429-8
Ключевые слова: кальциевые каналы, нейроразвитийные расстройства, индуцированные плюрипотентные стволовые клетки, органоиды мозга, гены риска аутизма