Clear Sky Science · ja
神経発達疾患のiPSCモデルにおけるL271H CACNA1D (Cav1.3) の異常なカルシウムシグナルとニューロン活動
一つの遺伝子変化が脳の発達に波及するとき
希少な遺伝子変異は、脳細胞が電気的・化学的シグナルを扱う仕方を微妙に変えることがあります。本研究は、発達遅滞、てんかん、および自閉症様症状と関連するカルシウムチャネル遺伝子の一例を追跡します。患者の血液細胞を幹細胞にし、それを皿上での小さな脳組織やニューロンに変えることで、極微の分子変化が初期の脳発達とニューロン活動をどのように歪めるかをマップしています。
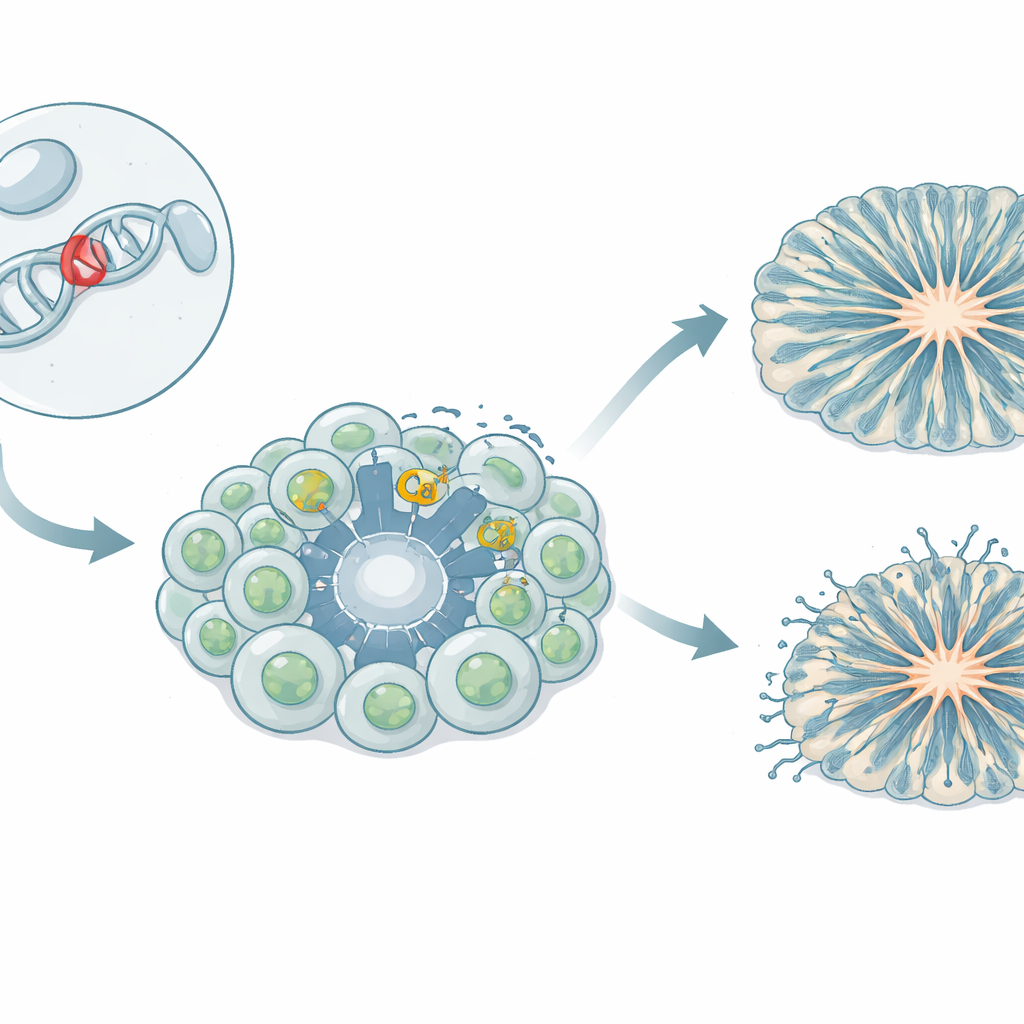
カルシウムを脳細胞に通すゲートキーパー
脳細胞は、成長し、互いにコミュニケーションを取り、遺伝子のオン・オフを切り替えるために制御された微量のカルシウムイオンに依存しています。細胞膜にある電位依存性カルシウムチャネルと呼ばれる特殊な「ゲート」は、電気活動の際に開いてカルシウムを取り込みます。そのうちの一つ、Cav1.3は脳やホルモン産生組織を含む多くの臓器で重要です。複数の患者で、Cav1.3遺伝子の希少な遺伝的変化が、ホルモン失調、筋力低下、けいれん、発達遅滞、および自閉症スペクトラム様の特徴の混在に結び付けられています。本研究で扱うL271Hという変異は、非神経細胞ではチャネルをより開きやすくすることが示されていましたが、人間の脳細胞における影響は不明でした。
患者特異的な脳細胞を試験管で作る
研究チームはiPSCモデルを作成しました。L271H変異を持つ女児の血液細胞を再プログラムして、あらゆる組織を形成できる幹細胞に変換しました。これらの誘導多能性幹細胞はさらに神経前駆細胞—後にニューロンを生み出す初期の構成要素—やドーパミンシグナルに関連する中脳ニューロンへと誘導されました。研究者たちはまた、ヒト皮質形成の初期段階を模倣する三次元の皮質オルガノイド(小さな「ミニ脳」構造)も育てました。患者由来の細胞と複数の健康なドナー由来のコントロール系を比較することで、変異の影響を自然な遺伝的多様性から切り離して評価できました。
初期細胞は過剰にシグナルを出し、成熟ニューロンは発火が不足する
最も初期の神経前駆細胞では、Cav1.3がこのカルシウムゲートの優勢な形式でした。L271H変異を持つ細胞は、基本的な電気的特性は類似しているにもかかわらず、対照よりも自発的なカルシウム上昇が頻繁に起こりました。これはこの段階で、変異が主に細胞内のカルシウムバランスを乱し、明瞭な電気的発火を直接増加させるわけではないことを示唆します。細胞が中脳ニューロンへ成熟するにつれて状況は逆転しました。全体として別のタイプのカルシウムチャネルの発現が増える一方で、L271H変異を持つニューロンはカルシウムスパイクが少なく、静止膜電位はより脱分極しており、繰り返し発火させるのが難しくなっていました。活動電位は振幅が小さく立ち上がり・立ち下がりが遅く、最終的に変異がニューロンの強い電気信号を送る能力を弱めることを示しています。
速く成長するが配列が乱れたミニ脳
皮質オルガノイドでは、L271H変異が構造に強い影響を与えました。対照と比べて、患者由来オルガノイドは脳室様の空洞が少なく小さく、前駆細胞が通常整然と並ぶリング状領域が減少していました。新生ニューロンを導く足場として働く放射状グリア細胞は、整然とした極性のある層を形成せず組織全体に散在していました。中間前駆細胞とニューロンは早期に出現してその後早く減少し、前駆細胞が過度に早く分化へ押し出されたことを示唆します。60日目までには総ニューロン数は追いつきましたが、初期のタイミングの狂いと組織の乱れは、ニューロンを作り損なったというよりも皮質回路を組み立てる設計図が乱れたことを示しています。
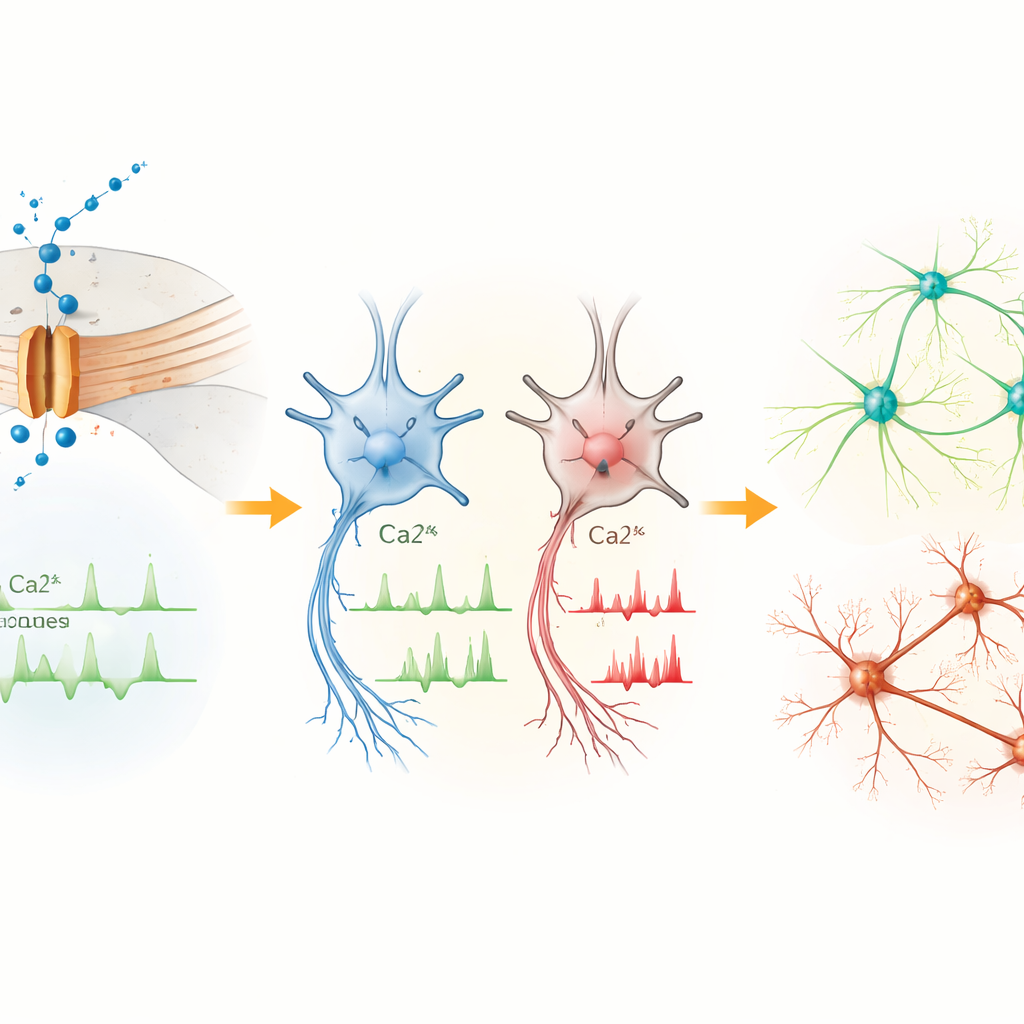
神経発達リスクに傾く遺伝子発現の変化
変化したカルシウム処理がどのように遺伝子制御に影響するかを理解するため、研究チームは異なる段階の患者・対照細胞からRNA配列解析を行いました。幹細胞では差異は控えめでしたが、Cav1.3の発現が増すにつれて前駆細胞やニューロンで差異は拡大しました。患者細胞で上方または下方に変化した多くの遺伝子は、転写制御、脳発達、神経新生に関与しています。PTN、MEIS2、POU3F2、CNTN4、CNTNAP2、AUTS2を含むいくつかは、自閉症や関連する神経発達障害の既知のリスク遺伝子です。これらの変化は、Cav1.3を通る異常なカルシウム流入が、脳細胞の増殖、移動、配線を導く活動依存的な遺伝子プログラムを再形成することを示唆します。
患者と将来の治療にとっての意味
簡潔に言えば、本研究は一つのカルシウムチャネル変異が最初に初期脳細胞を過剰刺激し、次に成熟ニューロンを力不足にし、同時に神経発達障害に関わる遺伝子ネットワークを軌道から逸らす仕組みを示しています。外見上は大きく正常に見える脳であっても、回路が過速に発達し不完全に組織されたことで機能に影響が出る可能性があります。患者の変異をヒト細胞とオルガノイドで再現することで、本研究は分子欠陥を細胞シグナル伝達、組織構築、遺伝子制御の変化に結びつける詳細なロードマップを提供します。このモデルは現在、Cav1.3関連チャネル病におけるより正常なカルシウムシグナルを回復することを目的とした標的薬剤や遺伝子戦略を試すプラットフォームを提供します。
引用: Tisch, M., Geisler, S.M., Gabassi, E. et al. Aberrant calcium signaling and neuronal activity in the L271H CACNA1D (Cav1.3) iPSC model of neurodevelopmental disease. Mol Psychiatry 31, 2927–2940 (2026). https://doi.org/10.1038/s41380-025-03429-8
キーワード: カルシウムチャネル, 神経発達障害, 誘導多能性幹細胞, 脳オルガノイド, 自閉症リスク遺伝子