Clear Sky Science · sv
Avvikande kalciumsignalering och neuronal aktivitet i L271H CACNA1D (Cav1.3) iPSC-modellen för neurodevelopmental sjukdom
När en enda genförändring får vågor genom hjärnans utveckling
Sällsynta förändringar i gener kan subtilt påverka hur hjärnceller hanterar elektriska och kemiska signaler. Denna studie följer en sådan förändring i en gen för en kalciumkanal som kopplats till utvecklingsförsening, anfall och autismliknande symtom. Genom att omvandla en patients blodceller till stamceller och sedan till miniatyrhjärnvävnader och neuroner i ett odlingskärl kartlägger forskarna hur en liten molekylär ändring kan snedvrida tidig hjärnutveckling och neuronal aktivitet.
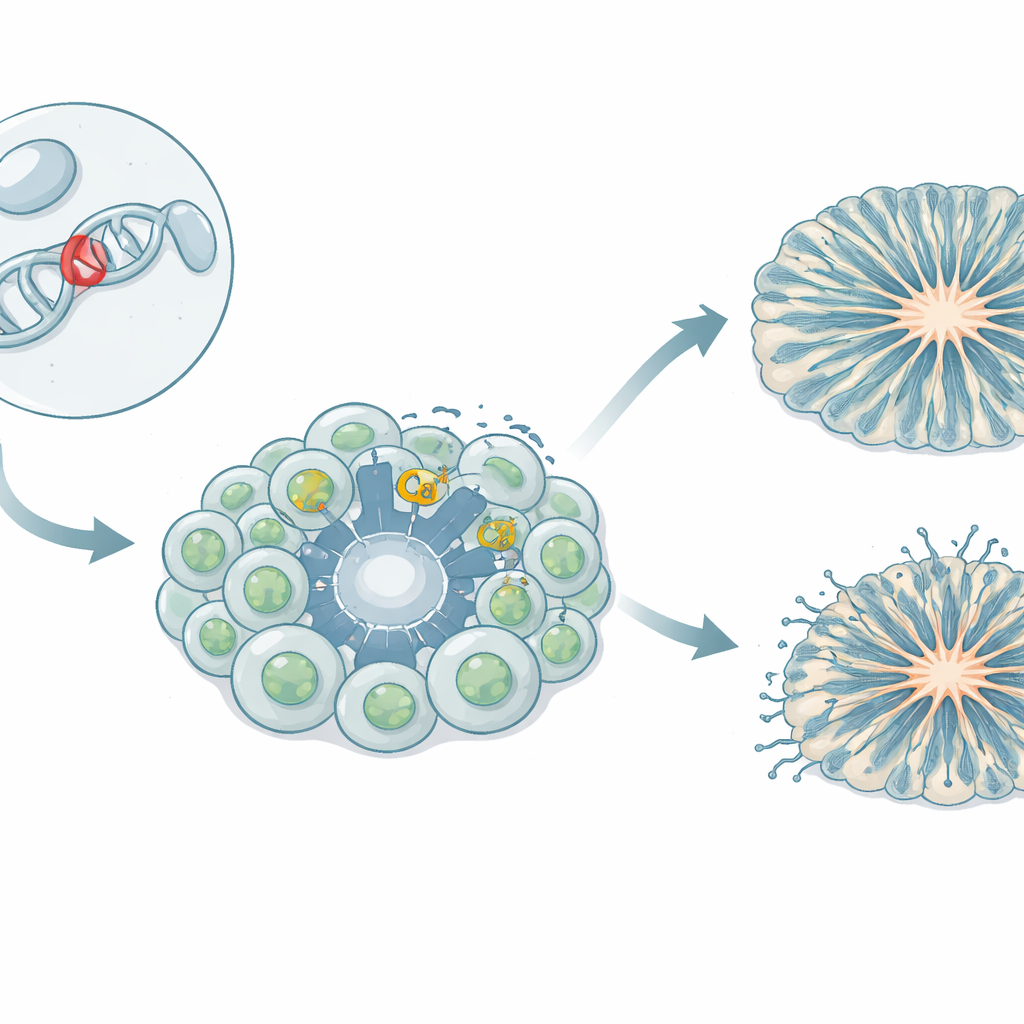
Portvakter som släpper in kalcium i hjärnceller
Hjärnceller är beroende av en kontrollerad tillströmning av kalciumjoner för att växa, kommunicera med varandra och slå på eller av gener. Specialiserade ”portar” i cellmembranet, så kallade spänningskänsliga kalciumkanaler, öppnas vid elektrisk aktivitet och släpper in kalcium. En sådan port, känd som Cav1.3, är viktig i många organ, inklusive hjärnan och hormonproducerande vävnader. Hos flera patienter har sällsynta ärftliga förändringar i Cav1.3‑genen kopplats till en blandning av symtom: hormonella obalanser, muskelsvaghet, anfall, försenad utveckling och drag inom autismspektrat. Varianten som studeras här, kallad L271H, hade visats i icke‑neurala celler göra kanalen lättare att öppna, men dess påverkan på mänskliga hjärnceller var tidigare okänd.
Att bygga patientspecifika hjärnceller i laboratoriet
Teamet skapade en iPSC‑modell där blodceller från en flicka som bär L271H‑varianten omprogrammerades till stamceller med förmåga att bilda vilken vävnad som helst. Dessa inducerade pluripotenta stamceller vägleddes sedan att bli neural progenitorceller — de tidiga byggstenarna som senare ger upphov till neuroner — och till mitthjärnsneuroner kopplade till dopaminsignalering. Forskarna odlade också tredimensionella kortikala organoider, små ”mini‑hjärnor” som efterliknar tidiga stadier av människans cortexbildning. Genom att jämföra patient‑härledda celler med flera kontrolllinjer från friska givare kunde de skilja variantens effekter från naturlig genetisk variation.
Tidiga celler signalerar för mycket, mogna neuroner avfyrar för lite
I de tidigaste neurala progenitorerna var Cav1.3‑kanalen den dominerande formen av denna kalciumport. Celler som bar L271H‑varianten uppvisade tätare spontana kalciumtoppar än kontroller, trots att deras grundläggande elektriska egenskaper var likartade. Det tyder på att varianten i detta stadium främst stör kalciumbalansen inne i cellen snarare än att orsaka uttalad elektrisk avfyrning. När cellerna mognade till mitthjärnsneuroner vände bilden. Trots att en annan kalciumkanaltyp blev mer dominerande totalt sett, visade neuroner med L271H‑varianten färre kalciumspikar, ett mer depolariserat vilopotential och var svårare att få att repetitivt avfyra. Deras aktionspotentialer var mindre och långsammare i upp- och nedgång, vilket indikerar att varianten i slutändan dämpar neuroners förmåga att skicka kraftfulla elektriska signaler.
Mini‑hjärnor som växer snabbare men organiserar sig dåligt
I kortikala organoider satte L271H‑varianten tydliga spår i vävnadsstrukturen. Jämfört med kontroller hade patient‑härledda organoider färre och mindre ventrikel‑liknande håligheter — ringformade zoner där progenitorceller normalt ligger upp i ordnade lager. Radiala gliaceller, som fungerar som ställningar och vägleder nyfödda neuroner, var utspridda genom vävnaden istället för att bilda prydliga, polariserade lager. Intermediära progenitorceller och neuroner dök upp tidigare och minskade sedan snabbare, vilket tyder på att progenitorerna tvingades differentiera för tidigt. Efter 60 dagar kom totala neuronantalet ikapp, men den tidiga felinrymningen och oordningen pekar på en störd ritning för att bygga kortikala kretsar snarare än ett absolut misslyckande att skapa neuroner.
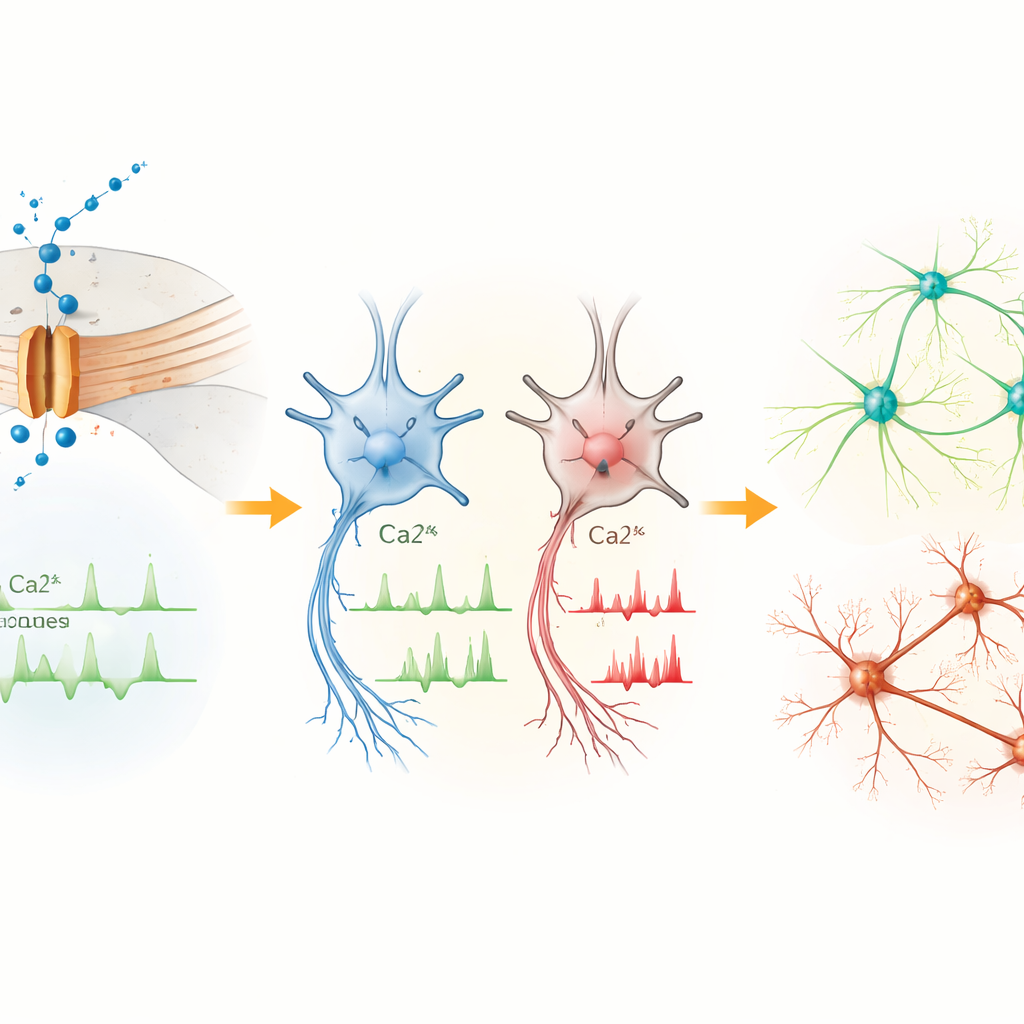
Genaktivitet förskjuts mot program kopplade till neurodevelopmental risk
För att förstå hur förändrad kalciumhantering påverkar genreglering sekvenserade teamet RNA från patient‑ och kontrollceller i olika stadier. Skillnaderna var blygsamma i stamceller men ökade i progenitorer och neuroner i takt med att Cav1.3‑uttrycket steg. Många gener som var upp‑ eller nedreglerade i patientcellerna är involverade i transkriptionskontroll, hjärnutveckling och neurogenes. Flera, inklusive PTN, MEIS2, POU3F2, CNTN4, CNTNAP2 och AUTS2, är kända riskgener för autism och närliggande neurodevelopmentala tillstånd. Dessa förändringar tyder på att onormal kalciuminflux genom Cav1.3 omformar aktivitet‑beroende genprogram som styr hur hjärnceller prolifererar, migrerar och kopplar ihop sig.
Vad detta betyder för patienter och framtida terapier
Enkelt uttryckt visar arbetet hur en enda variant i en kalciumkanal först kan överstimulerar tidiga hjärnceller, sedan lämna mogna neuroner underpresterande, samtidigt som gen-nätverk associerade med neurodevelopmentala störningar rubbas. Resultatet blir en hjärna som utåt kan se i stort sett normal ut men som är uppbyggd av kretsar som utvecklats för snabbt och organiserats ofullständigt. Genom att återskapa denna patients mutation i mänskliga celler och organoider ger studien en detaljerad karta som kopplar ett molekylärt fel till förändrad cellsignalering, vävnadsarkitektur och genreglering. Denna modell erbjuder nu en plattform för att testa riktade läkemedel och genetiska strategier som syftar till att återställa mer normal kalciumsignalering vid Cav1.3‑relaterade kanalopatier.
Citering: Tisch, M., Geisler, S.M., Gabassi, E. et al. Aberrant calcium signaling and neuronal activity in the L271H CACNA1D (Cav1.3) iPSC model of neurodevelopmental disease. Mol Psychiatry 31, 2927–2940 (2026). https://doi.org/10.1038/s41380-025-03429-8
Nyckelord: kalciumkanaler, neurodevelopmentala störningar, inducerade pluripotenta stamceller, hjärnorganoider, autismriskgener