Clear Sky Science · ar
إشارات كالسيوم شاذة ونشاط عصبي في نموذج iPSC لاضطراب التطور العصبي مع طفرة L271H في CACNA1D (Cav1.3)
عندما يترك تغيير جيني مفرد أثرًا خلال تطور الدماغ
يمكن للتغيرات النادرة في الجينات أن تعدّل برفق كيفية تعامل خلايا الدماغ مع الإشارات الكهربائية والكيميائية. تتتبع هذه الدراسة أحد هذه التغيرات في جين قناة الكالسيوم المرتبط بتأخر التطور والنوبات والأعراض الشبيهة بالتوحد. بتحويل خلايا دم المريضة إلى خلايا جذعية ثم إلى أنسجة دماغية وخلايا عصبية مصغرة في المختبر، يرسم الباحثون كيف يمكن لتعديل جزيئي طفيف أن يحرف تطور الدماغ المبكر ونشاط الخلايا العصبية.
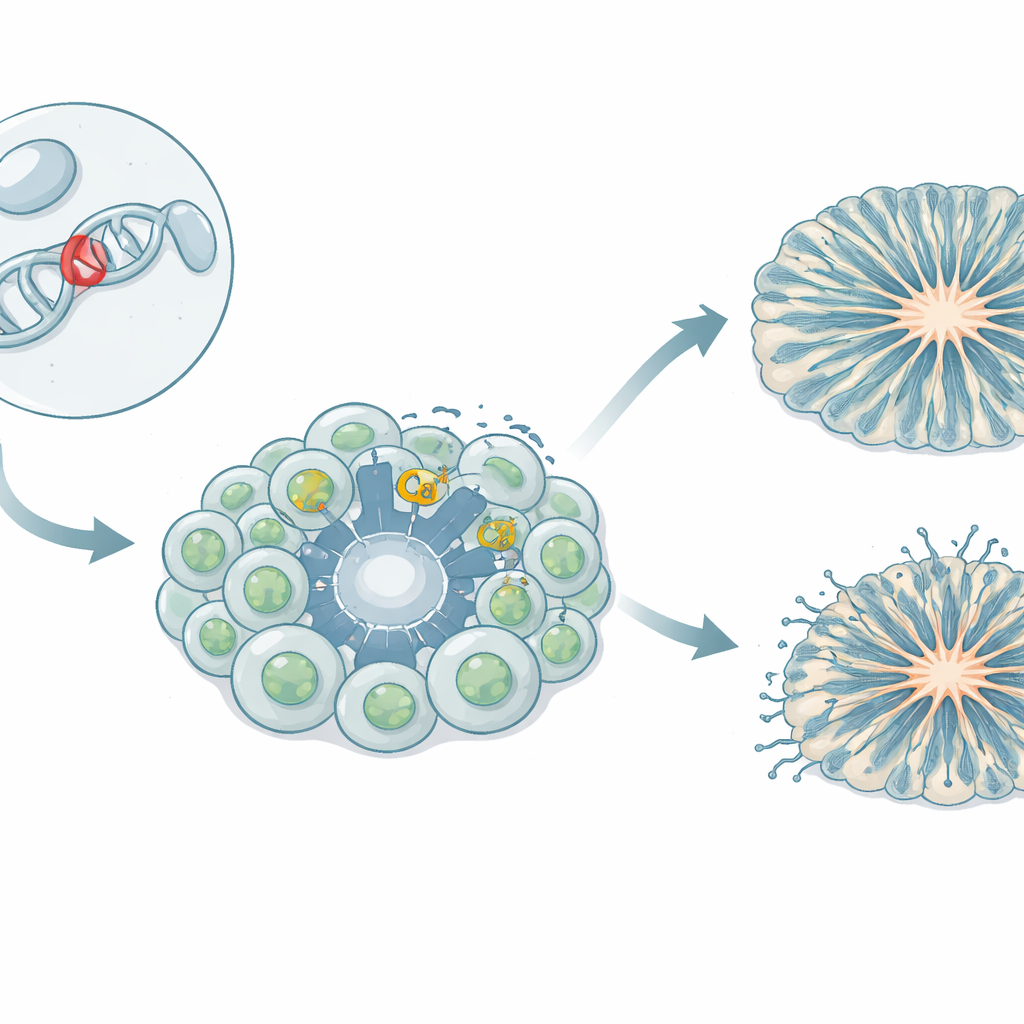
بوّابون تسمح بدخول الكالسيوم إلى خلايا الدماغ
تعتمد خلايا الدماغ على تسرب مسيطر عليه لأيونات الكالسيوم لتنمو وتتواصل مع بعضها وتفعيل أو إيقاف جينات معينة. "بوّابون" متخصّص في غشاء الخلية، يُعرف بقنوات الكالسيوم المعتمدة على الجهد، يفتح أثناء النشاط الكهربائي ويسمح بتدفق الكالسيوم إلى الداخل. إحدى هذه البوابات، المعروفة باسم Cav1.3، مهمة في العديد من الأنسجة بما في ذلك الدماغ والأنسجة المنتجة للهرمونات. في عدة مرضى، ارتبطت تغيّرات وراثية نادرة في جين Cav1.3 بمزيج من الأعراض: اختلالات هرمونية، ضعف عضلي، نوبات صرع، تأخر في التطور، وسمات على طيف التوحد. المتغير الذي دُرِس هنا، المُسَمَّى L271H، أظهر في خلايا غير عصبية أنه يجعل القناة تفتح بسهولة أكبر، لكن تأثيره على خلايا الدماغ البشرية كان مجهولًا.
بناء خلايا دماغية مخصصة للمريض في المختبر
أنشأ الفريق نموذجًا قائمًا على الخلايا الجذعية المحفّزة (iPSC)، حيث أعيد برمجة خلايا دم من فتاة تحمل متغير L271H إلى خلايا جذعية قادرة على تشكيل أي نسيج. ثم تم توجيه هذه الخلايا الجذعية المحدثة لتصبح خلايا سلف عصبية — اللبنات المبكرة التي تُنتج الخلايا العصبية لاحقًا — وإلى خلايا عصبية من منتصف الدماغ المرتبطة بإشارة الدوبامين. كما نما الباحثون أورجانويدات قشرية ثلاثية الأبعاد، وهي هياكل "مخ صغيرة" تحاكي المراحل المبكرة لتكوّن القشرة البشرية. من خلال مقارنة الخلايا المشتقة من المريضة مع عدة خطوط ضابطة من متبرعين أصحاء، استطاعوا فصل تأثير المتغير عن التباين الوراثي الطبيعي.
الخلايا المبكرة ترسل إشارات زائدة بينما الخلايا العصبية الناضجة تنشط أقل
في خلايا السلف العصبية المبكرة، كانت قناة Cav1.3 الشكل السائد لهذه البوابة الكلسية. أظهرت الخلايا الحاملة لمتغير L271H اندفاعات كالسيوم عفوية أكثر تواترًا من الضوابط، رغم تشابه خصائصها الكهربائية الأساسية. هذا يوحي بأنه، في هذه المرحلة، يخلّ المتغير بشكل أساسي بتوازن الكالسيوم داخل الخلية أكثر من تأثيره على إطلاق نبضات كهربائية واضحة. ومع نضوج الخلايا إلى خلايا عصبية من منتصف الدماغ، انقلبت الصورة. رغم أن نوعًا آخر من قنوات الكالسيوم أصبح أكثر وفرة عمومًا، أظهرت الخلايا العصبية الحاملة لمتغير L271H عددًا أقل من ذبذبات الكالسيوم، وحالة راحة أكثر إزالةً للقطبية (مطفّأة أكثر)، وكان من الأصعب تحفيزها لتكرار الإطلاق. كانت جهود الفعل (action potentials) أصغر وأبطأ في الصعود والهبوط، مما يدل على أن المتغير يضعف في النهاية قدرة الخلايا العصبية على إرسال إشارات كهربائية قوية.
مخّيات مصغرة تنمو بسرعة أكبر ولكنها تتنظم بشكل سيئ
في الأورجانويدات القشرية، ترك متغير L271H أثرًا قويًا على البنية. بالمقارنة مع الضوابط، كان لدى الأورجانويدات المأخوذة من المريضة تجاويف شبيهة بالبطينات أقل وعددها أصغر — مناطق حلقية حيث تصطف خلايا السلف عادةً بترتيب منظم. كانت الخلايا النجمية الشعاعية، التي تعمل كدعامات وتوجّه الخلايا العصبية الوليدة، متناثرة في الأنسجة بدلًا من تشكيل طبقات مستقطبة ومنظمة. ظهرت الخلايا السلفية الوسيطة والخلايا العصبية في وقت أبكر ثم انخفضت بسرعة أكبر، ما يشير إلى أن الخلايا السلفية دُفعت نحو التمايز بسرعة مفرطة. بحلول اليوم الستين، تعافت أعداد الخلايا العصبية الإجمالية، لكن التوقيت المبكر الخاطئ وسوء التنظيم يشيران إلى مخطط معطوب لبناء الدوائر القشرية بدلاً من فشل مطلق في إنتاج الخلايا العصبية.
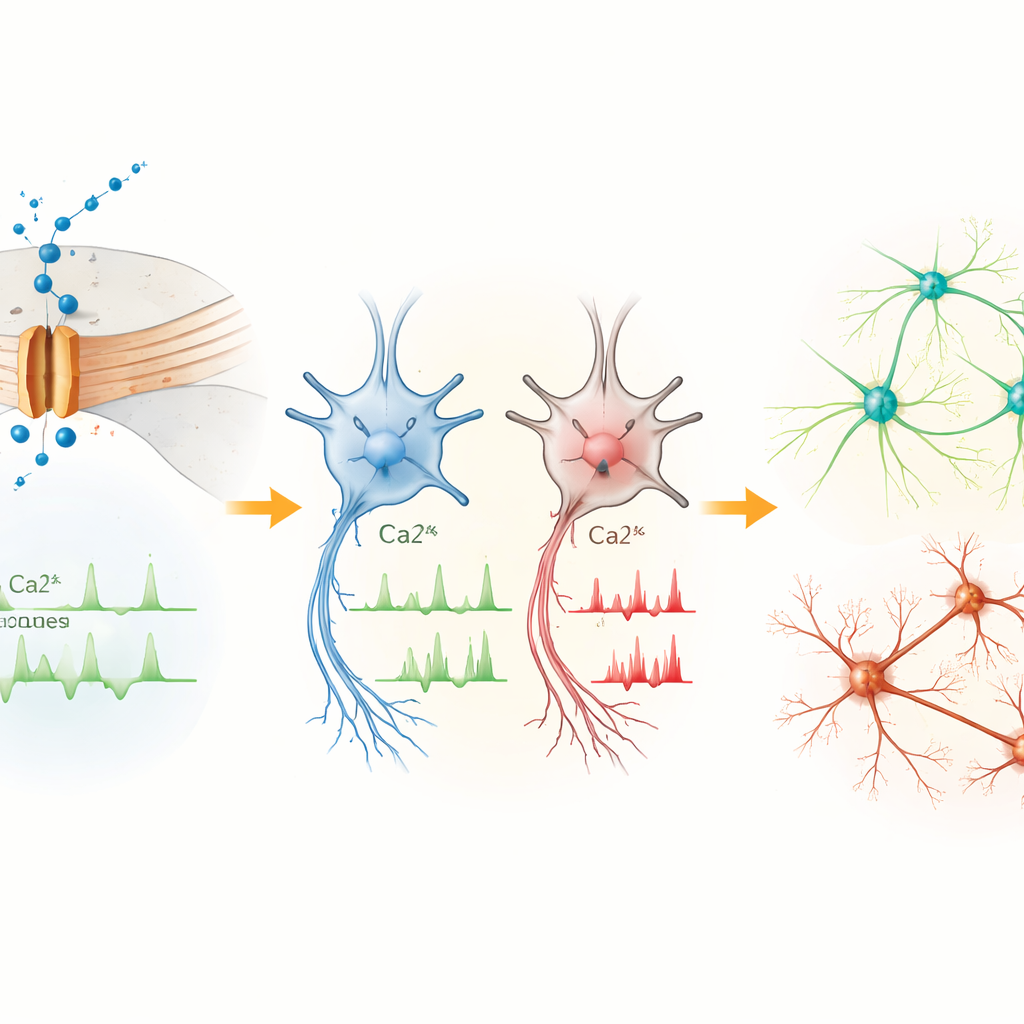
نشاط الجينات يتحول نحو برامج مخاطر التطور العصبي
لفهم كيف يساهم اضطراب توازن الكالسيوم في التحكم الجيني، قام الفريق بتسلسل الحمض النووي الريبوزي (RNA) من خلايا المريضة والضابطة في مراحل مختلفة. كانت الاختلافات متواضعة في الخلايا الجذعية لكنها اتسعت في الخلايا السلفية والخلايا العصبية مع ازدياد تعبير Cav1.3. العديد من الجينات التي ارتفعت أو انخفضت في خلايا المريضة تشارك في التحكم في النسخ، وتطور الدماغ، وتكوين الخلايا العصبية. عدةٌ منها، بما في ذلك PTN وMEIS2 وPOU3F2 وCNTN4 وCNTNAP2 وAUTS2، معروفة كجينات مخاطرة للتوحد والحالات التنموية العصبية ذات الصلة. تقترح هذه التغيرات أن دخول الكالسيوم الشاذ عبر Cav1.3 يعيد تشكيل برامج الجينات المعتمدة على النشاط التي توجه كيف تتكاثر خلايا الدماغ وتهاجر وتتصل ببعضها.
ماذا يعني هذا للمرضى والعلاجات المستقبلية
ببساطة، تُظهر هذه الدراسة كيف يمكن لمتغير واحد في قناة الكالسيوم أن يفرط أولًا في تحفيز خلايا الدماغ المبكرة، ثم يترك الخلايا العصبية الناضجة أقل قدرة، وفي الوقت نفسه يدفع شبكات الجينات المرتبطة باضطرابات التطور العصبي عن مسارها. النتيجة هي دماغ قد يبدو طبيعيًا إلى حد كبير من الخارج لكنه مُبنى من دوائر تطورت بسرعة مفرطة وتنظمت بشكل غير كامل. من خلال إعادة صنع طفرة هذه المريضة في خلايا بشرية وأورجانويدات، توفر الدراسة خريطة مفصلة تربط العيب الجزيئي بتغير إشارات الخلايا، وبنية النسيج، وتنظيم الجينات. يقدم هذا النموذج الآن منصة لاختبار أدوية موجهة واستراتيجيات جينية تهدف إلى استعادة إشارات الكالسيوم الأكثر طبيعية في اعتلالات القنوات المرتبطة بـ Cav1.3.
الاستشهاد: Tisch, M., Geisler, S.M., Gabassi, E. et al. Aberrant calcium signaling and neuronal activity in the L271H CACNA1D (Cav1.3) iPSC model of neurodevelopmental disease. Mol Psychiatry 31, 2927–2940 (2026). https://doi.org/10.1038/s41380-025-03429-8
الكلمات المفتاحية: قنوات الكالسيوم, اضطرابات التطور العصبي, الخلايا الجذعية المحدثة المشتقة من الخلايا الجسدية, أورجانويدات الدماغ, جينات مخاطر التوحد