Clear Sky Science · pl
Nieprawidłowe sygnalizowanie wapniowe i aktywność neuronalna w modelu iPSC L271H CACNA1D (Cav1.3) chorób neurorozwojowych
Kiedy jedna zmiana genetyczna rozchodzi się echem przez rozwój mózgu
Rzadkie zmiany w genach mogą subtelnie modyfikować sposób, w jaki komórki mózgowe radzą sobie z sygnałami elektrycznymi i chemicznymi. W tym badaniu śledzono jedną z takich zmian w genie kanału wapniowego związaną z opóźnieniem rozwoju, napadami i objawami podobnymi do autyzmu. Przekształcając krwi pacjentki w komórki macierzyste, a następnie w miniaturowe tkanki mózgowe i neurony w kulturze, badacze mapują, jak drobna modyfikacja molekularna może zniekształcić wczesny rozwój mózgu i aktywność neuronalną.
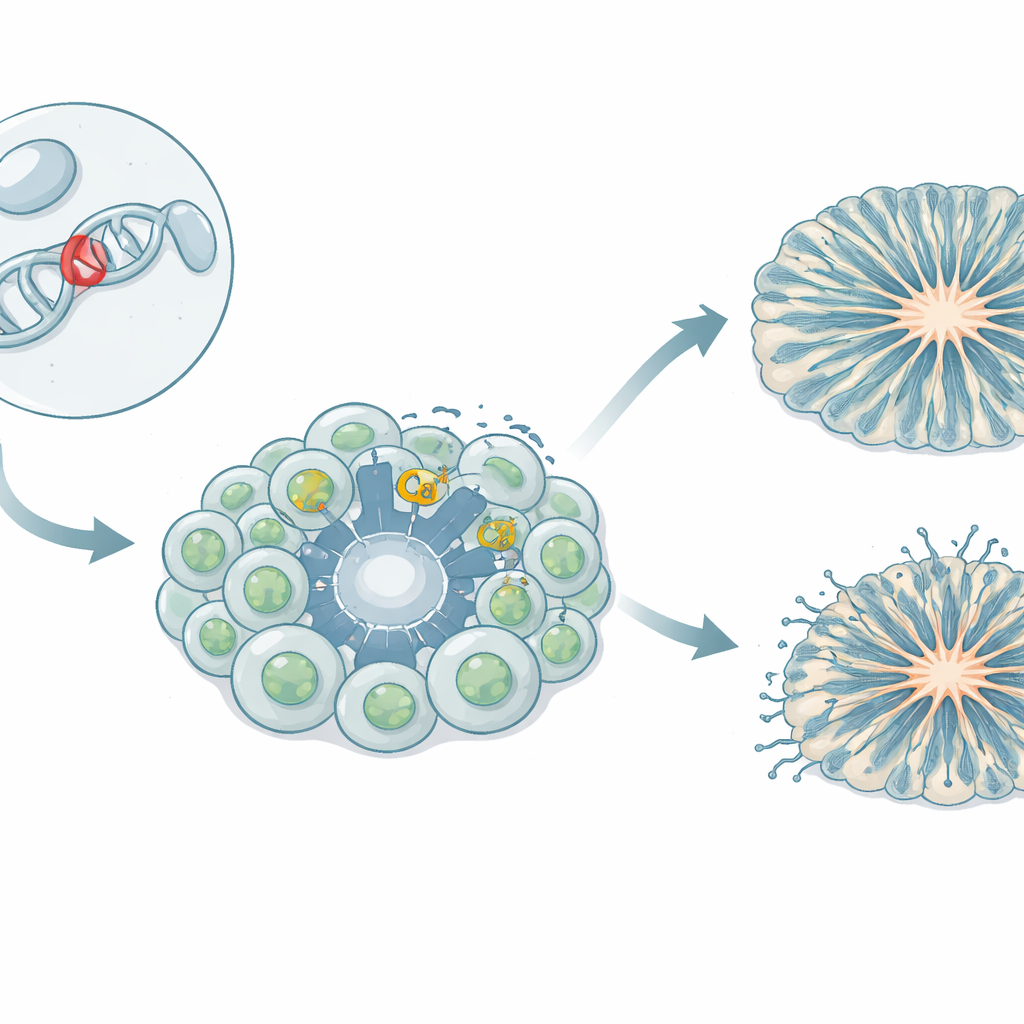
Stróże bramki przepuszczające wapń do komórek mózgu
Komórki mózgowe polegają na kontrolowanym dopływie jonów wapnia, by rosnąć, komunikować się ze sobą i włączać lub wyłączać ekspresję genów. Specjalne „bramki” w błonie komórkowej, zwane kanałami wapniowymi zależnymi od napięcia, otwierają się podczas aktywności elektrycznej i pozwalają wapniowi napływać do wnętrza. Jedna z tych bramek, znana jako Cav1.3, odgrywa ważną rolę w wielu narządach, w tym w mózgu i tkankach wydzielających hormony. U kilku pacjentów rzadkie odziedziczone zmiany w genie Cav1.3 powiązano z mieszanką objawów: zaburzeniami hormonalnymi, osłabieniem mięśni, napadami, opóźnieniem rozwoju i cechami ze spektrum autyzmu. Badany wariant, oznaczony jako L271H, wykazywał w komórkach nie-neuronalnych skłonność do łatwiejszego otwierania kanału, ale jego wpływ na ludzkie komórki mózgowe był nieznany.
Tworzenie komórek mózgowych pacjenta w laboratorium
Zespół stworzył model iPSC, w którym komórki krwi dziewczynki z wariantem L271H zostały przeprogramowane do postaci komórek macierzystych zdolnych do tworzenia dowolnej tkanki. Te indukowane komórki pluripotentne poprowadzono następnie do stanu progenitorów nerwowych — wczesnych elementów budulcowych, które później dają początek neuronom — oraz w kierunku neuronów śródmózgowia związanych z sygnalizacją dopaminergiczną. Badacze hodowali także trójwymiarowe organoidy korowe, niewielkie „mini-mózgi” naśladujące wczesne etapy formowania kory ludzkiej. Porównując komórki pochodzące od pacjentki z kilkoma liniami kontrolnymi od zdrowych dawców, mogli oddzielić efekty wariantu od naturalnej zmienności genetycznej.
Wczesne komórki sygnalizują zbyt mocno, dojrzałe neurony strzelają zbyt słabo
W najwcześniejszych progenitorach nerwowych kanał Cav1.3 był dominującą formą tej bramki wapniowej. Komórki z wariantem L271H wykazywały częstsze spontaniczne skoki wapniowe niż kontrolne, mimo że ich podstawowe właściwości elektryczne były podobne. Sugeruje to, że na tym etapie wariant głównie zaburza równowagę wapniową wewnątrz komórki, a nie bezpośrednio wywołuje wzmożone wyładowania elektryczne. W miarę dojrzewania komórek w neurony śródmózgowia obraz się odwrócił. Chociaż inny typ kanału wapniowego stał się ogólnie bardziej obfity, neurony z wariantem L271H miały mniej skoków wapniowych, bardziej zdepolaryzowany stan spoczynkowy i trudniej było je sprowokować do powtarzalnego wyładowywania. Ich potencjały czynnościowe były mniejsze i wolniej narastały oraz opadały, co wskazuje, że wariant ostatecznie osłabia zdolność neuronów do przekazywania silnych sygnałów elektrycznych.
Mini-mózgi, które rosną szybciej, ale słabo się organizują
W organoidach korowych wariant L271H pozostawił wyraźny ślad w strukturze. W porównaniu z kontrolami organoidy pochodzące od pacjentki miały mniej i mniejsze przestrzenie przypominające komory — pierścieniowe strefy, w których progenitory zwykle ustawiają się w uporządkowany sposób. Komórki glejowe promieniste, które pełnią rolę rusztowania i kierują nowo powstającymi neuronami, były rozrzucone po całej tkance zamiast tworzyć schludne, spolaryzowane warstwy. Progenitory pośrednie i neurony pojawiały się wcześniej, a następnie wcześniej zanikały, co sugeruje, że progenitory zostały popchnięte do zbyt szybkiej różnicowania. Po 60 dniach ogólna liczba neuronów wyrównała się, ale wczesne rozregulowanie czasowe i dezorganizacja wskazują na zaburzoną „mapę” budowy obwodów korowych, a nie na całkowitą niezdolność do wytwarzania neuronów.
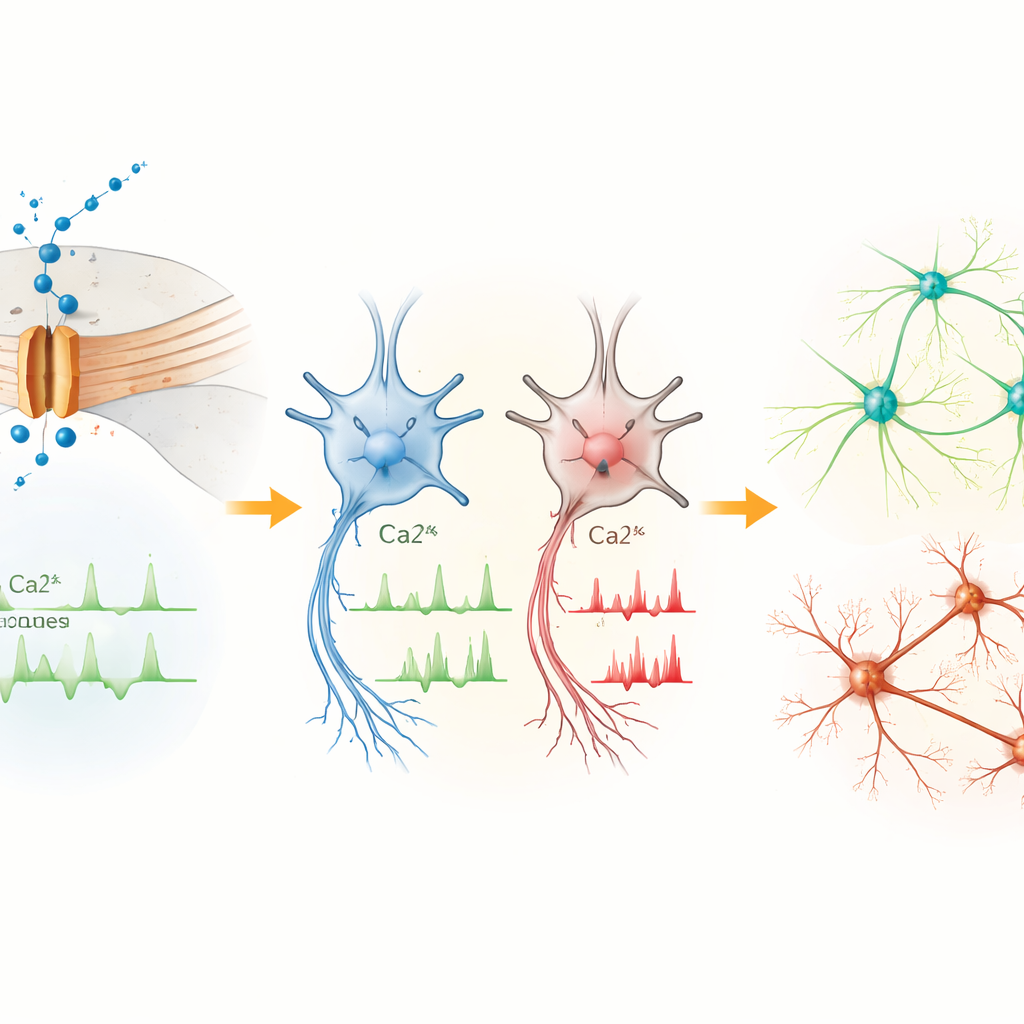
Aktywność genów przesuwa się w stronę programów ryzyka neurorozwojowego
Aby zrozumieć, jak zmienione gospodarowanie wapniem wpływa na kontrolę genów, zespół sekwencjonował RNA z komórek pacjentki i kontroli na różnych etapach. Różnice były niewielkie w komórkach macierzystych, ale narastały w progenitorach i neuronach wraz ze wzrostem ekspresji Cav1.3. Wiele genów zwiększało lub zmniejszało ekspresję w komórkach pacjentki i bierze udział w kontroli transkrypcji, rozwoju mózgu i neurogenezie. Kilka z nich, w tym PTN, MEIS2, POU3F2, CNTN4, CNTNAP2 i AUTS2, to znane geny ryzyka autyzmu i powiązanych zaburzeń neurorozwojowych. Te zmiany sugerują, że nieprawidłowy napływ wapnia przez Cav1.3 przekształca programy zależne od aktywności, które kierują proliferacją, migracją i łączeniem się komórek mózgowych.
Co to oznacza dla pacjentów i przyszłych terapii
Mówiąc prościej, praca ta pokazuje, jak pojedynczy wariant kanału wapniowego może najpierw nadmiernie pobudzać wczesne komórki mózgowe, potem osłabiać dojrzałe neurony, jednocześnie wypychając sieci genowe związane z zaburzeniami neurorozwojowymi z właściwej trajektorii. Efektem jest mózg, który z zewnątrz może wydawać się w dużej mierze normalny, ale zbudowany z obwodów rozwijających się zbyt szybko i zorganizowanych niedoskonałe. Odtworzenie tej mutacji pacjenta w ludzkich komórkach i organoidach daje szczegółową mapę łączącą defekt molekularny ze zmienionym sygnalizowaniem komórkowym, architekturą tkankową i regulacją genów. Ten model oferuje teraz platformę do testowania ukierunkowanych leków i strategii genetycznych mających na celu przywrócenie bardziej prawidłowego sygnalizowania wapniowego w kanałopatiach związanych z Cav1.3.
Cytowanie: Tisch, M., Geisler, S.M., Gabassi, E. et al. Aberrant calcium signaling and neuronal activity in the L271H CACNA1D (Cav1.3) iPSC model of neurodevelopmental disease. Mol Psychiatry 31, 2927–2940 (2026). https://doi.org/10.1038/s41380-025-03429-8
Słowa kluczowe: kanały wapniowe, zaburzenia neurorozwojowe, indukowane komórki pluripotentne, organoidy mózgowe, geny ryzyka autyzmu