Clear Sky Science · it
Segnalazione del calcio aberrante e attività neuronale nel modello iPSC L271H CACNA1D (Cav1.3) di malattia neuroevolutiva
Quando una singola variazione genica riverbera nello sviluppo cerebrale
Variazioni rare nei geni possono modificare in modo sottile il modo in cui le cellule cerebrali gestiscono segnali elettrici e chimici. Questo studio segue una di queste varianti in un gene dei canali del calcio associata a ritardo dello sviluppo, crisi epilettiche e sintomi simili all’autismo. Trasformando le cellule del sangue di una paziente in cellule staminali e poi in tessuti cerebrali in miniatura e neuroni in vitro, i ricercatori tracciano come una piccola alterazione molecolare possa distorcere lo sviluppo cerebrale precoce e l’attività neuronale.
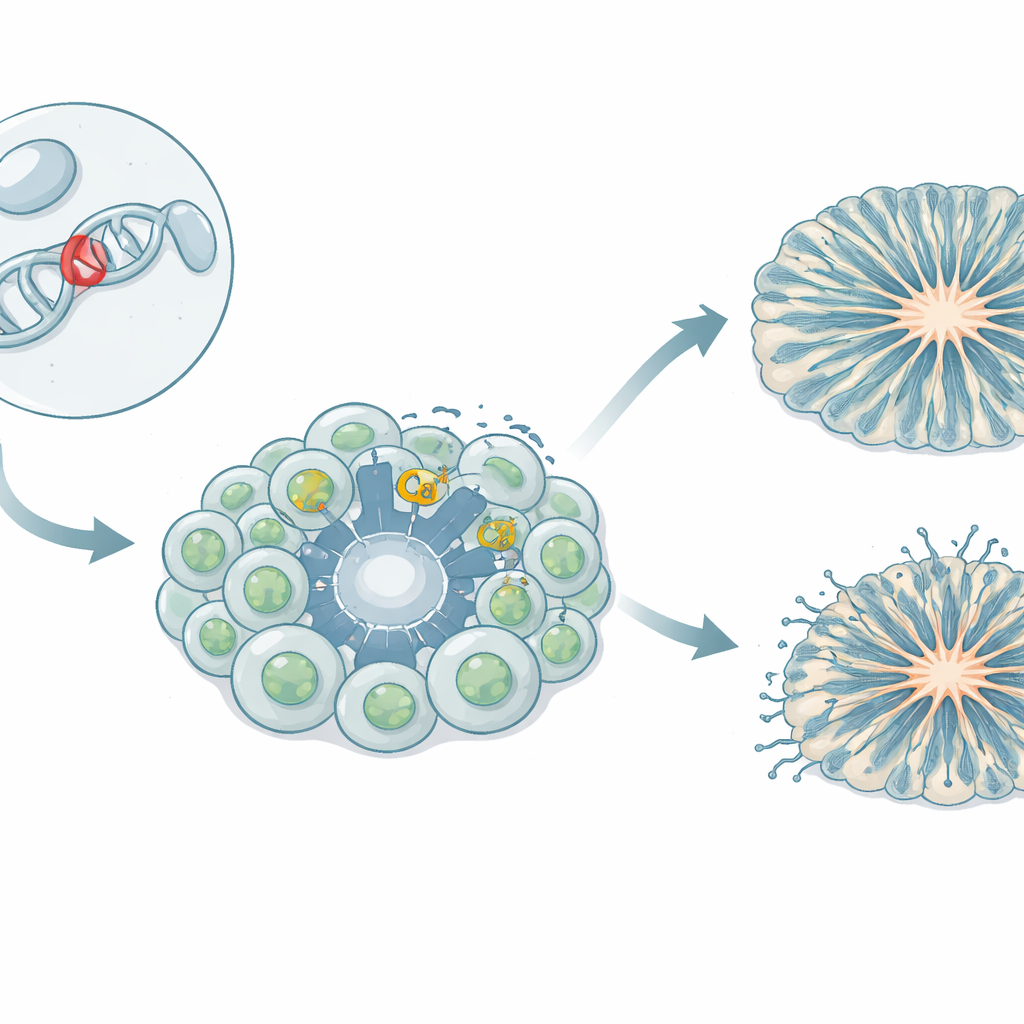
Guardiani che lasciano entrare il calcio nelle cellule cerebrali
Le cellule del cervello dipendono da un flusso controllato di ioni calcio per crescere, comunicare tra loro e attivare o disattivare geni. «Cancelli» specializzati nella membrana cellulare, chiamati canali del calcio voltaggio‑dipendenti, si aprono durante l’attività elettrica e permettono l’ingresso del calcio. Uno di questi canali, noto come Cav1.3, è importante in molti organi, compreso il cervello e i tessuti che producono ormoni. In diversi pazienti, rare varianti ereditarie del gene Cav1.3 sono state associate a un insieme di sintomi: squilibri ormonali, debolezza muscolare, crisi, ritardo dello sviluppo e tratti dello spettro autistico. La variante studiata qui, chiamata L271H, era stata mostrata in cellule non neuronali rendere il canale più facile da aprire, ma il suo impatto sulle cellule cerebrali umane era sconosciuto.
Costruire cellule cerebrali specifiche del paziente in laboratorio
Il gruppo ha creato un modello iPSC in cui le cellule del sangue di una ragazza portatrice della variante L271H sono state riprogrammate in cellule staminali capaci di formare qualsiasi tessuto. Queste cellule staminali pluripotenti indotte sono state poi indirizzate a diventare progenitori neurali—i primi mattoni che poi generano neuroni—e neuroni del tronco encefalico medio correlati alla segnalazione dopaminergica. I ricercatori hanno anche coltivato organoidi corticali tridimensionali, piccole «mini‑cervelli» che imitano le fasi iniziali della formazione della corteccia umana. Confrontando le cellule derivate dalla paziente con diverse linee di controllo da donatrici sane, hanno potuto separare gli effetti della variante dalla variazione genetica naturale.
Le cellule precoci segnalano troppo, i neuroni maturi sparano troppo poco
Nei progenitori neurali più precoci, il canale Cav1.3 era la forma dominante di questo tipo di canale del calcio. Le cellule portatrici della variante L271H mostravano più frequenti ondate spontanee di calcio rispetto ai controlli, pur avendo proprietà elettriche di base simili. Questo suggerisce che, a questo stadio, la variante disturbi principalmente l’equilibrio del calcio intracellulare piuttosto che provocare un evidente aumento dell’emissione di impulsi elettrici. Man mano che le cellule maturavano in neuroni del mesencefalo, il quadro si capovolgeva. Sebbene un altro tipo di canale del calcio diventasse complessivamente più abbondante, i neuroni con la variante L271H mostravano meno picchi di calcio, uno stato di riposo più depolarizzato e risultavano più difficili da indurre a scariche ripetute. I loro potenziali d’azione erano più piccoli e più lenti a salire e scendere, indicando che la variante alla fine attenua la capacità dei neuroni di inviare segnali elettrici robusti.
Mini‑cervelli che crescono più in fretta ma si organizzano male
Negli organoidi corticali, la variante L271H lasciava un’impronta netta sulla struttura. Rispetto ai controlli, gli organoidi derivati dalla paziente avevano cavità simili a ventricoli meno numerose e di dimensioni inferiori—zone ad anello dove i progenitori normalmente si dispongono in modo ordinato. Le cellule gliali radiali, che fungono da impalcatura e guidano i neuroni neonati, erano sparse nel tessuto invece di formare strati polarizzati e ordinati. I progenitori intermedi e i neuroni apparivano prima e poi declinavano più presto, suggerendo che i progenitori venivano spinti a differenziarsi troppo rapidamente. Entro 60 giorni, il numero totale di neuroni raggiungeva valori comparabili, ma il disallineamento temporale iniziale e la disorganizzazione indicano un progetto disturbato per la costruzione dei circuiti corticali piuttosto che un’insufficienza assoluta nella produzione di neuroni.
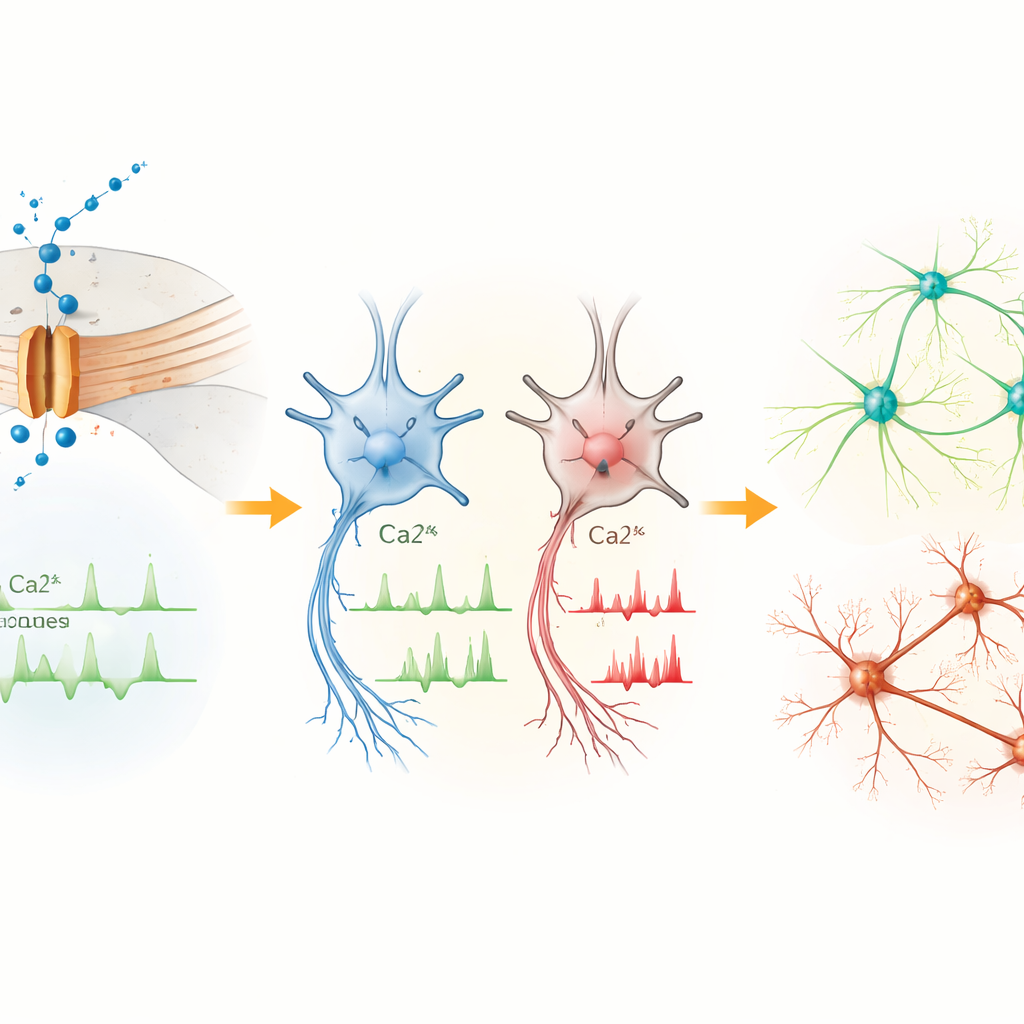
L’attività genica si sposta verso programmi di rischio neuroevolutivo
Per capire come la gestione alterata del calcio influisca sul controllo genico, il gruppo ha sequenziato l’RNA delle cellule di paziente e dei controlli in diverse fasi. Le differenze erano modeste nelle cellule staminali ma aumentavano nei progenitori e nei neuroni all’aumentare dell’espressione di Cav1.3. Molti geni up‑ o down‑regolati nelle cellule della paziente sono coinvolti nel controllo della trascrizione, nello sviluppo cerebrale e nella neurogenesi. Diversi di essi, tra cui PTN, MEIS2, POU3F2, CNTN4, CNTNAP2 e AUTS2, sono noti geni di rischio per l’autismo e condizioni neuroevolutive correlate. Questi cambiamenti suggeriscono che l’ingresso anomalo di calcio attraverso Cav1.3 rimodella programmi genici dipendenti dall’attività che guidano la proliferazione, la migrazione e l’integrazione delle cellule cerebrali.
Cosa significa per i pazienti e per terapie future
In sintesi, questo lavoro mostra come una singola variante di un canale del calcio possa prima sovrastimolare le cellule cerebrali precoci, poi lasciare i neuroni maturi sotto‑alimentati, spingendo al contempo reti geniche associate a disturbi neuroevolutivi fuori dal loro corso. Il risultato è un cervello che può apparire in gran parte normale dall’esterno ma costruito a partire da circuiti che si sono sviluppati troppo in fretta e si sono organizzati in modo imperfetto. Ricreando la mutazione di questa paziente in cellule umane e organoidi, lo studio fornisce una mappa dettagliata che collega un difetto molecolare a segnali cellulari alterati, architettura tissutale e regolazione genica. Questo modello offre ora una piattaforma per testare farmaci mirati e strategie genetiche volte a ripristinare una segnalazione del calcio più normale nelle canalopatie correlate a Cav1.3.
Citazione: Tisch, M., Geisler, S.M., Gabassi, E. et al. Aberrant calcium signaling and neuronal activity in the L271H CACNA1D (Cav1.3) iPSC model of neurodevelopmental disease. Mol Psychiatry 31, 2927–2940 (2026). https://doi.org/10.1038/s41380-025-03429-8
Parole chiave: canali del calcio, disturbi neuroevolutivi, cellule staminali pluripotenti indotte, organoidi cerebrali, geni di rischio per l’autismo