Clear Sky Science · zh
并行化液滴微流控机械穿孔实现稳健且抗堵塞的细胞内基因递送
这对未来药物有什么重要意义
许多最令人兴奋的新疗法——例如基因编辑和基于mRNA的治疗——都依赖将脆弱的生物分子安全地送入活细胞内。现有方法虽然强大,但常常会损伤细胞、在不同细胞类型间表现不一致,或难以扩展到治疗所需的数十亿细胞规模。本文介绍了一种基于微芯片的新方法,能够高效、温和且超高通量地将遗传物质递送到细胞,同时解决了一个顽固的实际问题:器件在运行中发生堵塞和失效。
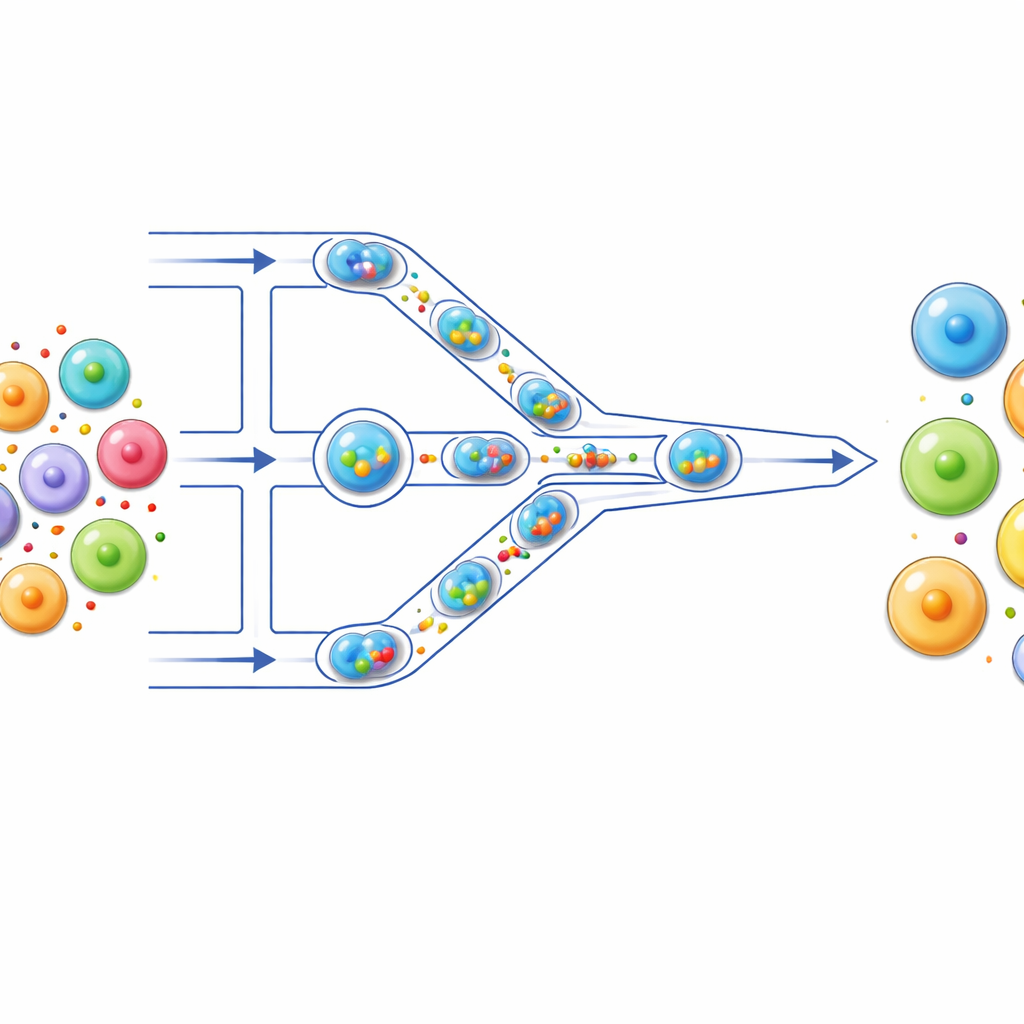
一个为细胞设计的小型装配线
作者构建了一个微流控“装配线”,细胞沿着透明芯片上的极细通道移动。首先,每个细胞连同其载荷——例如荧光染料、mRNA或CRISPR组件——被封装在由油包裹的微小水滴中。这些液滴像独立的反应容器,保持每个细胞及其载荷相互隔离。当液滴被推动通过通道时,会遇到一系列比细胞本身更窄的狭窄收缩区。当液滴被挤压通过时,内部的细胞会短暂变形,然后恢复,这一循环在通过多个收缩区时重复发生。
温和挤压如何打开细胞之门
当柔软的细胞被迫通过比其直径更窄的收缩区时,细胞膜会被拉伸,形成暂时的纳米级开口。由于细胞位于快速通过收缩区的液滴内,流体在细胞表面流动并将载荷分子推动通过这些微小开口进入细胞内。一旦液滴离开窄区,细胞恢复圆形,细胞膜重新封闭,此时载荷被困在细胞内部。高速成像和定量测量显示,提高流速和精心选择收缩尺寸能增加膜拉伸和递送效率,但研究者调节这些参数,使大多数细胞——超过80%——仍然存活且健康。
一种抗堵塞的智能设计
将此类芯片用于实验室外的一个主要障碍是堵塞:尘粒、细胞团聚或材料碎片可能堵住单一窄通道并使系统停摆。为了解决这一问题,研究团队将许多收缩区并联排列,并用旁路通道将它们连接,使得流动可以绕过阻塞重新分配。该并行互联的布局稳定了芯片内部的压力,即便某些通路部分堵塞也能保持液滴移动。对比有无旁路的芯片测试表明,新设计不仅在堵塞事件中保持了高递送效率,还提高了每个细胞接收的物质量,而对细胞存活率的影响仅为温和程度。
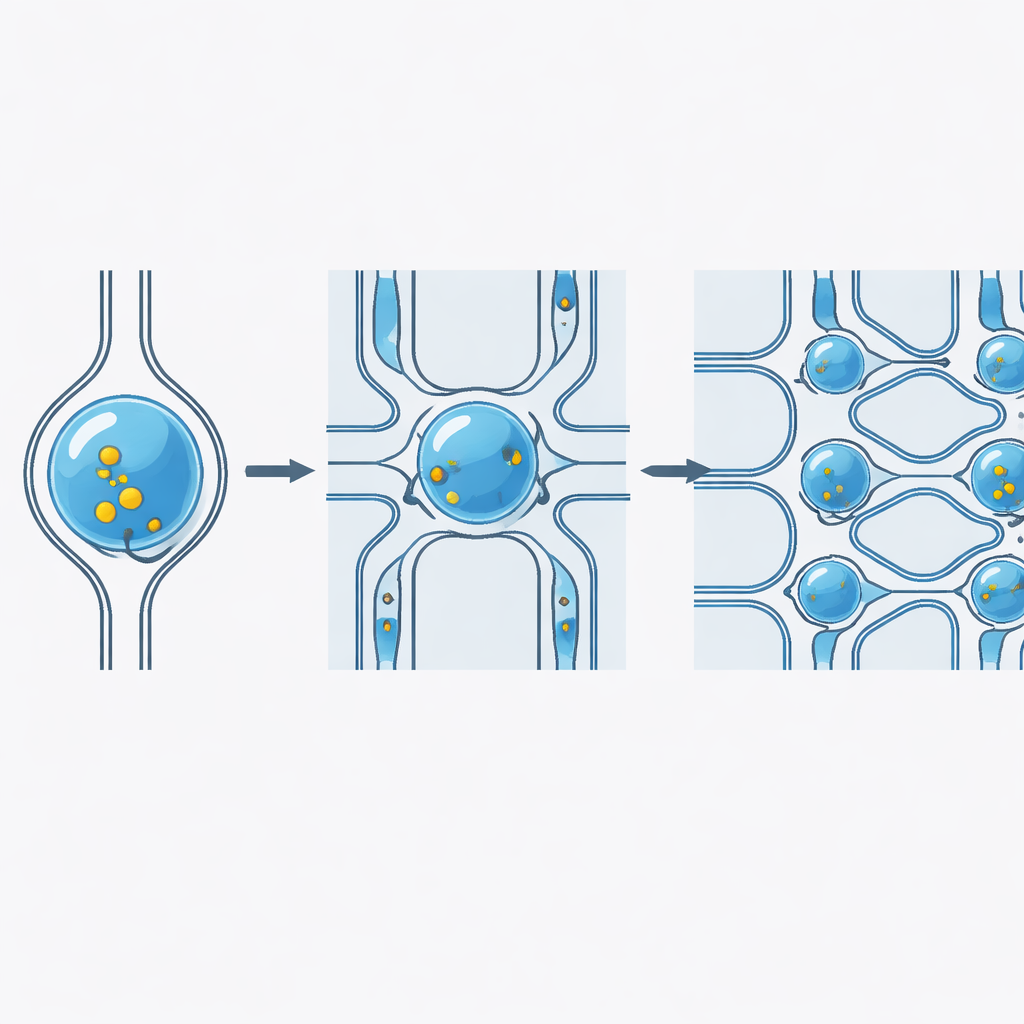
适用于多种载荷、细胞类型和速度
研究者系统地探查了该平台在真实条件下的表现。他们递送了尺寸差别很大的荧光分子,从小分子染料到大分子聚合物,并持续达到了超过98%的递送效率,且进入每个细胞的量可通过载荷浓度加以控制。通过调整收缩宽度以匹配细胞的大小和刚性,该芯片能在多种人类和动物细胞系上工作,包括来源于血液的细胞和贴壁细胞。即使在每小时处理高达1亿个细胞时,性能仍保持稳定,这表明该器件可以应对细胞治疗所需的细胞数量,而不丧失效率或细胞活力。
从发光蛋白到基因编辑
为展示实际影响,作者将编码荧光蛋白的mRNA递送到白血病细胞,并将他们的方法与两种常见的非病毒技术进行了比较:基于脂质的转染和电穿孔。他们的液滴挤压芯片在表达蛋白的细胞比例和表达强度两方面匹配或超过了电穿孔,同时比这两种替代方法保留了更多存活细胞。随后,他们使用该平台将CRISPR/Cas9基因编辑复合体递送到T细胞以敲除一个关键的表面受体。编辑在超过99%的细胞中成功,目标受体的荧光信号下降了二十倍以上,且数天内细胞活力仍保持在80%以上。
这对未来细胞工程意味着什么
简单来说,这项研究表明,通过巧妙设计且抗堵塞的微通道阵列温和地将液滴封装的细胞挤压过去,几乎可以将遗传载荷装入所有细胞,同时保持大多数细胞存活,并能以工业相关的速度完成。该平台可处理不同分子和细胞类型,其性能可与或优于标准的非病毒方法,并可通过增加通道和液滴发生器进行扩展。结合改进的细胞回收步骤,这种方法有望成为制造工程化治疗细胞的实用主力,也可作为需要对大量细胞群体进行可靠、定量递送的基础研究的多功能工具。
引用: Liu, Q., Chung, A.J. Parallelized droplet microfluidic mechanoporation enables robust and clogging-resistant intracellular gene delivery. Microsyst Nanoeng 12, 157 (2026). https://doi.org/10.1038/s41378-026-01273-6
关键词: 微流控基因递送, 液滴机械穿孔, 细胞内mRNA转染, CRISPR细胞工程, 抗堵塞微器件