Clear Sky Science · fr
La mécanoporotion microfluidique par gouttelettes parallélisée permet une délivrance génétique intracellulaire robuste et résistante aux obstructions
Pourquoi cela compte pour les médicaments de demain
Beaucoup des thérapies les plus prometteuses — comme l'édition génomique et les traitements à base d'ARNm — reposent sur l'introduction sûre de biomolécules fragiles à l'intérieur de cellules vivantes. Les méthodes actuelles peuvent être puissantes mais endommagent souvent les cellules, sont peu fiables selon les types cellulaires, ou sont difficiles à mettre à l'échelle pour atteindre les milliards de cellules nécessaires aux thérapies. Cet article présente une nouvelle approche sur puce qui délivre du matériel génétique dans les cellules de manière efficace, douce et à très haut débit, tout en résolvant un problème pratique persistant : l'obstruction et la défaillance des dispositifs en fonctionnement.
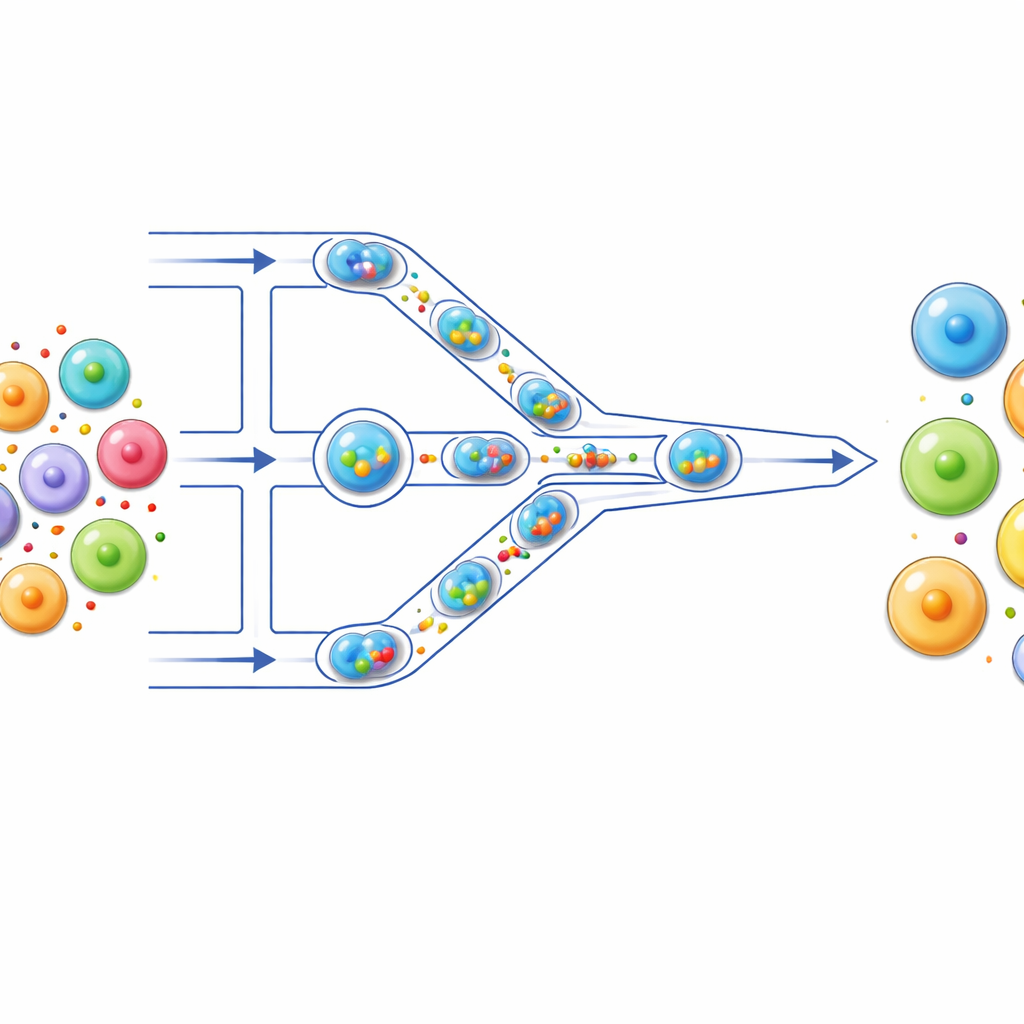
Une petite chaîne de production pour cellules
Les auteurs ont construit une « chaîne de montage » microfluidique où les cellules circulent dans des canaux aussi fins qu'un cheveu sur une puce transparente. D'abord, chaque cellule est encapsulée avec sa cargaison — par exemple un colorant fluorescent, de l'ARNm ou des composants CRISPR — à l'intérieur d'une goutte microscopique d'eau entourée d'huile. Ces gouttes jouent le rôle de micro‑réacteurs individuels, isolant chaque cellule et son contenu. Lorsque les gouttes sont poussées le long du canal, elles rencontrent une série de constrictions étroites plus petites que les cellules elles‑mêmes. Quand une goutte se faufile, la cellule à l'intérieur est brièvement déformée puis se relâche, un cycle qui se répète plusieurs fois en franchissant plusieurs constrictions.
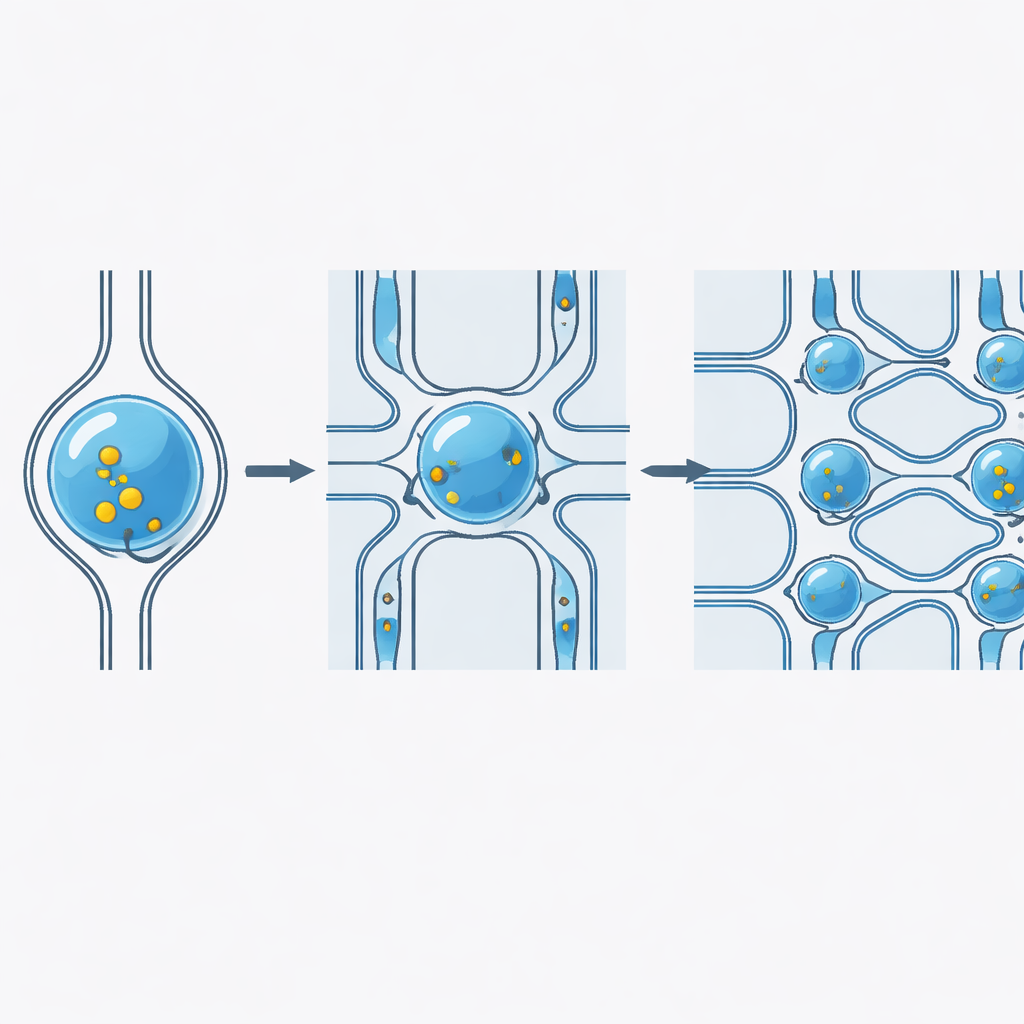
Comment le pincement doux ouvre la porte cellulaire
Quand une cellule souple est forcée à travers une constriction plus étroite que son diamètre, sa membrane s'étire, formant des ouvertures temporaires à l'échelle nanométrique. Parce que la cellule est enfermée dans une goutte se déplaçant rapidement à travers la constriction, des flux de fluide balaient sa surface et poussent les molécules cargo à travers ces petites ouvertures vers l'intérieur cellulaire. Une fois la goutte sortie de la zone étroite, la cellule reprend sa forme ronde et la membrane se referme, avec la cargaison désormais piégée à l'intérieur. Des images à grande vitesse et des mesures quantitatives ont montré que des vitesses d'écoulement plus élevées et des tailles de constriction bien choisies augmentent l'étirement membranaire et la délivrance, mais les chercheurs ont ajusté ces paramètres pour que la plupart des cellules — plus de 80 % — restent vivantes et en bonne santé.
Une conception intelligente qui résiste aux obstructions
Un obstacle majeur à l'utilisation de telles puces hors laboratoire est l'obstruction : poussière, amas cellulaires ou débris peuvent bloquer un canal étroit et arrêter le système. Pour y remédier, l'équipe a disposé de nombreuses constrictions en parallèle et les a reliées par des canaux de dérivation qui permettent à l'écoulement de contourner les obstructions. Cette configuration parallèle et interconnectée stabilise la pression à l'intérieur de la puce et maintient le mouvement des gouttes même lorsque certaines voies sont partiellement bloquées. Des tests comparant des puces avec et sans dérivation ont montré que le nouveau design non seulement conservait une efficacité de délivrance élevée lors d'événements d'obstruction, mais améliorait aussi la quantité de matière reçue par chaque cellule, avec seulement des effets modestes sur la survie cellulaire.
Fonctionne avec plusieurs cargaisons, types cellulaires et débits
Les chercheurs ont étudié systématiquement le comportement de la plateforme dans des conditions proches du réel. Ils ont délivré des molécules fluorescentes de tailles très différentes, des petits colorants aux grands polymères, et ont obtenu de manière constante des efficacités de délivrance supérieures à 98 %, la quantité entrant dans chaque cellule étant contrôlée par la concentration de cargaison. La puce a fonctionné sur une gamme de lignées cellulaires humaines et animales, y compris des cellules dérivées du sang et des cellules adhérentes, en ajustant la largeur des constrictions pour correspondre à la taille et à la rigidité des cellules. Les performances sont restées stables même en traitant jusqu'à 100 millions de cellules par heure, ce qui indique que le dispositif peut gérer les effectifs cellulaires requis pour les thérapies cellulaires sans perdre en efficacité ni en viabilité cellulaire.
Des protéines fluorescentes aux gènes édités
Pour démontrer l'impact pratique, les auteurs ont délivré de l'ARNm codant une protéine fluorescente dans des cellules leucémiques et ont comparé leur méthode à deux techniques non virales courantes : la transfection lipidique et l'électroporation. Leur puce à pincement par gouttelettes égalait ou dépassait l'électroporation tant pour la fraction de cellules exprimant la protéine que pour l'intensité d'expression, tout en maintenant davantage de cellules en vie que les deux alternatives. Ils ont ensuite utilisé la plateforme pour délivrer des complexes d'édition CRISPR/Cas9 dans des cellules T afin d'inactiver un récepteur de surface clé. L'édition a réussi dans plus de 99 % des cellules, avec des signaux fluorescents du récepteur ciblé diminuant de plus de vingt fois, et la viabilité cellulaire restant supérieure à 80 % sur plusieurs jours.
Ce que cela signifie pour l'ingénierie cellulaire future
En termes simples, cette étude montre que le pincement doux de cellules encapsulées dans des gouttes, à travers un réseau de microcanaux astucieusement conçu et résistant aux obstructions, peut charger du matériel génétique dans presque toutes les cellules tout en en conservant la majorité, et ce à des vitesses pertinentes pour l'industrie. La plateforme prend en charge différentes molécules et types cellulaires, rivalise avec — voire surpasse — les méthodes non virales standard, et peut être montée en échelle en ajoutant des canaux et des générateurs de gouttes. Avec des étapes améliorées de récupération cellulaire, cette approche pourrait devenir un outil de travail pratique pour la production de cellules modifiées destinées aux thérapies, ainsi qu'un instrument polyvalent pour la recherche fondamentale nécessitant une délivrance fiable et quantitative dans de grandes populations cellulaires.
Citation: Liu, Q., Chung, A.J. Parallelized droplet microfluidic mechanoporation enables robust and clogging-resistant intracellular gene delivery. Microsyst Nanoeng 12, 157 (2026). https://doi.org/10.1038/s41378-026-01273-6
Mots-clés: transfert génétique microfluidique, mécanoporotion par gouttelettes, transfection d'ARNm intracellulaire, ingénierie cellulaire CRISPR, microdispositifs résistants aux obstructions