Clear Sky Science · ar
تمكين الميكانوبوراشن المجهري المتوازي للقطرات لتوصيل الجينات داخل الخلايا بمقاومة عالية للانسداد
لماذا هذا مهم لأدوية المستقبل
العديد من أهم العلاجات الجديدة — مثل تحرير الجينات والعلاجات القائمة على mRNA — تعتمد على إدخال جزيئات حيوية حساسة إلى داخل الخلايا الحية بأمان. الطرق الحالية قد تكون فعالة لكنها غالباً ما تُلحق ضرراً بالخلايا، تعمل بتباين بين أنواع الخلايا، أو يصعب توسيعها لتغطي بلايين الخلايا المطلوبة للعلاجات. تقدم هذه الورقة نهجاً جديداً قائمًا على شرائح ميكروفلويديك يتيح توصيل المواد الجينية إلى الخلايا بكفاءة ولطف ومعدل تدفق عالٍ جداً، مع حل مشكلة عملية مزمنة: انسداد الأجهزة وتعطلها أثناء التشغيل.
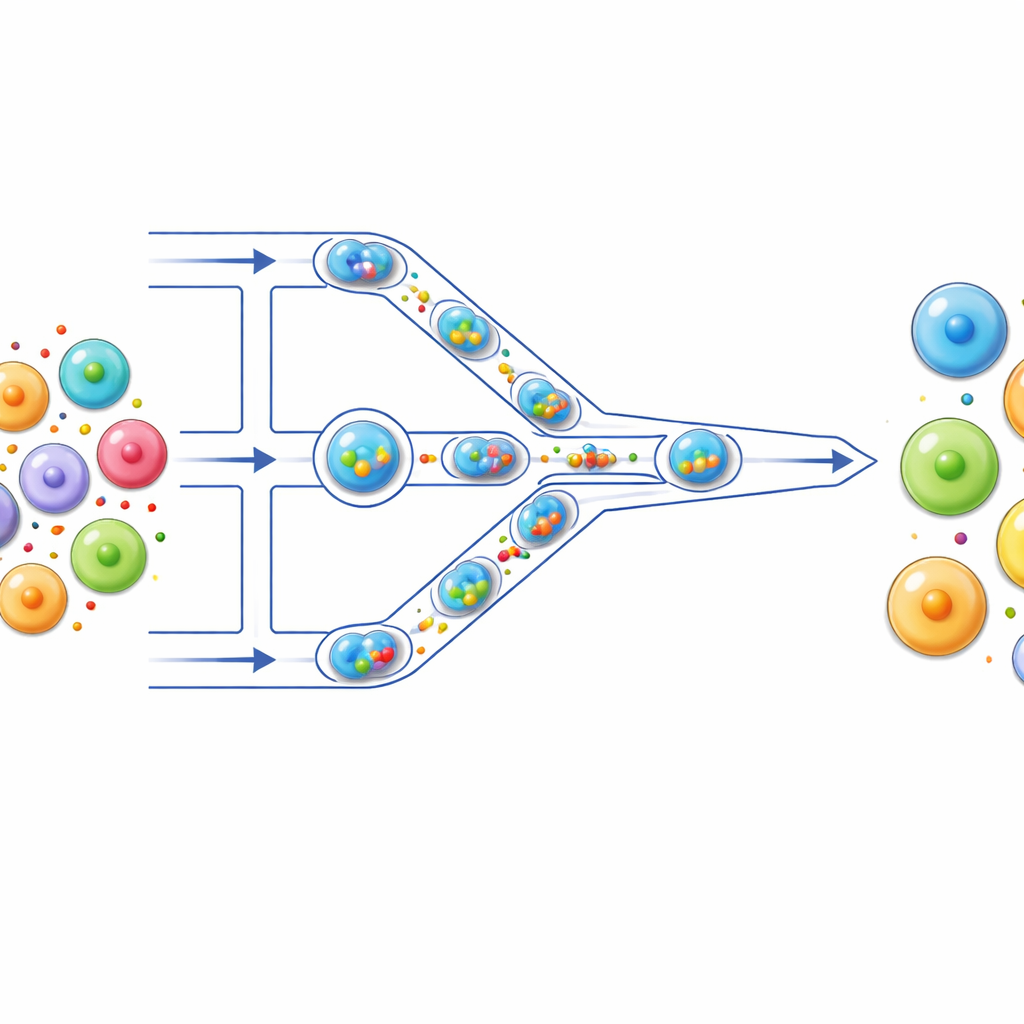
خط تجميع صغير للخلايا
بنى المؤلفون "خط تجميع" ميكروفلويديك حيث تنتقل الخلايا عبر قنوات رفيعة كالخيوط على شريحة شفافة. أولاً، تُحاط كل خلية وشحنتها — مثل صبغة فلورية، mRNA، أو مكونات CRISPR — داخل قطرة مائية مجهرية مغلفة بالزيت. تعمل هذه القطرات كأوعية تفاعل منفصلة، تحافظ على عزل كل خلية وشحنتها. أثناء دفع القطرات على طول القناة، تصادف سلسلة من التضييقات الضيقة التي أصغر من الخلايا نفسها. عندما تضيق القطرة وتعبر، تُشوه الخلية داخلها مؤقتًا ثم تسمح لها بالاسترخاء، وتتكرر هذه الدورة عدة مرات أثناء مرورها عبر تضييقات متعددة.
كيف يفتح العصر اللطيف باب الخلية
عندما تُجبر خلية رخوة على المرور عبر تضييق أضيق من قطرها، يتمدد غشاؤها مكوِّناً فتحات نانوية مؤقتة. وبما أن الخلية داخل قطرة تتحرك بسرعة عبر التضييق، يتدفق السائل عبر سطح الخلية ويدفع جزيئات الشحنة عبر هذه الفتحات الصغيرة إلى داخل الخلية. بمجرد خروج القطرة من المنطقة الضيقة، تعود الخلية إلى شكلها الكروي ويُغلق الغشاء من جديد، مع احتجاز الشحنة داخل الخلية. أظهرت تصويرات عالية السرعة وقياسات كمية أن معدلات التدفق الأعلى وأحجام التضييق المختارة بعناية تزيد من تمدد الغشاء والتوصيل، لكن الباحثين ضبطوا هذه المعاملات بحيث تبقى غالبية الخلايا — أكثر من 80% — حية وبصحة جيدة.
تصميم ذكي يقاوم الانسدادات
حاجز رئيسي أمام استخدام هذه الشرائح خارج المختبر هو الانسداد: الغبار، تكتلات الخلايا، أو قطع المواد قد تسد قناة ضيقة واحدة وتوقف النظام. للتغلب على ذلك، رتب الفريق العديد من التضييقات بالتوازي وربطها بقنوات تجاوز تسمح بتغيير مجرى التدفق حول العوائق. هذا التخطيط المتوازي المترابط يثبت الضغط داخل الشريحة ويحافظ على حركة القطرات حتى عندما تُسد بعض المسارات جزئياً. أظهرت الاختبارات مقارنةً بين شرائح مع وبدون قنوات تجاوز أن التصميم الجديد لم يحافظ فقط على كفاءة التوصيل أثناء أحداث الانسداد، بل حسّن أيضاً كمية المادة التي تستلمها كل خلية، مع تأثيرات متواضعة فقط على بقاء الخلايا.
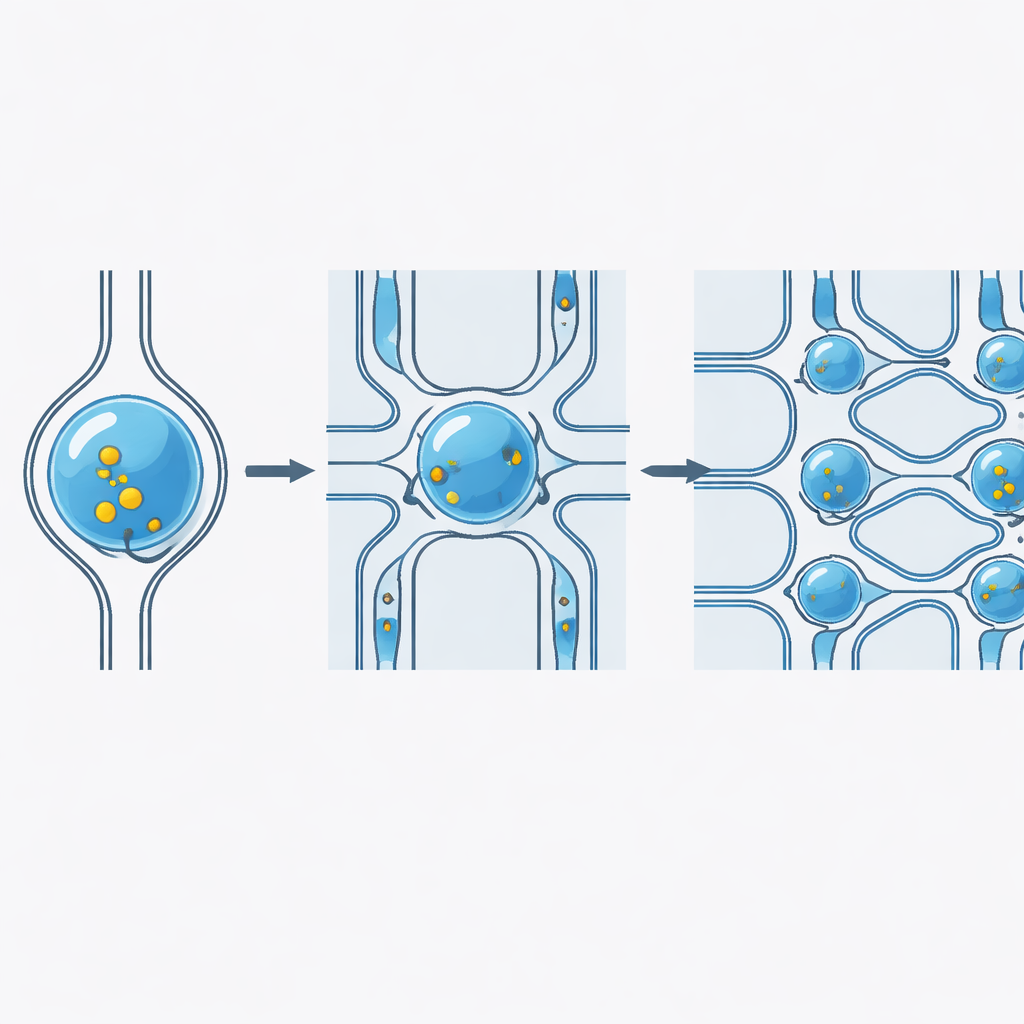
يعمل عبر حمولات وأنواع خلايا وسرعات مختلفة
استقصى الباحثون منهجياً كيف يتصرف النظام في ظروف العالم الحقيقي. قاموا بتوصيل جزيئات فلورية ذات أحجام مختلفة جداً، من أصباغ صغيرة إلى بوليمرات كبيرة، وحققوا باستمرار كفاءات توصيل أعلى من 98%، مع التحكم في كمية ما يدخل كل خلية عن طريق تركيز الحمولة. عملت الشريحة على مجموعة من خطوط الخلايا البشرية والحيوانية، بما في ذلك الخلايا المشتقة من الدم والخلايا الملتحمة بالسطح، عبر تعديل عرض التضييق لمطابقة حجم الخلية وصلابتها. بقي الأداء مستقراً حتى عند معالجة ما يصل إلى 100 مليون خلية في الساعة، مما يشير إلى أن الجهاز يمكنه التعامل مع أعداد الخلايا المطلوبة للعلاجات الخلوية دون فقدان للكفاءة أو لبقاء الخلايا.
من البروتينات المتوهجة إلى الجينات المعدلة
لإظهار التأثير العملي، سلَّم المؤلفون mRNA يُرمّز بروتيناً فلوريسينياً إلى خلايا سرطان دم وقارنوا طريقتهم بطريقتين غير فيروسيتين شائعتين: التحويل المعتمد على الدهون والتفريغ الكهربائي. طابقت شريحة العصر بالقطرات أو تفوقت على التفريغ الكهربائي من حيث نسبة الخلايا المعبرة عن البروتين وشدة التعبير، مع إبقاء خلايا أكثر حيوية مقارنةً بأي من البديلين. ثم استخدموا النظام لتوصيل مركبات تحرير الجينات CRISPR/Cas9 إلى خلايا T لتعطيل مستقبل سطحي رئيسي. نجحت التعديلات في أكثر من 99% من الخلايا، مع انخفاض الإشارات الفلورية من المستقبل المستهدف بأكثر من عشرين ضعفاً، وبقاء الخلايا فوق 80% حية خلال عدة أيام.
ما الذي يعنيه هذا لهندسة الخلايا في المستقبل
بعبارات بسيطة، تظهر هذه الدراسة أن عصر الخلايا المغلفة بالقطرات برفق عبر مصفوفة قنوات ميكروية مصممة بذكاء ومقاومة للانسداد يمكن أن يحمّل الحمولة الجينية في كل خلية تقريباً مع الحفاظ على حيوية معظمها، ويمكنه القيام بذلك بسرعات ذات صلة صناعية. يتعامل النظام مع جزيئات وأنواع خلايا مختلفة، ينافس أو يتفوق على الطرق غير الفيروسية القياسية، ويمكن توسيعه بإضافة قنوات ومولِّدات قطرات إضافية. مع تحسين خطوات استرداد الخلايا، قد يصبح هذا النهج أداة عملية رئيسية لتصنيع الخلايا المهندسة للعلاجات، فضلاً عن أداة متعددة الاستخدامات للبحث الأساسي الذي يحتاج إلى توصيل موثوق وكمي إلى مجموعات خلوية كبيرة.
الاستشهاد: Liu, Q., Chung, A.J. Parallelized droplet microfluidic mechanoporation enables robust and clogging-resistant intracellular gene delivery. Microsyst Nanoeng 12, 157 (2026). https://doi.org/10.1038/s41378-026-01273-6
الكلمات المفتاحية: توصيل الجينات بالميكروفلويديك, ميكانوبوراشن بالقطرات, نقل mRNA داخل الخلايا, هندسة الخلايا بتقنية CRISPR, أجهزة ميكروية مقاومة للانسداد