Clear Sky Science · ja
並列化ドロップレットマイクロフルイディクス機械穿孔により堅牢で詰まりにくい細胞内遺伝子導入を実現
将来の医療にとってなぜ重要か
遺伝子編集やmRNAベースの治療のような最も期待される新規治療法の多くは、壊れやすい生体分子を生きた細胞の内部へ安全に届けることに依存しています。現在の手法は強力である一方、細胞を損傷しやすかったり、細胞種によって再現性に欠けたり、治療に必要な数十億の細胞へスケールアップするのが難しかったりします。本論文は、遺伝物質を効率的かつ穏やかに高スループットで細胞に送り込み、かつ実務上の厄介な問題であるデバイスの詰まりと動作停止を解決する新しいマイクロチップベースのアプローチを紹介します。
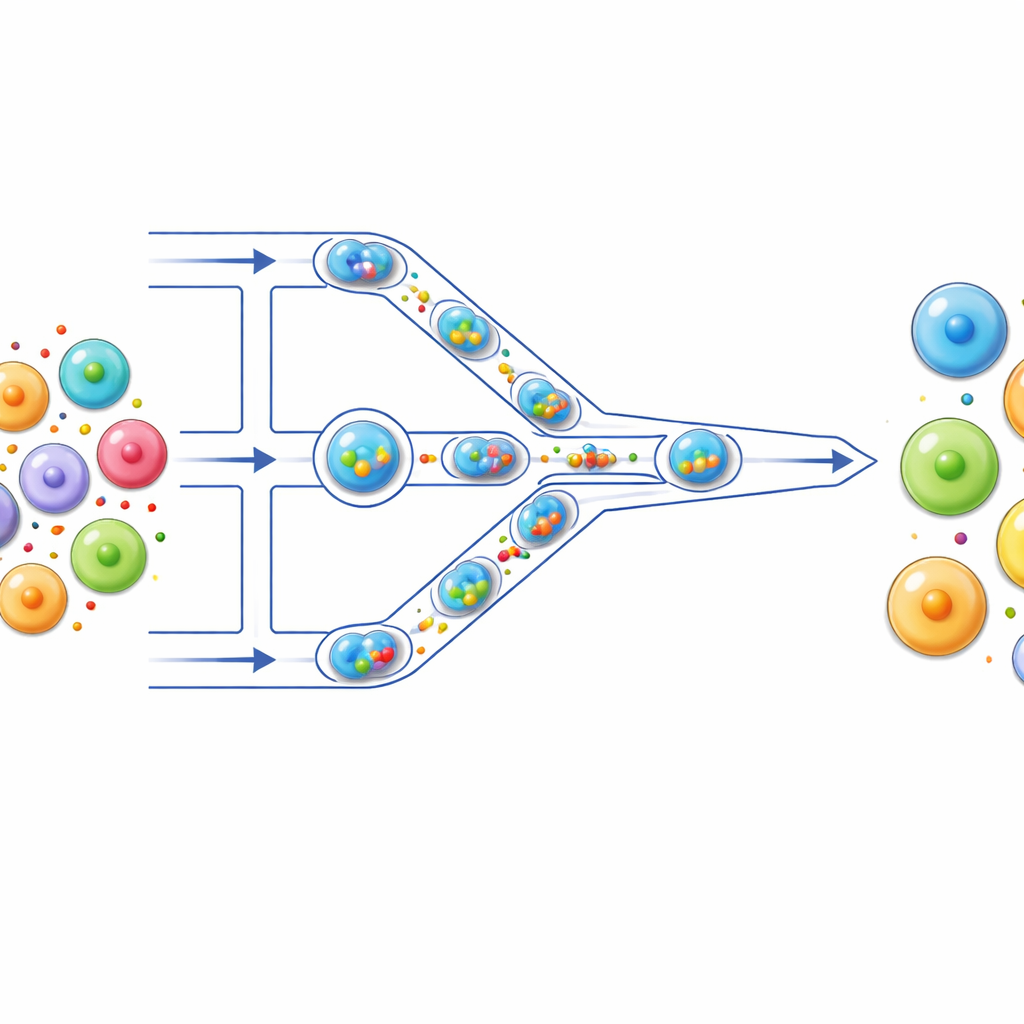
細胞のための小さな組立ライン
著者らは、細いチャネルを透明なチップ上で細胞が流れるマイクロフルイディクスの「組立ライン」を構築しました。まず、各細胞は蛍光色素、mRNA、あるいはCRISPR成分などの運搬物とともに、油で囲まれた微小な水滴内にパッケージされます。これらのドロップレットは個々の反応容器のように働き、各細胞とその搭載物を孤立させます。ドロップレットがチャネルを押し進められると、一連の細胞よりも狭い収縮部に遭遇します。ドロップレットが絞りを通過すると内部の細胞は一時的に変形し、その後緩和します。このサイクルは複数の収縮部を通過する間に繰り返されます。
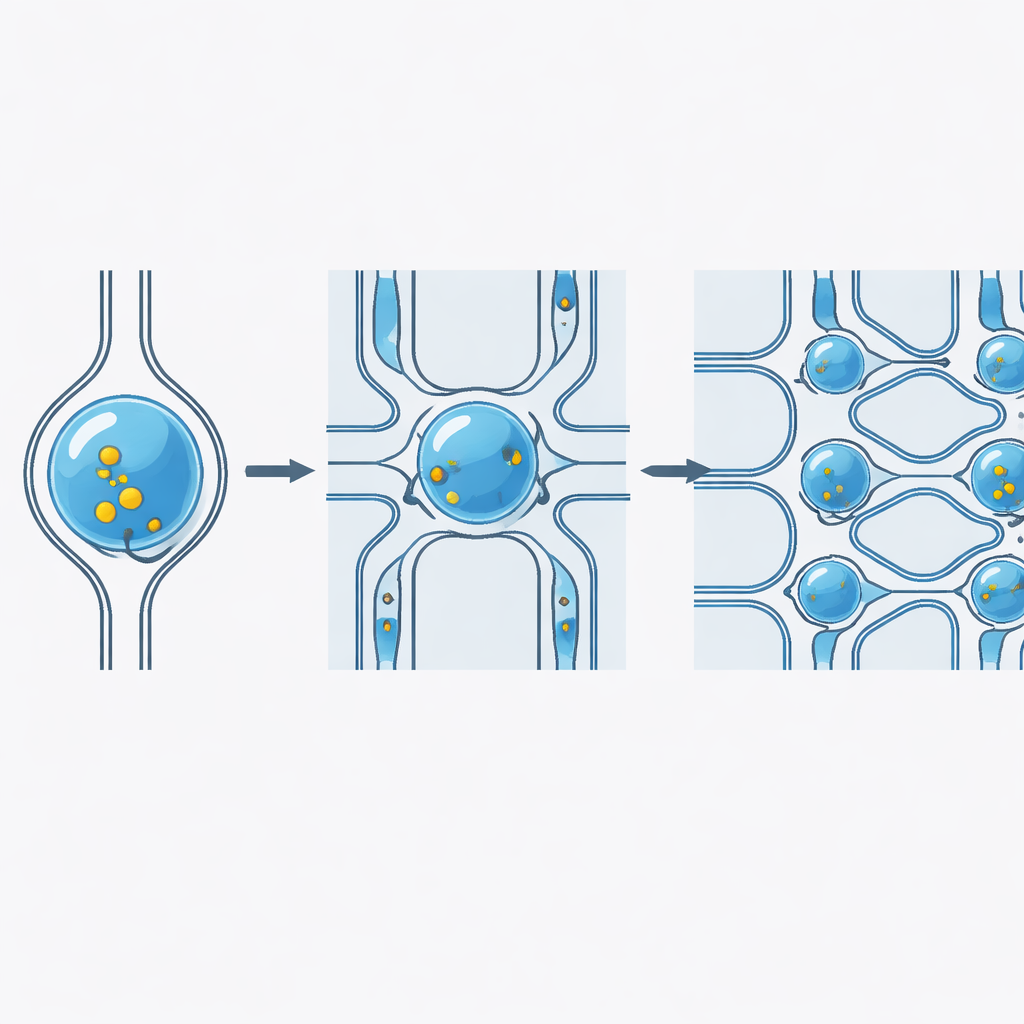
穏やかな圧迫が細胞の扉を開く仕組み
柔らかい細胞がその直径より狭い収縮部を通らされると、膜が伸張して一時的なナノスケールの開口が生じます。細胞がドロップレット内で高速に移動するため、細胞表面に流れが生じ、貨物分子がこれらの微小な開口を通って細胞内へ押し込まれます。ドロップレットが狭い領域を抜けると、細胞は元の球状に戻り膜が再封され、貨物は内部に閉じ込められます。高速撮影と定量測定により、より高い流速と慎重に選ばれた収縮幅が膜の伸張と導入効率を高めることが示されましたが、研究者らはこれらのパラメータを調整して大多数の細胞(80%以上)が生存かつ健全であるようにしました。
詰まりに強い賢い設計
この種のチップを研究室外で使う際の大きな障害は詰まりです:ほこり、細胞塊、あるいは微小片が単一の狭いチャネルを塞ぎシステムを停止させる可能性があります。これを克服するために、チームは多くの収縮部を並列に配置し、バイパスチャネルで相互接続して流れが障害物の周りを回避できるようにしました。この並列で相互接続されたレイアウトはチップ内部の圧力を安定させ、一部の経路が部分的に塞がれてもドロップレットの移動を維持します。バイパス有無のチップを比較した試験では、新しい設計は詰まりが発生した際にも導入効率を高く保つだけでなく、各細胞が受け取る物質量も改善し、細胞生存率への影響は控えめであることが示されました。
搭載物、細胞種、処理速度に幅広く対応
研究者らはプラットフォームが実世界の条件下でどのように振る舞うかを体系的に調べました。小さな色素から大きな高分子まで非常に異なるサイズの蛍光分子を導入し、一貫して98%以上の導入効率を達成し、各細胞に入る量は搭載物の濃度で制御できました。チップは血液由来細胞や接着性細胞を含むさまざまなヒトおよび動物の細胞株で機能し、収縮幅を細胞の大きさや剛性に合わせて調整することで対応しました。毎時最大1億個の細胞まで処理しても性能は安定しており、デバイスは細胞ベース治療に必要な細胞数を扱えることを示しています。効率や細胞生存率を失うことはありませんでした。
蛍光タンパク質の発現から遺伝子編集まで
実用的な影響を示すために、著者らは白血病細胞に蛍光タンパク質をコードするmRNAを導入し、自分たちの手法を脂質ベースのトランスフェクションと電気穿孔という二つの一般的な非ウイルス法と比較しました。ドロップレット圧搾チップは、タンパク質を発現する細胞の割合と発現強度の両面で電気穿孔に匹敵するか上回り、かつどちらの代替法よりも多くの細胞の生存を保ちました。続いてプラットフォームを用いてT細胞にCRISPR/Cas9遺伝子編集複合体を導入し、主要な表面受容体をノックアウトしました。その編集は99%以上の細胞で成功し、標的受容体からの蛍光信号は20倍以上低下し、細胞生存率は数日間にわたって80%以上を維持しました。
将来の細胞工学にとっての意義
簡潔に言えば、本研究はドロップレットに封入した細胞を巧妙に設計された詰まりに強いマイクロチャネルアレイで穏やかに圧迫することで、ほぼすべての細胞に遺伝的貨物を搭載しつつ大部分の細胞を生存させ、産業的に妥当な速度でこれを行えることを示しています。プラットフォームは異なる分子や細胞種に対応し、標準的な非ウイルス法と競合またはそれを上回る性能を示し、チャネルやドロップレット生成器を増やすことでスケールアップできます。細胞回収プロセスを改善すれば、このアプローチは治療用に改変された細胞を製造するための実用的な主力手法となる可能性があり、大規模な細胞集団への信頼性の高い定量的導入を必要とする基礎研究にも汎用的に使えるツールとなり得ます。
引用: Liu, Q., Chung, A.J. Parallelized droplet microfluidic mechanoporation enables robust and clogging-resistant intracellular gene delivery. Microsyst Nanoeng 12, 157 (2026). https://doi.org/10.1038/s41378-026-01273-6
キーワード: マイクロフルイディクスによる遺伝子導入, ドロップレット機械穿孔, 細胞内mRNAトランスフェクション, CRISPRによる細胞改変, 詰まりに強いマイクロデバイス