Clear Sky Science · pl
Równoległa mikrofluidyczna mechanoporacja kroplowa umożliwia wydajne i odpornie na zatykanie wewnątrzkomórkowe dostarczanie genów
Dlaczego to ma znaczenie dla przyszłych leków
Wiele najciekawszych nowych terapii — takich jak edycja genów czy terapie oparte na mRNA — zależy od bezpiecznego wprowadzenia wrażliwych biomolekuł do wnętrza żywych komórek. Obecne metody bywają potężne, ale często uszkadzają komórki, działają nieregularnie w różnych typach komórek lub trudno je skalować do miliardów komórek potrzebnych w terapiach. W artykule przedstawiono nowe podejście oparte na mikrochipie, które dostarcza materiał genetyczny do komórek wydajnie, delikatnie i przy bardzo wysokiej przepustowości, rozwiązując przy tym uporczywy problem praktyczny: zapychanie i awarie urządzeń podczas pracy.
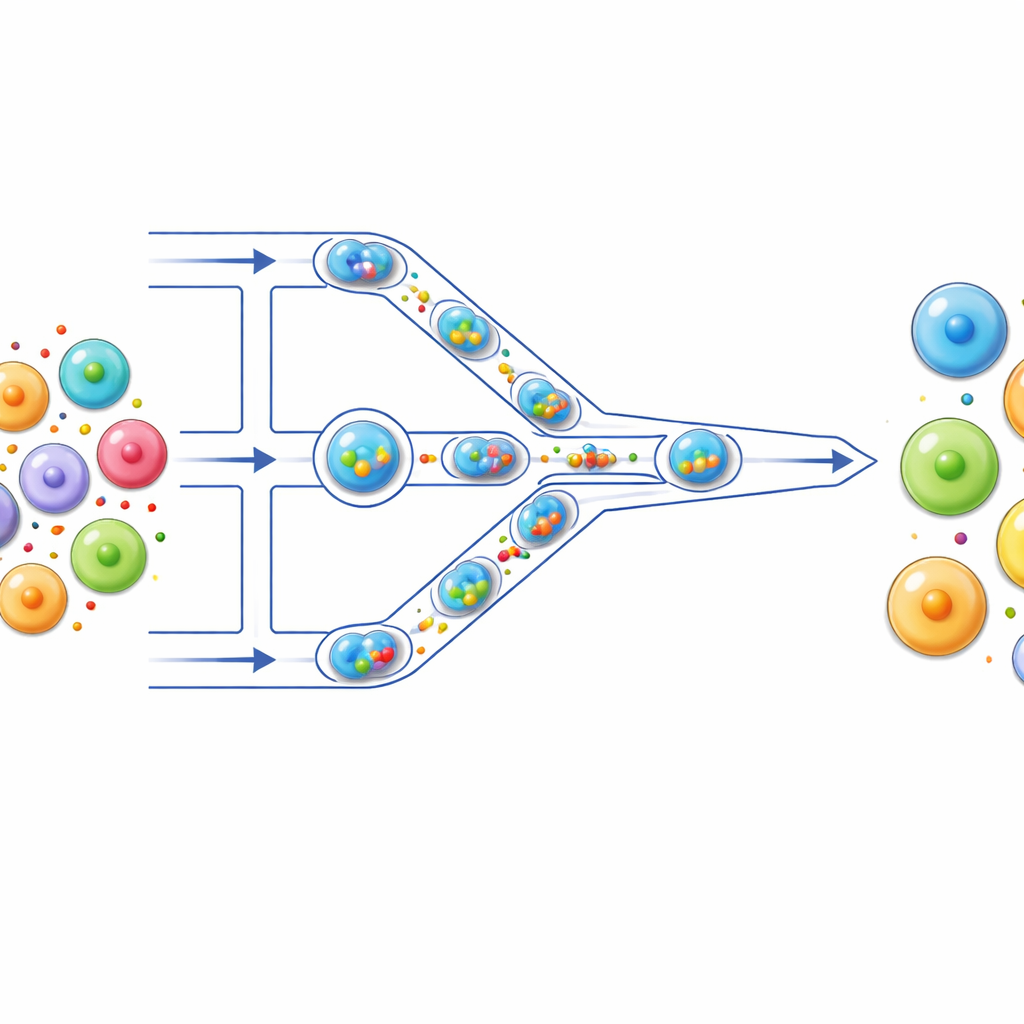
Maleńka linia montażowa dla komórek
Autorzy zbudowali mikrofluidyczną „linię montażową”, w której komórki przemieszczają się włosowato cienkimi kanałami na przezroczystym chipie. Najpierw każda komórka jest zapakowana razem z ładunkiem — na przykład barwnikiem fluorescencyjnym, mRNA lub składnikami CRISPR — wewnątrz mikroskopijnej kropli wody otoczonej olejem. Krople pełnią rolę oddzielnych naczyń reakcyjnych, izolując każdą komórkę z jej ładunkiem. Gdy krople są przepychane wzdłuż kanału, napotykają serię wąskich zwężeń mniejszych niż same komórki. Gdy kropla przeciska się przez zwężenie, komórka wewnątrz jest chwilowo odkształcana, a następnie ma czas się zrelaksować — cykl powtarza się kilkakrotnie, gdy przechodzi kolejne zwężenia.
Jak delikatne ściskanie otwiera drogę do wnętrza komórki
Gdy miękka komórka jest zmuszona przejść przez zwężenie węższe niż jej średnica, jej błona się rozciąga, tworząc tymczasowe nanoodstępy. Ponieważ komórka znajduje się w kropli poruszającej się szybko przez zwężenie, przepływ płynu po powierzchni komórki wypycha cząsteczki ładunku przez te maleńkie otwory do wnętrza komórki. Po opuszczeniu przez kroplę wąskiego obszaru komórka wraca do swojego okrągłego kształtu, a błona się zamyka, zatrzymując ładunek wewnątrz. Obrazowanie z dużą prędkością i pomiary ilościowe wykazały, że wyższe prędkości przepływu i starannie dobrane rozmiary zwężeń zwiększają rozciąganie błony i skuteczność dostarczania, ale badacze dostroili te parametry tak, by większość komórek — ponad 80% — pozostała żywa i zdrowa.
Inteligentny projekt odporny na zatory
Główną barierą stosowania takich chipów poza laboratorium jest zatykanie: kurz, skupiska komórek lub fragmenty materiału mogą zablokować pojedynczy wąski kanał i wyłączyć system. Aby temu zaradzić, zespół ułożył wiele zwężeń równolegle i połączył je kanałami obejściowymi, które pozwalają przepływowi omijać przeszkody. Ten równoległy, połączony układ stabilizuje ciśnienie wewnątrz chipa i utrzymuje ruch kropli nawet wtedy, gdy niektóre ścieżki są częściowo zablokowane. Testy porównujące chipy z obejściami i bez nich wykazały, że nowy projekt nie tylko utrzymuje wysoką skuteczność dostarczania podczas zdarzeń zapchania, ale także zwiększa ilość materiału otrzymywaną przez każdą komórkę, przy jedynie umiarkowanym wpływie na przeżywalność komórek.
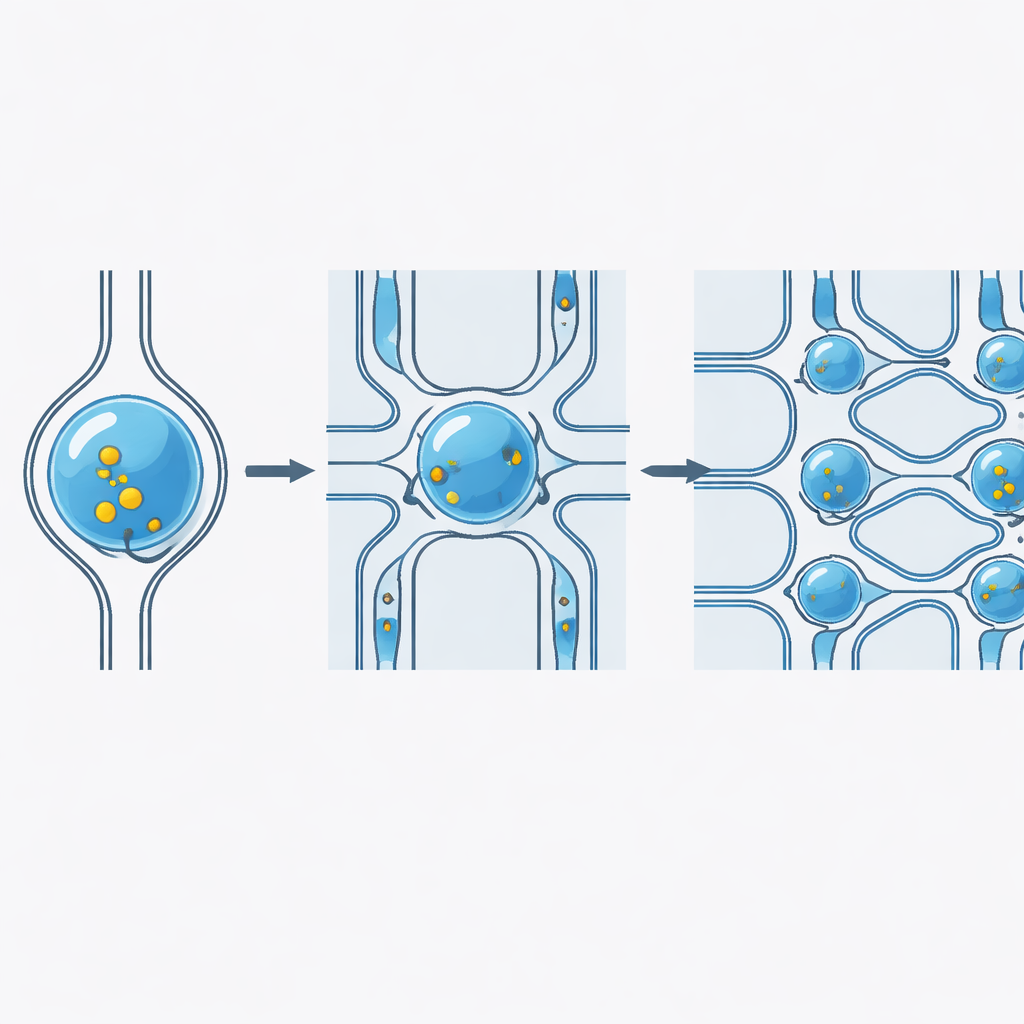
Działa dla różnych ładunków, typów komórek i prędkości
Badacze systematycznie sprawdzili, jak platforma zachowuje się w warunkach zbliżonych do rzeczywistych. Dostarczali molekuły fluorescencyjne o bardzo różnych rozmiarach, od małych barwników po duże polimery, i konsekwentnie osiągali skuteczność dostarczania powyżej 98%, przy czym ilość wchodząca do każdej komórki była kontrolowana przez stężenie ładunku. Chip działał na szeregu ludzkich i zwierzęcych linii komórkowych, w tym komórkach pochodzących z krwi i komórkach adhezyjnych, poprzez dostosowanie szerokości zwężenia do rozmiaru i sztywności komórek. Wydajność pozostawała stabilna nawet podczas przetwarzania do 100 milionów komórek na godzinę, co wskazuje, że urządzenie może obsłużyć liczby komórek wymagane w terapiach komórkowych bez utraty skuteczności czy żywotności komórek.
Od świecących białek do edytowanych genów
Aby wykazać praktyczny wpływ, autorzy dostarczyli mRNA kodujące białko fluorescencyjne do komórek białaczkowych i porównali swoją metodę z dwiema powszechnymi technikami niewirusowymi: transfekcją lipidową i elektroporacją. Ich chip wykorzystujący ściskanie kropli dorównywał lub przewyższał elektroporację zarówno pod względem odsetka komórek ekspresujących białko, jak i intensywności ekspresji, przy jednoczesnym utrzymaniu większej liczby żywych komórek niż przy obu alternatywach. Następnie użyli platformy do dostarczenia kompleksów CRISPR/Cas9 do komórek T w celu wyłączenia kluczowego receptora powierzchniowego. Edycja zadziałała w ponad 99% komórek, sygnały fluorescencyjne z docelowego receptora spadły ponad dwudziestokrotnie, a żywotność komórek utrzymała się powyżej 80% przez kilka dni.
Co to oznacza dla przyszłej inżynierii komórek
Mówiąc wprost, to badanie pokazuje, że delikatne ściskanie komórek otoczonych kroplami przez sprytnie zaprojektowaną, odporną na zatykanie tablicę mikrokanalików może załadować materiał genetyczny do niemal każdej komórki, przy jednoczesnym zachowaniu większości z nich przy życiu, i robić to z prędkościami istotnymi przemysłowo. Platforma radzi sobie z różnymi molekułami i typami komórek, dorównuje lub przewyższa standardowe metody niewirusowe i można ją skalować przez dodanie większej liczby kanałów i generatorów kropli. Przy udoskonalonych etapach odzyskiwania komórek podejście to mogłoby stać się praktycznym narzędziem produkcyjnym do wytwarzania zmodyfikowanych komórek do terapii, a także wszechstronnym narzędziem dla badań podstawowych wymagających niezawodnego, ilościowego dostarczania do dużych populacji komórek.
Cytowanie: Liu, Q., Chung, A.J. Parallelized droplet microfluidic mechanoporation enables robust and clogging-resistant intracellular gene delivery. Microsyst Nanoeng 12, 157 (2026). https://doi.org/10.1038/s41378-026-01273-6
Słowa kluczowe: dostarczanie genów w mikrofluidyce, mechanoporacja kroplowa, transfekcja mRNA do wnętrza komórki, inżynieria komórek CRISPR, urządzenia mikrofluidyczne odporne na zatykanie