Clear Sky Science · ru
Параллелизированная капельная микрофлюидная механопорация обеспечивает надежную и устойчивая к засорению доставку генетического материала в клетки
Почему это важно для будущих лекарств
Многие из самых перспективных новых терапий — такие как редактирование генов и препараты на основе мРНК — зависят от безопасной доставки хрупких биомолекул внутрь живых клеток. Современные методы могут быть эффективны, но часто повреждают клетки, дают непостоянные результаты в разных типах клеток или плохо масштабируются до миллиардов клеток, необходимых для терапии. В этой работе предложен новый чип‑основанный подход, который вводит генетический материал в клетки эффективно, бережно и с очень высокой пропускной способностью, одновременно решая практическую проблему: засорение и выход устройств из строя в процессе работы.
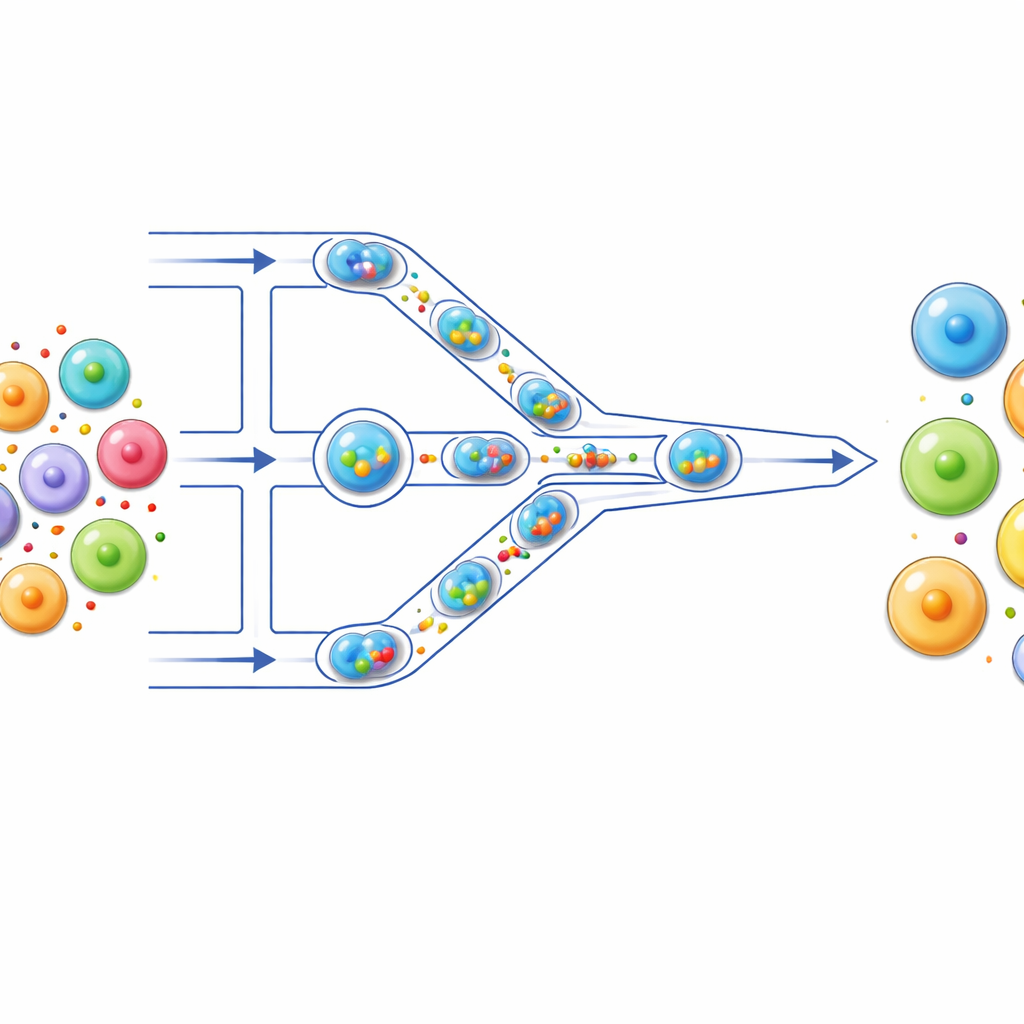
Крошечная конвейерная линия для клеток
Авторы создали микрофлюидный «конвейер», по которому клетки движутся по тончайшим каналам на прозрачном чипе. Сначала каждую клетку упаковывают вместе с грузом — например, флуоресцентным красителем, мРНК или компонентами CRISPR — внутрь микроскопической водной капли, окружённой маслом. Эти капли функционируют как индивидуальные реакционные сосуды, изолируя каждую клетку и её груз. По мере продвижения капель по каналу они сталкиваются с серией узких сужений, которые меньше самих клеток. Когда капля проходит через сужение, содержащаяся в ней клетка кратковременно деформируется, а затем восстанавливается — этот цикл повторяется несколько раз при прохождении нескольких сужений.
Как деликатное сжатие открывает «дверь» клетки
Когда мягкую клетку вынуждают пройти через сужение, уже узкое по сравнению с её диаметром, её мембрана растягивается и образует временные наноразмерные отверстия. Поскольку клетка находится внутри капли, быстро проходящей через сужение, поток жидкости проходит по поверхности клетки и проталкивает молекулы груза через эти крошечные отверстия внутрь клетки. После выхода капли из узкой области клетка возвращается к округлой форме, а мембрана снова запечатывается, оставляя груз внутри. Съёмка на высоких скоростях и количественные измерения показали, что более высокие скорости потока и тщательно подобранные размеры сужений усиливают растяжение мембраны и доставку, при этом исследователи настроили параметры так, чтобы большинство клеток — более 80% — оставались живыми и здоровыми.
Умная конструкция, устойчивая к засорам
Серьёзным препятствием для применения таких чипов вне лаборатории являются засоры: пыль, комки клеток или частицы материала могут заблокировать один узкий канал и остановить систему. Чтобы справиться с этим, команда расположила множество сужений параллельно и связала их обходными каналами, которые позволяют потоку перенаправляться вокруг препятствий. Такая параллельная, взаимосвязанная компоновка стабилизирует давление внутри чипа и поддерживает движение капель даже при частичной блокировке некоторых путей. Тесты сопоставления чипов с обходными каналами и без них показали, что новая конструкция не только сохраняет высокую эффективность доставки при событиях засорения, но и увеличивает количество материала, попадающего в каждую клетку, при умеренном влиянии на выживаемость клеток.
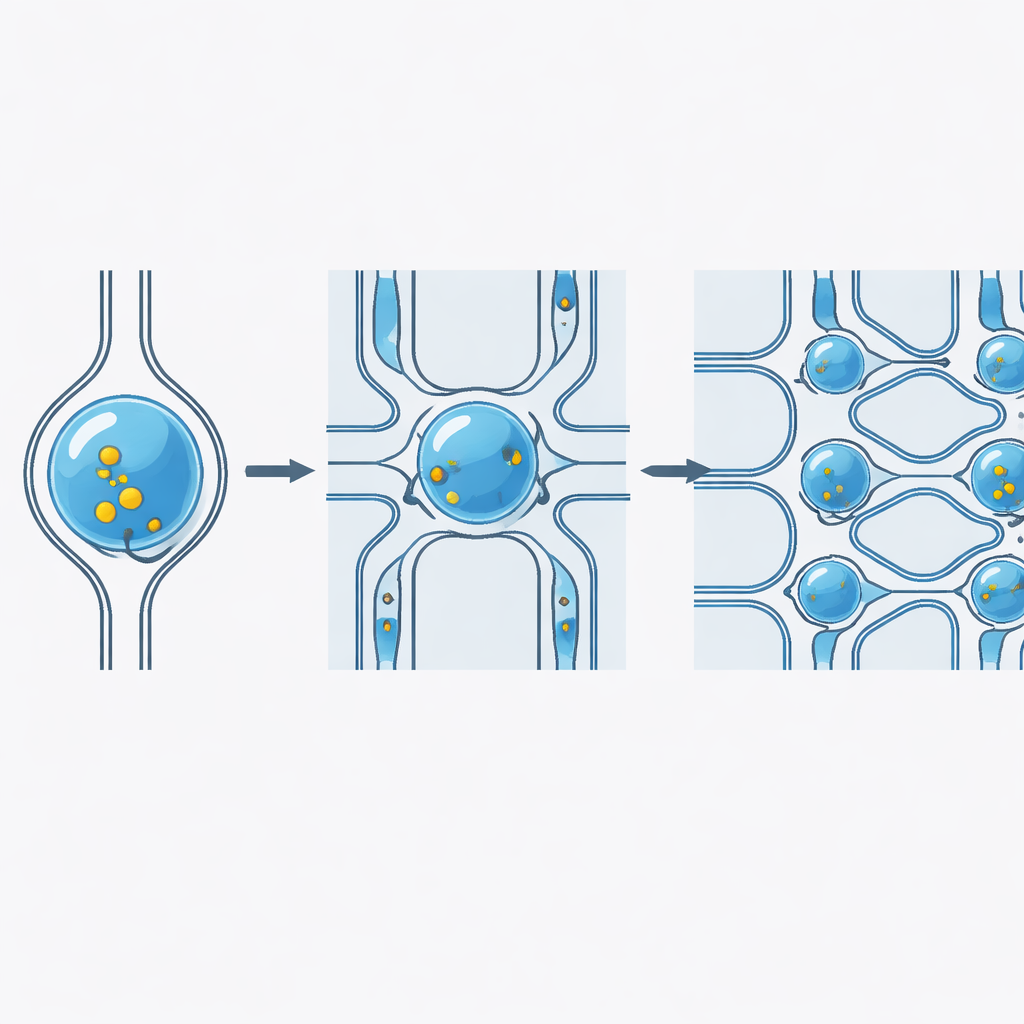
Работает с разными грузами, типами клеток и скоростями
Исследователи систематически изучали поведение платформы в условиях, близких к реальным. Они доставляли флуоресцентные молекулы очень разных размеров — от мелких красителей до крупных полимеров — и последовательно достигали эффективности доставки выше 98%, при этом количество проникшего вещества в каждую клетку контролировалось концентрацией груза. Чип работал с рядом человеческих и животных линий клеток, включая клетки, полученные из крови, и прикрепляющиеся клетки, при этом ширину сужений подбирали в соответствии с размером и жёсткостью клеток. Производительность оставалась стабильной даже при обработке до 100 миллионов клеток в час, что указывает на способность устройства обрабатывать числа клеток, требуемые для клеточных терапий, без потери эффективности или жизнеспособности.
От светящихся белков до отредактированных генов
Чтобы продемонстрировать практическое значение, авторы доставили мРНК, кодирующую флуоресцентный белок, в клетки лейкемии и сравнили свой метод с двумя распространёнными безвирусными подходами: липид‑переносящей трансфекцией и электропорацией. Их капельный чип по показателям доли клеток, экспрессирующих белок, и интенсивности экспрессии сравним или превосходил электропорацию, при этом сохранял больше клеток живыми, чем оба альтернативных метода. Затем платформу использовали для доставки комплексов CRISPR/Cas9 в Т‑клетки с целью выведения ключевого поверхностного рецептора. Редактирование сработало в более чем 99% клеток, сигналы флуоресценции от целевого рецептора упали более чем в двадцать раз, а жизнеспособность клеток оставалась выше 80% в течение нескольких дней.
Что это значит для будущей инженерии клеток
Проще говоря, в этом исследовании показано, что бережное сжатие клеток, заключённых в капли, через продуманно спроектированный массив микро каналов, устойчивых к засорам, может загрузить генетический груз почти в каждую клетку, сохранив при этом большинство из них живыми, и делать это на промышленных скоростях. Платформа справляется с разными молекулами и типами клеток, сопоставима или превосходит стандартные безвирусные методы и может быть масштабирована добавлением каналов и генераторов капель. При совершенствовании этапов восстановления клеток этот подход может стать практичным рабочим инструментом для производства инженерных клеток для терапий, а также универсальным инструментом для базовых исследований, требующих надёжной и количественной доставки в большие популяции клеток.
Цитирование: Liu, Q., Chung, A.J. Parallelized droplet microfluidic mechanoporation enables robust and clogging-resistant intracellular gene delivery. Microsyst Nanoeng 12, 157 (2026). https://doi.org/10.1038/s41378-026-01273-6
Ключевые слова: микрофлюидная доставка генов, капельная механопорация, внутриклеточная трансфекция мРНК, редактирование клеток CRISPR, микроустройства, устойчивые к засорам