Clear Sky Science · sv
Parallelliserad dropp-mikrofluidisk mekanoporering möjliggör robust och igensättningsresistent intracellulär genleverans
Varför detta är viktigt för framtidens mediciner
Många av de mest spännande nya terapierna — som genredigering och mRNA-baserade behandlingar — förutsätter att känsliga biomolekyler säkert kommer in i levande celler. Dagens metoder kan vara kraftfulla men skadar ofta celler, fungerar ojämnt mellan celltyper eller är svåra att skala upp till de miljarder celler som krävs för terapier. Denna artikel presenterar en ny chipbaserad metod som levererar genetiskt material till celler effektivt, skonsamt och i mycket hög genomströmning, samtidigt som den löser ett segdraget praktiskt problem: att enheter igensätts och slutar fungera under drift.
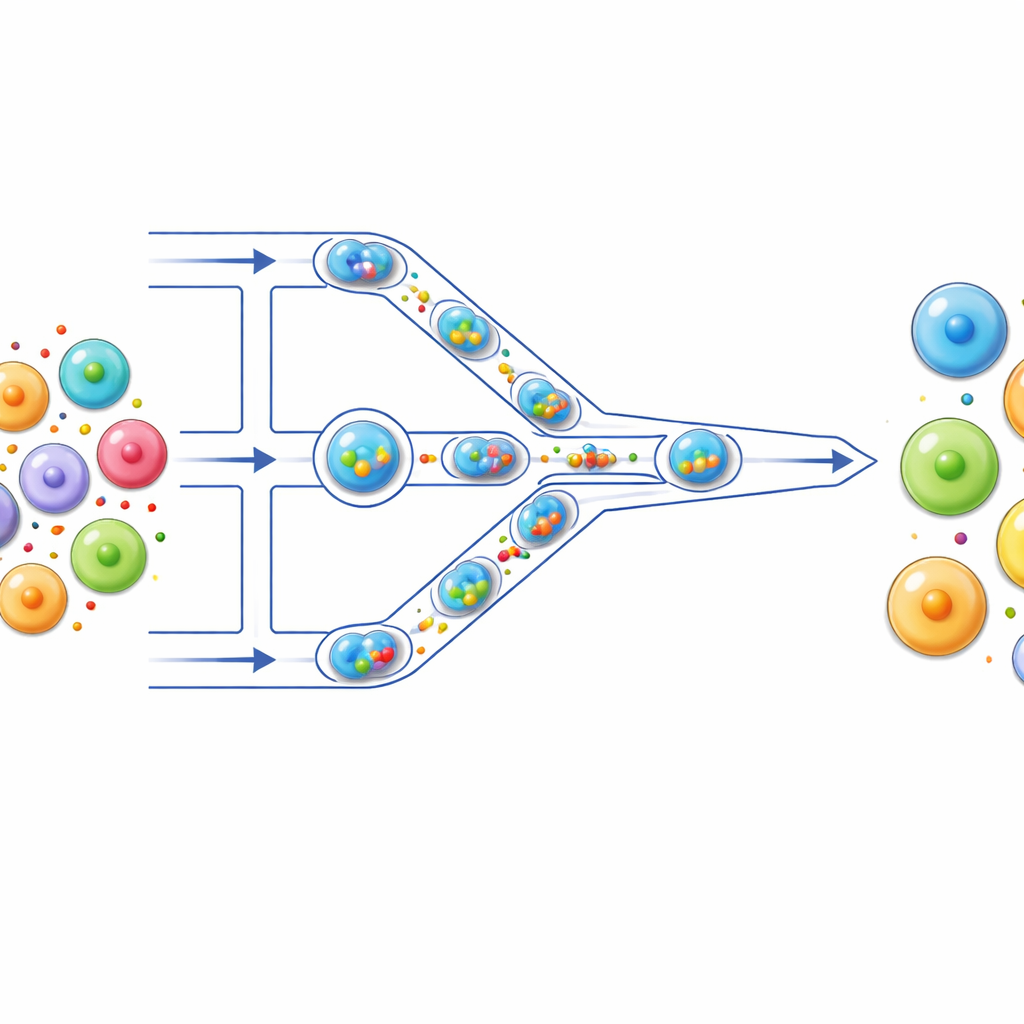
En pytteliten löpande band för celler
Författarna byggde ett mikrofluidiskt ”löpande band” där celler färdas genom hårfint tunna kanaler på en transparent chip. Först paketeras varje cell tillsammans med dess last — som fluorescerande färg, mRNA eller CRISPR-komponenter — inuti en mikroskopisk vattendroppe omsluten av olja. Dessa droppar fungerar som individuella reaktionskärl och håller varje cell och dess last isolerade. När dropparna pressas framåt i kanalen möter de en serie smalare förträngningar som är mindre än cellerna själva. När en droppe pressas igenom deformeras cellen inuti kortvarigt och tillåts sedan att återgå, en cykel som upprepas flera gånger när den passerar flera förträngningar.
Hur skonsam pressning öppnar cellens dörr
När en mjuk cell tvingas genom en förträngning som är smalare än dess diameter sträcks membranet och bildar tillfälliga nanoskaliga öppningar. Eftersom cellen är innesluten i en dropp som rör sig snabbt genom förträngningen, uppstår vätskeflöde över cellens yta som pressar lastmolekyler genom dessa små öppningar in i cellens inre. När droppen lämnar det smala området återtar cellen sin runda form och membranet försluts igen, nu med lasten infångad inuti. Högspänningsavbildning och kvantitativa mätningar visade att högre flödeshastigheter och noggrant valda förträngningsstorlekar ökar membransträckningen och leveransen, men forskarna ställde in dessa parametrar så att de flesta celler — över 80 % — förblir levande och friska.
En smart design som motstår igensättning
En stor barriär för att använda sådana chip utanför laboratoriet är igensättning: damm, cellklumpar eller materialbitar kan blockera en enskild smal kanal och stänga ner systemet. För att övervinna detta arrangerade teamet många förträngningar i parallell och kopplade dem med omledningskanaler som tillåter flödet att gå runt hinder. Denna parallella, sammankopplade layout stabiliserar trycket inne i chipet och håller dropparna i rörelse även när vissa vägar är delvis blockerade. Tester som jämförde chip med och utan omledare visade att den nya designen inte bara bibehöll hög leveranseffektivitet under igensättningshändelser utan också förbättrade hur mycket material varje cell mottog, med endast måttliga effekter på cellöverlevnad.
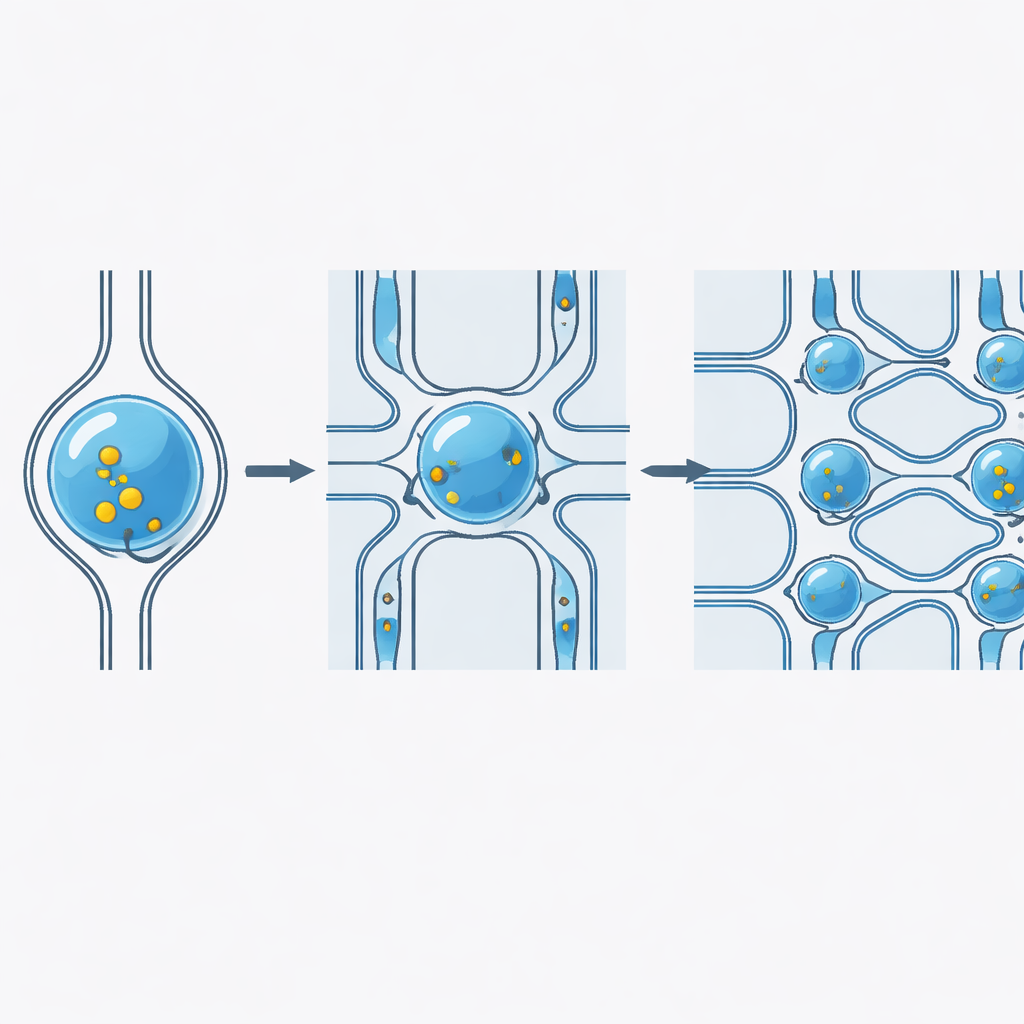
Fungerar för olika laster, celltyper och hastigheter
Forskarna undersökte systematiskt hur plattformen beter sig under verkliga förhållanden. De levererade fluorescerande molekyler i mycket olika storlekar, från små färgämnen till stora polymerer, och uppnådde konsekvent leveranseffektivitet över 98 %, där mängden som kom in i varje cell styrdes av lastkoncentrationen. Chipet fungerade på en rad mänskliga och djuriska cellinjer, inklusive blod‑ härledda och adherenta celler, genom att justera förträngningsbredden för att matcha cellstorlek och styvhet. Prestandan förblev stabil även vid bearbetning av upp till 100 miljoner celler per timme, vilket indikerar att enheten kan hantera de cellantal som krävs för cellbaserade terapier utan att förlora effektivitet eller cellviabilitet.
Från lysande proteiner till redigerade gener
För att visa praktisk påverkan levererade författarna mRNA som kodar för ett fluorescerande protein till leukemiceller och jämförde sin metod med två vanliga icke-virala tekniker: lipidbaserad transfektion och elektroporering. Deras dropp‑pressningschip matchade eller överträffade elektroporering både vad gäller andel celler som uttryckte proteinet och uttrycksintensitet, samtidigt som fler celler hölls vid liv än med något av alternativen. De använde sedan plattformen för att leverera CRISPR/Cas9-genredigeringskomplex till T‑celler för att slå ut en viktig ytreceptor. Redigeringen lyckades i över 99 % av cellerna, med fluorescenssignaler från den målinriktade receptorn som sjönk mer än tjugofalt, och cellviabiliteten hölls över 80 % under flera dagar.
Vad detta betyder för framtida cellteknik
Enkelt uttryckt visar denna studie att skonsamt pressande av dropp‑inkapslade celler genom en smart utformad, igensättningsresistent mikrokanałsarray kan ladda genetisk last i nästan varje cell samtidigt som de flesta förblir levande, och att detta kan ske i industriellt relevanta hastigheter. Plattformen hanterar olika molekyler och celltyper, matchar eller överträffar standard icke‑virala metoder och kan skalas upp genom att lägga till fler kanaler och droppgeneratorer. Med förbättrade steg för cellåtervinning skulle detta tillvägagångssätt kunna bli ett praktiskt arbetsdjur för tillverkning av konstruerade celler för terapier, liksom ett mångsidigt verktyg för grundforskning som behöver pålitlig, kvantitativ leverans till stora cellpopulationer.
Citering: Liu, Q., Chung, A.J. Parallelized droplet microfluidic mechanoporation enables robust and clogging-resistant intracellular gene delivery. Microsyst Nanoeng 12, 157 (2026). https://doi.org/10.1038/s41378-026-01273-6
Nyckelord: mikrofluidisk genleverans, dropp-mekanoporering, intracellulär mRNA-transfektion, CRISPR-cellteknik, igensättningsresistenta mikroanordningar