Clear Sky Science · he
מכנופורציה מיקרו-נוזלית מקבילית באמצעות טיפות מאפשרת העברת גנים תוך-תאית יציבה ועמידה לסתימות
מדוע זה חשוב לתרופות העתיד
הרבה מהטיפולים החדשים המרגשים — כמו עריכת גנים וטיפולים מבוססי mRNA — מסתמכים על היכולת להעביר מולקולות ביולוגיות עדינות לתוך תאים חיים בצורה בטוחה. השיטות הקיימות יכולות להיות עוצמתיות אך לעיתים פוגעות בתאים, פועלות באופן לא אחיד בין סוגי תאים שונים או שקשה להגדילן למיליארדי תאים הנדרשים לטיפולים. מאמר זה מציג שיטה חדשה מבוססת שבב שמעבירה חומר גנטי לתאים בצורה יעילה, עדינה ובקצב גבוה מאוד, ובו בזמן פותרת בעיה מעשית עקשנית: הסתימות וכשלי המכשיר במהלך הפעולה.
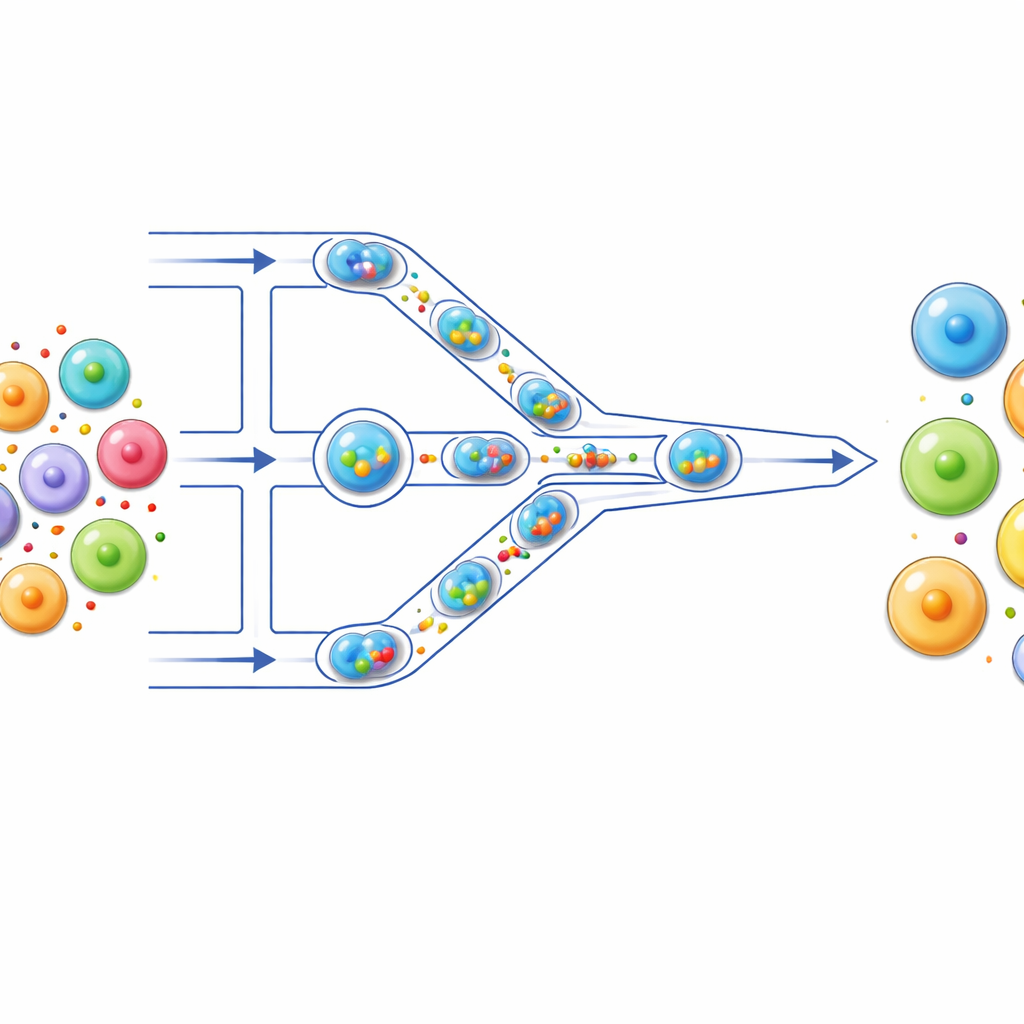
קו ייצור זעיר לתאים
החוקרים בנו "קו ייצור" מיקרו-נוזלי שבו תאים נוסעים בערוצים דקיקים על שבב שקוף. קודם כל, כל תא נארז יחד עם המטען שלו — כמו צבע זוהר, mRNA או רכיבי CRISPR — בתוך טיפה מיקרוסקופית של מים מוקפת שמן. טיפות אלה משמשות ככלים תגובתיים בודדים, השומרות על בידודו של כל תא ומטענו. כשהטיפות נדחפות לאורך הערוץ, הן פוגשות סדרה של ההיצעוות צרות שקטנות מגודל התאים עצמם. כשהטיפה נדחסת ונעשרת דרך ההיצע, התא שבתוכה מעוות לזמן קצר ואז נרפא, מעגל שחוזר על עצמו מספר פעמים כשהטיפה עוברת מספר היצעוות.
איך לכידה עדינה פותחת את דלת התא
כאשר תא רך נדחס דרך היצע צר שמצטמצם מקוטרו, הממברנה שלו נמתחת ונפתחות פתחים זמניים בקנה-מידה ננו. מאחר שהתא נמצא בתוך טיפה שנעה במהירות דרך ההיצע, זרימת נוזל חוצה את פני התא ודוחפת מולקולות מטען דרך הפתחים הזעירים אל פנים התא. כשהטיפה יוצאת מאזור ההיצע, התא חוזר לצורתו העגולה והממברנה נסתמת מחדש, כשכעת המטען כלוא בפנים. הדמיה במהירות גבוהה ומדידות כמותיות הראו שמהירויות זרימה גבוהות יותר וגודל היצע מותאם מגדילים את מתיחת הממברנה והעברה, אך החוקרים כיוונו פרמטרים אלה כך שרוב התאים — מעל 80% — יישארו חיים ובריאים.
עיצוב חכם העמיד לסתימות
מחסום מרכזי לשימוש בשבבים כאלה מחוץ למעבדה הוא הסתימות: אבק, גושי תאים או חלקיקים עלולים לחסום ערוץ צר יחיד ולשעתק את המערכת. כדי להתגבר על זאת, הצוות סידר הרבה היצעוות במקביל וקשר ביניהן ערוצי עקיפה שמאפשרים לזרימה לעקוף חסימות. פריסת המקביליות והקישוריות הזו מייצבת את הלחץ בתוך השבב ושומרת על תנועת הטיפות גם כאשר חלק מהנתיבים חסומים חלקית. בדיקות המשוות שבבים עם ובלי ערוצי עקיפה הראו שהעיצוב החדש לא רק שומר על יעילות ההעברה גבוהה במהלך אירועי הסתימה, אלא גם שיפר את כמות החומר שכל תא קיבל, עם השפעות צנועות על הישרדות התאים.
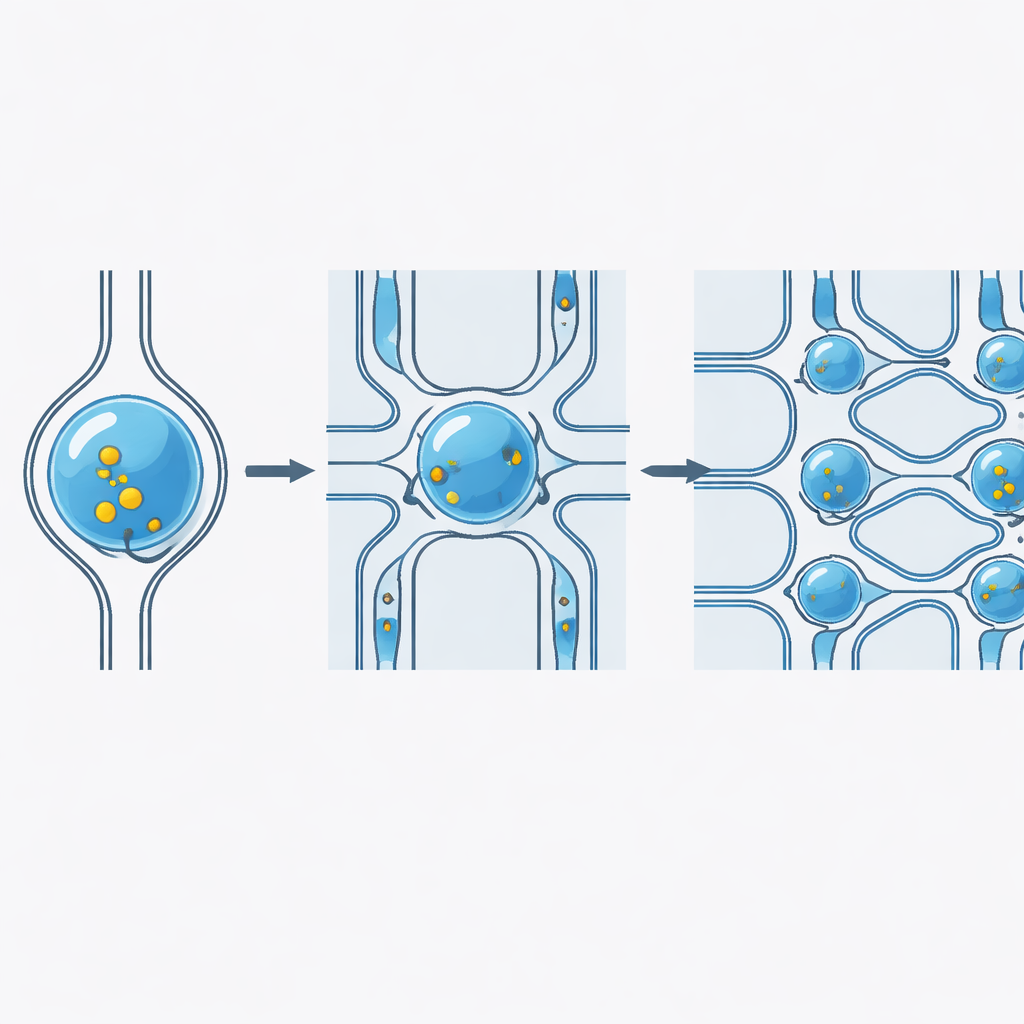
עובד על מטענים, סוגי תאים ומהירויות שונות
החוקרים בחנו באופן שיטתי כיצד הפלטפורמה מתנהגת בתנאי עולם-אמיתי. הם העבירו מולקולות זוהרות בגדלים שונים מאוד, מצבעים קטנים ועד פולימרים גדולים, והשיגו בעקביות יעילות העברה מעל 98%, כשהכמות הנכנסת לכל תא נשלטת על-ידי ריכוז המטען. השבב עבד על מגוון של תאי אדם ובעלי חיים, כולל תאי דם ותאים דביקים, על-ידי כוונון רוחב ההיצע לפי גודל וקשיחות התא. הביצועים נשארו יציבים גם בעיבוד של עד 100 מיליון תאים לשעה, מה שמצביע על יכולת המכשיר לטפל במספרי התאים הנדרשים לטיפולי תאים מבלי לאבד יעילות או ויאביליות של התאים.
מפרוטאינים זוהרים ועד גנים נערכים
כדי להדגים השפעה מעשית, המחברים העבירו mRNA המקודד לחלבון זוהר לתאי לוקמיה והשוו את שיטתם לשתי טכניקות לא-ויראליות נפוצות: טרנספקציה מבוססת שומנים ואלקטרופורציה. השבב המבוסס סחיטת הטיפות השיג תוצאות שוות או גבוהות מאלקטרופורציה הן באחוז התאים המביעים את החלבון והן בעוצמת הביטוי, תוך שמירה על יותר תאים בחיים מאשר כל אחת מהחלופות. לאחר מכן השתמשו בפלטפורמה כדי להעביר קומפלקסי עריכת גנים CRISPR/Cas9 לתאי T כדי להשבית קולט פני-משטח מרכזי. העריכה הצליחה בלמעלה מ-99% מהתאים, עם ירידה של יותר מעשרים-פעמיים באותות הפלורסצנטיים של הקולטן הממוקד, והוויאביליות של התאים נשמרה מעל 80% לאורך מספר ימים.
מה משמעות הדבר להנדסת תאים בעתיד
במונחים פשוטים, המחקר מראה כי סחיטת תאים בתוך טיפות דרך מערך ערוצים חכם ועמיד לסתימות יכולה לטעון מטען גנטי כמעט לכל תא תוך שמירה על רובם בחיים, ובמהירויות הרלוונטיות לתעשייה. הפלטפורמה מטפלת במולקולות וסוגי תאים שונים, מתחרה או עולה על שיטות לא-ויראליות סטנדרטיות, וניתנת להגדלה באמצעות הוספת ערוצים ומפיקי טיפות. עם שיפורים בשלבי השבה של התאים, הגישה הזו עשויה להפוך לכלי עבודה מעשי לייצור תאים מהונדסים לטיפולים, וכן לכלי רב-תכליתי למחקר בסיסי שדורש העברה אמינה וכמותית לאוכלוסיות תאים גדולות.
ציטוט: Liu, Q., Chung, A.J. Parallelized droplet microfluidic mechanoporation enables robust and clogging-resistant intracellular gene delivery. Microsyst Nanoeng 12, 157 (2026). https://doi.org/10.1038/s41378-026-01273-6
מילות מפתח: העברת גנים מיקרו-נוזלית, מכנופורציה בטיפות, טרנספקציה של mRNA תוך-תאית, הנדסת תאים עם CRISPR, מכשירים מיקרו-נוזליים עמידים לסתימות