Clear Sky Science · tr
Paralelleştirilmiş damlacık mikroakışkan mekanoporasyonu, sağlam ve tıkanmaya dirençli hücre içi gen aktarımı sağlar
Geleceğin ilaçları için neden önemli
En heyecan verici yeni tedavilerden birçoğu — gen düzenleme ve mRNA temelli tedaviler gibi — hassas biyomolekülleri canlı hücrelerin içine güvenle sokmaya dayanıyor. Bugünün yöntemleri güçlü olabilse de genellikle hücrelere zarar veriyor, hücre tipleri arasında tutarsız çalışıyor veya terapiler için gereken milyarlarca hücreye ölçeklenmesi zor oluyor. Bu makale, genetik materyali hücrelere verimli, nazik ve çok yüksek verimde ulaştıran mikroçip tabanlı yeni bir yaklaşım sunuyor; ayrıca operasyon sırasında cihazların tıkanması ve çalışamaz hale gelmesi gibi inatçı bir pratik sorunu da çözüyor.
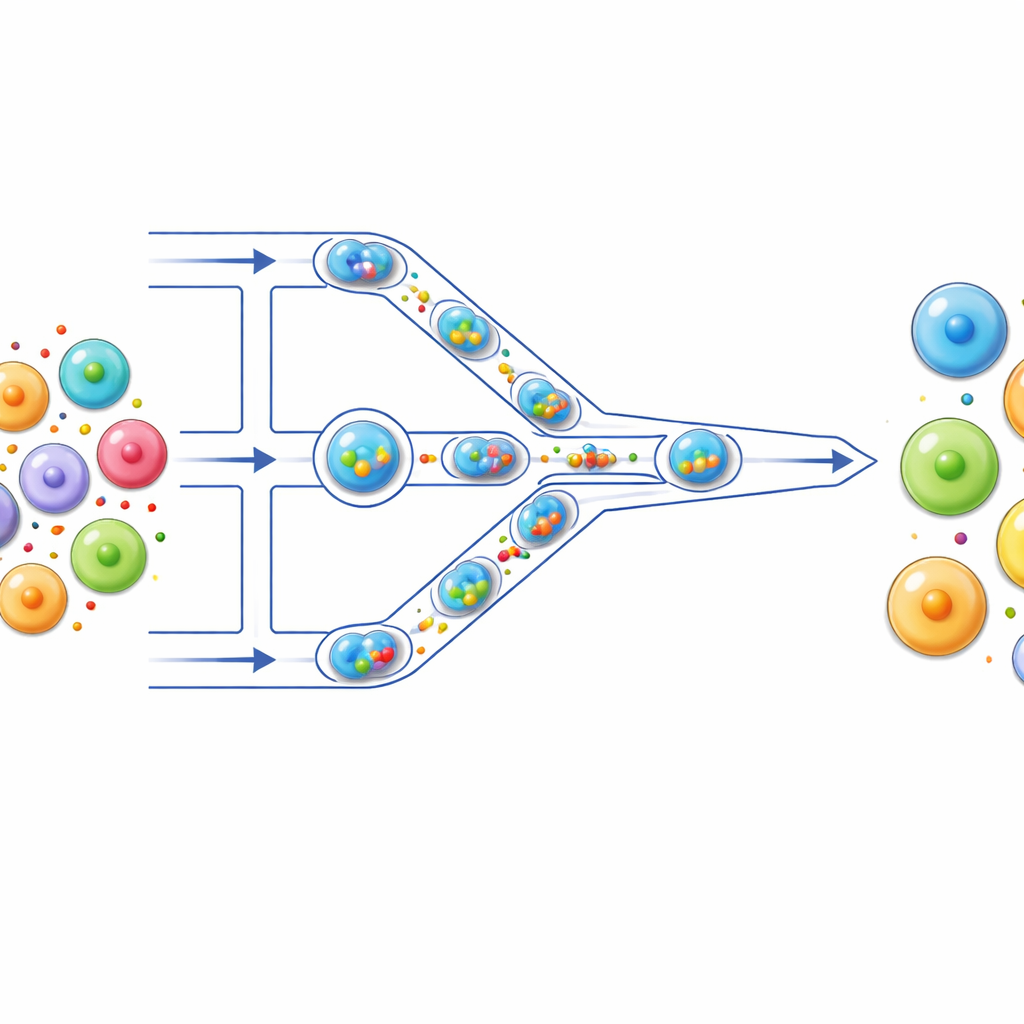
Hücreler için küçük bir montaj hattı
Yazarlar, hücrelerin şeffaf bir çip üzerindeki kıl inceliğindeki kanallar boyunca ilerlediği bir mikroakışkan “montaj hattı” kurdular. Önce her hücre, floresan boya, mRNA veya CRISPR bileşenleri gibi yüküyle birlikte, yağ ile çevrelenmiş mikroskobik bir su damlacığının içine paketlenir. Bu damlacıklar, her hücreyi ve yükünü izole eden bireysel reaksiyon kapları gibi davranır. Damlacıklar kanal boyunca itildiğinde, hücrelerden daha küçük dar bir dizi sıkışma bölgesiyle karşılaşırlar. Damlacık sıkışıp geçtiğinde içindeki hücre kısa süreliğine şekil değiştirir ve rahatlamasına izin verilir; bu döngü, birden çok daralmadan geçerken birkaç kez tekrarlanır.
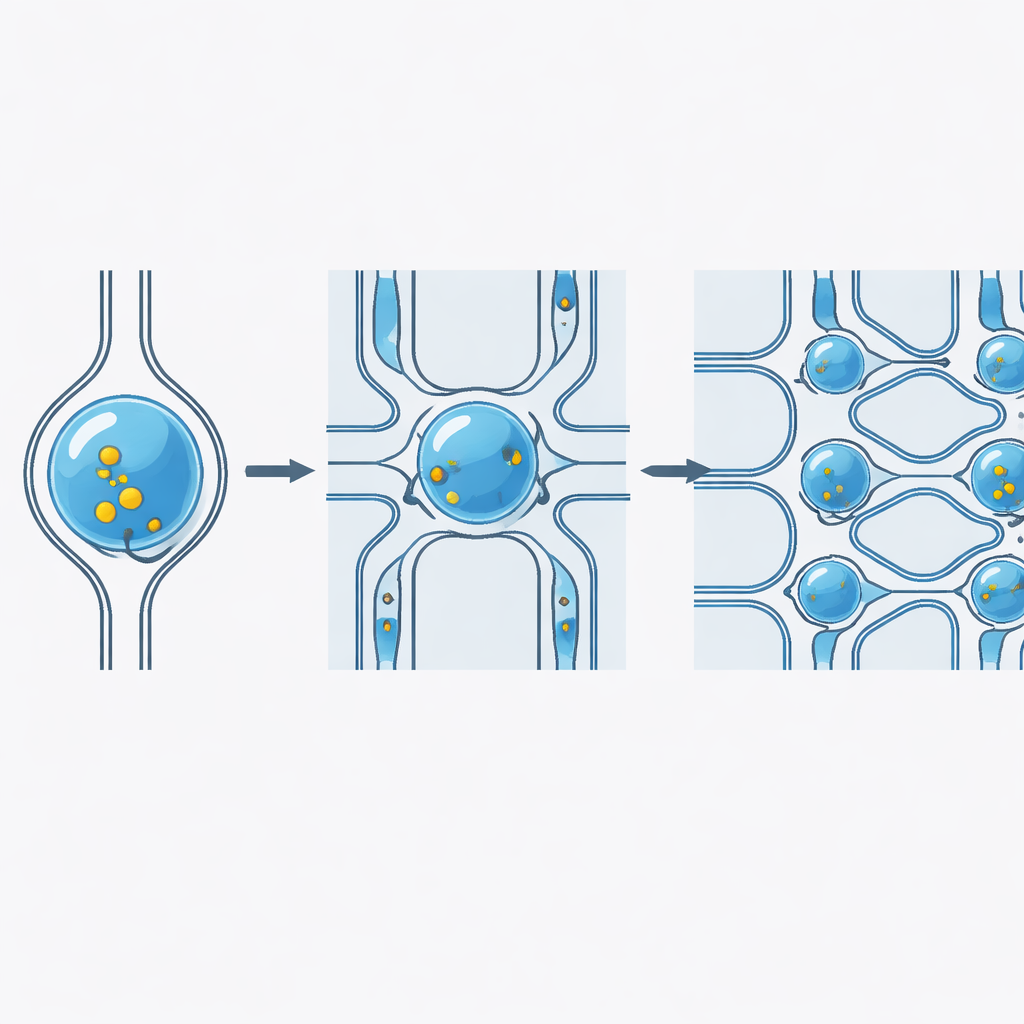
Nazik sıkıştırma hücre kapısını nasıl açar
Yumuşak bir hücre, çapından daha dar bir daralmadan zorlanarak geçirildiğinde, zar gerilir ve geçici nanoskaladaki açıklıklar oluşur. Hücre, daralmadan hızla geçen bir damlacığın içinde bulunduğundan, sıvı hücre yüzeyinde akış yapar ve yük moleküllerini bu küçük açıklıklardan hücre içine iter. Damlacık dar bölgeden çıktıktan sonra hücre tekrar yuvarlak şekline döner ve zar yeniden kapanır; böylece yük hücre içinde hapsolmuş olur. Yüksek hızlı görüntüleme ve nicel ölçümler, daha yüksek akış hızlarının ve dikkatle seçilmiş daralma boyutlarının zar gerilmesini ve aktarımı artırdığını gösterdi, ancak araştırmacılar bu parametreleri hücrelerin çoğunun — %80'in üzerinde — canlı ve sağlıklı kalacağı şekilde ayarladılar.
Tıkanmalara dirençli akıllı bir tasarım
Bu tür çipleri laboratuvar dışında kullanmanın büyük bir engeli tıkanmadır: toz, hücre kümeleri veya malzeme parçacıkları tek bir dar kanalı tıkayarak sistemi durdurabilir. Bunu aşmak için ekip, birçok daralmayı paralel olarak düzenledi ve engeller etrafında akışın yeniden yönlenmesine izin veren baypas kanallarıyla bağladı. Bu paralel, birbirine bağlı düzen, çip içindeki basıncı stabilize eder ve bazı yollar kısmen tıkansa bile damlacıkların hareket etmesini sağlar. Baypaslı ve baypassız çipleri karşılaştıran testler, yeni tasarımın tıkanma olayları sırasında sadece aktarım verimliliğini yüksek tutmakla kalmadığını, aynı zamanda her hücrenin aldığı materyal miktarını da artırdığını ve hücre canlılığı üzerinde sadece ılımlı etkiler olduğunu gösterdi.
Farklı yükler, hücre tipleri ve hızlarda çalışır
Araştırmacılar platformun gerçek dünya koşullarında nasıl davrandığını sistematik olarak incelediler. Küçük boyutlu boyalardan büyük polimerlere kadar çok farklı boyutlardaki floresan molekülleri verdiler ve her durumda aktarım verimliliğini tutarlı şekilde %98'in üzerinde elde ettiler; her hücreye giren miktar, yük konsantrasyonuyla kontrol edilebiliyordu. Çip, hücre boyutu ve sertliğine uymak için daralma genişliğini ayarlayarak kan kökenli ve adhezan hücreler dahil olmak üzere çeşitli insan ve hayvan hücre hatlarında çalıştı. Performans, saatte 100 milyon hücreye kadar işlem yapıldığında bile stabil kaldı; bu da cihazın hücre tabanlı terapiler için gereken hücre sayılarını verim veya hücre yaşamsallığını kaybetmeden işleyebileceğini gösteriyor.
Parlayan proteinlerden düzenlenen genlere
Pratik etkiyi göstermek için yazarlar lösemi hücrelerine floresan protein kodlayan mRNA verdiler ve yöntemlerini iki yaygın viral olmayan teknikle karşılaştırdılar: lipit tabanlı transfeksiyon ve elektroporasyon. Damlacık‑sıkıştırma çipleri, proteini ifade eden hücre oranı ve ifade yoğunluğu açısından elektroporasyonla eşleşti veya onu aştı, aynı zamanda her iki alternatiften daha fazla hücreyi canlı tutmayı başardı. Daha sonra platformu, T hücrelerine kritik bir yüzey reseptörünü hedefleyerek CRISPR/Cas9 gen düzenleme kompleksleri taşımak için kullandılar. Düzenleme hücrelerin %99'undan fazlasında işe yaradı, hedeflenen reseptörden gelen floresan sinyaller yirmiden fazla kat azaldı ve hücre canlılığı birkaç gün boyunca %80'in üzerinde kaldı.
Geleceğin hücre mühendisliği için ne anlama geliyor
Basitçe söylemek gerekirse, bu çalışma damlacık içinde kapsüllenmiş hücreleri tıkanmaya dayanıklı, zeki tasarlanmış mikrokanal dizisi boyunca nazikçe sıkıştırmanın, genetik yükü neredeyse her hücreye yükleyebileceğini ve hücrelerin çoğunu canlı tutabileceğini; üstelik bunu endüstriyel düzeydeki hızlarda yapabileceğini gösteriyor. Platform farklı moleküller ve hücre tipleriyle başa çıkıyor, standart viral olmayan yöntemlerle rekabet ediyor veya onları geride bırakıyor ve daha fazla kanal ve damlacık üreteci eklenerek ölçeklendirilebiliyor. Hücre geri kazanım adımları iyileştirildiğinde, bu yaklaşım terapiler için mühendislik hücrelerin üretiminde pratik bir işçi haline gelebilir; ayrıca büyük hücre popülasyonlarına güvenilir, niceliksel aktarım gerektiren temel araştırmalar için çok yönlü bir araç olabilir.
Atıf: Liu, Q., Chung, A.J. Parallelized droplet microfluidic mechanoporation enables robust and clogging-resistant intracellular gene delivery. Microsyst Nanoeng 12, 157 (2026). https://doi.org/10.1038/s41378-026-01273-6
Anahtar kelimeler: mikroakışkan gen aktarımı, damlacık mekanoporasyonu, hücre içi mRNA transfeksiyonu, CRISPR hücre mühendisliği, tıkanmaya dayanıklı mikro cihazlar