Clear Sky Science · es
La mecanoporación microfluídica en gotas paralelizada permite una entrega intracelular de genes robusta y resistente a obstrucciones
Por qué esto importa para las medicinas del futuro
Muchas de las terapias más prometedoras —como la edición genética y los tratamientos basados en ARNm— dependen de introducir de forma segura moléculas biológicas frágiles dentro de las células vivas. Los métodos actuales pueden ser potentes, pero a menudo dañan las células, funcionan de manera inconsistente según el tipo celular o son difíciles de escalar hasta los miles de millones de células necesarios para terapias. Este artículo presenta un nuevo enfoque basado en microchips que entrega material genético a las células de forma eficaz, suave y con muy alto rendimiento, al tiempo que resuelve un problema práctico persistente: la obstrucción y fallo de los dispositivos durante la operación.
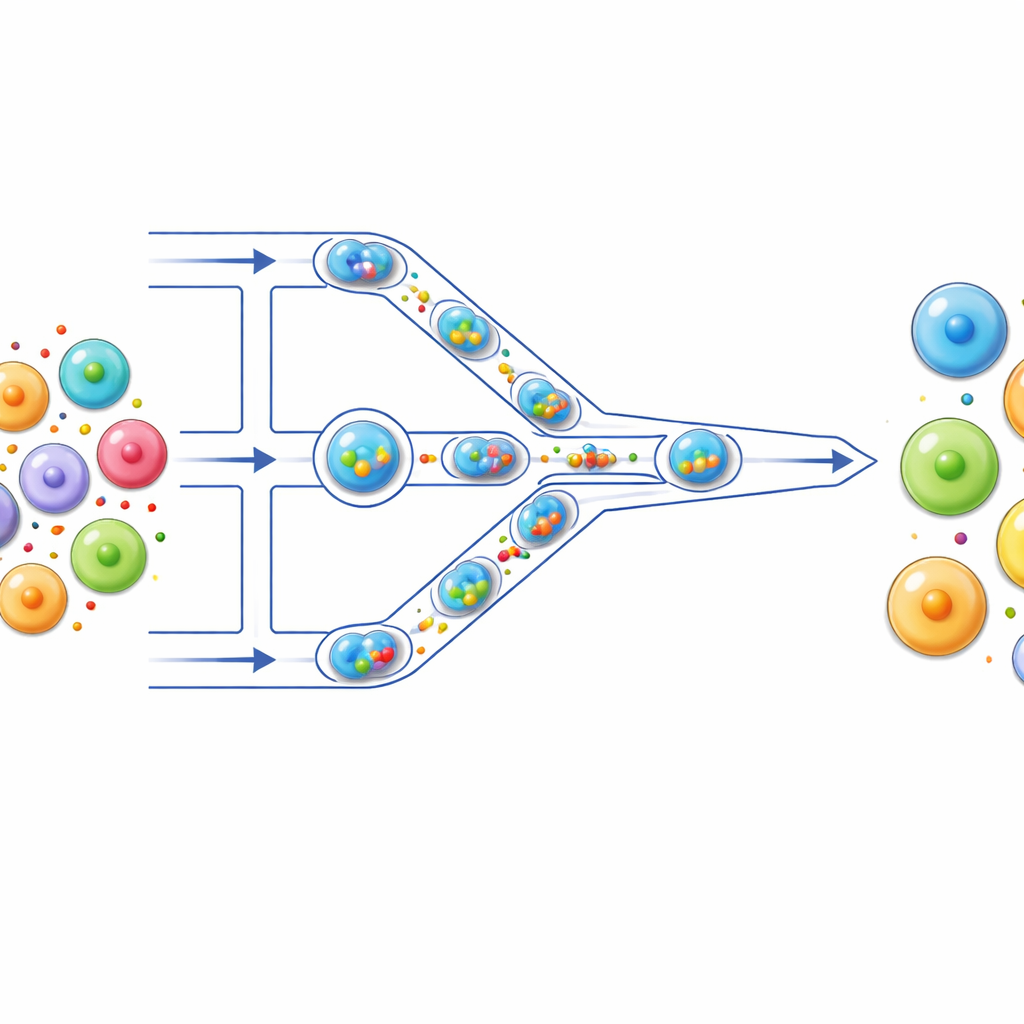
Una pequeña línea de montaje para células
Los autores construyeron una "línea de montaje" microfluídica en la que las células viajan por canales tan finos como un cabello sobre un chip transparente. Primero, cada célula se empaqueta junto con su carga —como colorante fluorescente, ARNm o componentes CRISPR— dentro de una gota microscópica de agua rodeada por aceite. Estas gotas actúan como recipientes de reacción individuales, manteniendo aisladas cada célula y su carga. A medida que las gotas son impulsadas por el canal, encuentran una serie de constricciones estrechas, más pequeñas que las propias células. Cuando una gota se aprieta para pasar, la célula dentro se deforma brevemente y luego se relaja; este ciclo se repite varias veces al atravesar múltiples constricciones.
Cómo el apriete suave abre la puerta celular
Cuando una célula blanda es forzada a pasar por una constricción más estrecha que su diámetro, su membrana se estira y se forman aperturas temporales a escala nanométrica. Porque la célula está dentro de una gota que se mueve rápidamente por la constricción, el flujo de fluido a través de la superficie celular empuja las moléculas de carga a través de esas pequeñas aberturas hacia el interior de la célula. Una vez que la gota sale de la región estrecha, la célula recupera su forma redondeada y la membrana se vuelve a sellar, con la carga ya atrapada dentro. Imágenes a alta velocidad y mediciones cuantitativas mostraron que mayores velocidades de flujo y tamaños de constricción cuidadosamente seleccionados incrementan el estiramiento de la membrana y la entrega, pero los investigadores ajustaron estos parámetros para que la mayoría de las células —más del 80%— permanecieran vivas y saludables.
Un diseño inteligente que resiste las obstrucciones
Una barrera importante para usar estos chips fuera del laboratorio es la obstrucción: polvo, cúmulos celulares o fragmentos de material pueden bloquear un único canal estrecho y paralizar el sistema. Para superar esto, el equipo dispuso muchas constricciones en paralelo y las conectó con canales de derivación que permiten que el flujo se redirija alrededor de las obstrucciones. Esta disposición paralela e interconectada estabiliza la presión dentro del chip y mantiene las gotas en movimiento incluso cuando algunos caminos están parcialmente bloqueados. Pruebas comparativas entre chips con y sin derivaciones mostraron que el nuevo diseño no solo mantuvo alta la eficiencia de entrega durante eventos de obstrucción, sino que además mejoró la cantidad de material que recibía cada célula, con solo efectos modestos sobre la supervivencia celular.
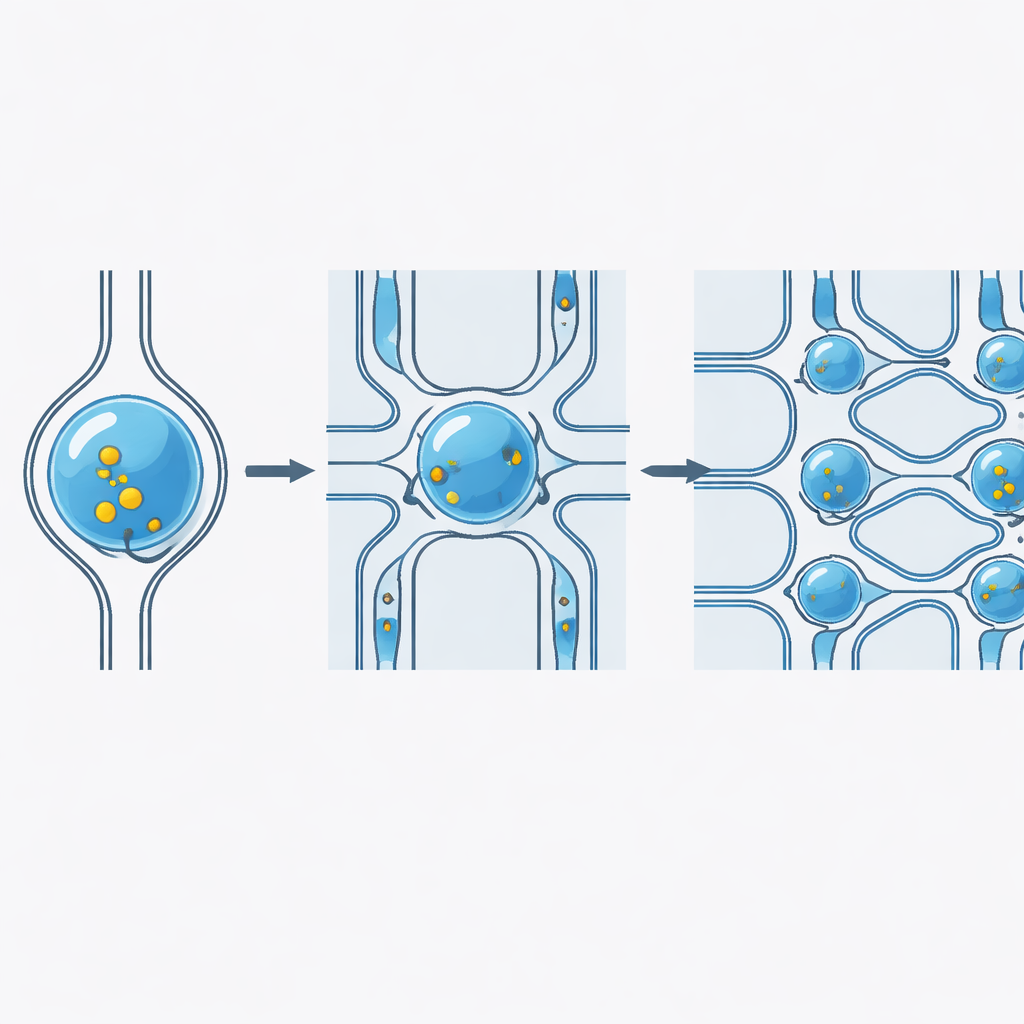
Funciona con diferentes cargas, tipos celulares y velocidades
Los investigadores examinaron sistemáticamente cómo se comporta la plataforma en condiciones del mundo real. Entregaron moléculas fluorescentes de tamaños muy distintos, desde tintes pequeños hasta polímeros grandes, y lograron de forma consistente eficiencias de entrega superiores al 98%, con la cantidad que entraba en cada célula controlada por la concentración de la carga. El chip funcionó en una gama de líneas celulares humanas y animales, incluidas células derivadas de sangre y células adherentes, ajustando el ancho de las constricciones para adaptarse al tamaño y la rigidez celular. El rendimiento se mantuvo estable incluso procesando hasta 100 millones de células por hora, lo que indica que el dispositivo puede manejar los números celulares requeridos para terapias basadas en células sin perder eficiencia ni viabilidad celular.
De proteínas fluorescentes a genes editados
Para demostrar el impacto práctico, los autores entregaron ARNm que codifica una proteína fluorescente en células de leucemia y compararon su método con dos técnicas no virales comunes: transfección basada en lípidos y electroporación. Su chip de apriete en gotas igualó o superó a la electroporación tanto en la fracción de células que expresaron la proteína como en la intensidad de la expresión, manteniendo además más células vivas que cualquiera de las alternativas. Luego usaron la plataforma para entregar complejos de edición genética CRISPR/Cas9 en células T para eliminar un receptor de superficie clave. La edición funcionó en más del 99% de las células, con señales fluorescentes del receptor objetivo disminuyendo más de veinte veces, y la viabilidad celular permaneciendo por encima del 80% durante varios días.
Qué significa esto para la ingeniería celular futura
En términos simples, este estudio muestra que apretar suavemente células encapsuladas en gotas a través de una matriz de microcanales inteligentemente diseñada y resistente a obstrucciones puede cargar material genético en casi todas las células manteniendo la mayoría de ellas vivas, y hacerlo a velocidades relevantes para la industria. La plataforma maneja diferentes moléculas y tipos celulares, iguala o supera a métodos no virales estándar y puede escalarse añadiendo más canales y generadores de gotas. Con pasos mejorados de recuperación celular, este enfoque podría convertirse en una herramienta práctica para la fabricación de células modificadas para terapias, así como en un instrumento versátil para la investigación básica que necesita una entrega fiable y cuantitativa en poblaciones celulares grandes.
Cita: Liu, Q., Chung, A.J. Parallelized droplet microfluidic mechanoporation enables robust and clogging-resistant intracellular gene delivery. Microsyst Nanoeng 12, 157 (2026). https://doi.org/10.1038/s41378-026-01273-6
Palabras clave: entrega génica microfluídica, mecanoporación en gotas, transfección intracelular de ARNm, ingeniería celular CRISPR, microdispositivos resistentes a obstrucciones